
Wetenschap
Waarom wordt bruisen waargenomen als zoutzuur wordt toegevoegd aan een gebroken stalagmiet?
De chemische reactie die plaatsvindt is als volgt:
2HCl (zoutzuur) + CaCO3 (calciumcarbonaat) → CaCl2 (calciumchloride) + H2O (water) + CO2 (kooldioxide)
Het calciumchloride en het water blijven opgelost in de oplossing, terwijl het kooldioxidegas in de atmosfeer ontsnapt. Deze reactie staat ook bekend als "zure oplossing" en is een veel voorkomend proces dat in de natuur plaatsvindt wanneer zure stoffen in contact komen met carbonaatgesteenten, zoals stalagmieten.
Stalagmieten worden gevormd door de neerslag van calciumcarbonaat uit water dat door de scheuren en spleten van grotten sijpelt. Terwijl het water uit het plafond van de grot druppelt, verliest het koolstofdioxide en wordt het opgeloste calciumcarbonaat afgezet, waardoor in de loop van de tijd de stalagmiet wordt opgebouwd.
Wanneer zoutzuur in contact komt met de stalagmiet, reageert het met het calciumcarbonaat en produceert het kooldioxidegas. De ontsnappende gasbellen veroorzaken het waargenomen bruisen.
 Wat is de kleur van het gas dat wordt gevormd door koper en salpeterzuur te combineren?
Wat is de kleur van het gas dat wordt gevormd door koper en salpeterzuur te combineren?  Hoe een biofysische simulatiemethode het ontdekken van medicijndoelen kan versnellen?
Hoe een biofysische simulatiemethode het ontdekken van medicijndoelen kan versnellen? Vind het aantal protonen, neutronen en elektronen in xenon?
Vind het aantal protonen, neutronen en elektronen in xenon?  Heeft chemie invloed op het leven, en zo ja, hoe?
Heeft chemie invloed op het leven, en zo ja, hoe?  Schimmelwegen op kaaskorst beïnvloeden voedselveiligheid, rijpheid
Schimmelwegen op kaaskorst beïnvloeden voedselveiligheid, rijpheid
 Arctische kustmachten steunen vreedzame dialoog over geschillen
Arctische kustmachten steunen vreedzame dialoog over geschillen Zou dit de laatste eeuw van de mensheid kunnen zijn?
Zou dit de laatste eeuw van de mensheid kunnen zijn?  Zet je schrap! Klimaatverandering om ernstige vliegtuigturbulentie te vergroten
Zet je schrap! Klimaatverandering om ernstige vliegtuigturbulentie te vergroten Verveeld door fysiotherapie? Focus in plaats daarvan op burgerwetenschap
Verveeld door fysiotherapie? Focus in plaats daarvan op burgerwetenschap  Oude wortelloze planten gekoppeld aan toename van de productie van modderrots
Oude wortelloze planten gekoppeld aan toename van de productie van modderrots
Hoofdlijnen
- Welke soorten organismen leefden voordat de mens op aarde verscheen?
- Kunnen meisjes beter lezen dan jongens? Als dat zo is, kunnen genderstereotypen hiervan de oorzaak zijn
- De primaire primaire productiviteit berekenen
- Zeer uiteenlopende skinks bieden inzicht in hoe evolutie werkt
- No-till management kan de uitstoot van lachgas verminderen, klimaatverandering bestrijden
- Burgerwetenschap kan de betrokkenheid en het begrip bij niet-gegradueerde biologielessen vergroten
- Hoge genetische diversiteit ontdekt bij Zuid-Afrikaanse luipaarden
- Giftige mannelijkheid:waarom mannelijke trechterwebspinnen zo gevaarlijk zijn
- Wat is de subeenheid van DNA genaamd?
- Polymeermembranen vergemakkelijken de uitwisseling van zuurstof in het lichaam

- Nieuwe lijm kan miljoenen medische procedures veiliger maken, minder invasief voor patiënten

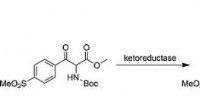
- Synthese van het veterinaire antibioticum florfenicol via een snelle chemo-enzymatische route
- Nieuw organisch plastic materiaal zorgt ervoor dat elektronica bij extreme temperaturen kan functioneren zonder in te boeten aan prestaties

- Schorpioenen maken een fluorescerende stof die hen kan helpen beschermen tegen parasieten

 De perfecte zeef op atomaire schaal
De perfecte zeef op atomaire schaal Wetenschappers ontdekken een proces dat het helderder maken van kwantumstippen in de weg staat
Wetenschappers ontdekken een proces dat het helderder maken van kwantumstippen in de weg staat Welk proces vindt niet plaats in dierlijke cellen?
Welk proces vindt niet plaats in dierlijke cellen?  Hoe zien fossiele brandstoffen eruit?
Hoe zien fossiele brandstoffen eruit?  Bemanning-7 astronauten verlaten het ISS na bijna 200 dagen in de ruimte
Bemanning-7 astronauten verlaten het ISS na bijna 200 dagen in de ruimte  Wat vloeistofdynamica kan verklaren over de verspreiding van COVID-19 - en hoe u uzelf kunt beschermen
Wat vloeistofdynamica kan verklaren over de verspreiding van COVID-19 - en hoe u uzelf kunt beschermen Video:Hoe kinine de Eerste Wereldoorlog veroorzaakte
Video:Hoe kinine de Eerste Wereldoorlog veroorzaakte Onderzoekers ontdekken zeer actieve organische fotokatalysator
Onderzoekers ontdekken zeer actieve organische fotokatalysator
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

