
Wetenschap
Waarom bevatten de afgassen bij verbranding CO2 en Nimethaan?
```
CH4 + 2O2 → CO2 + 2H2O
```
Bij deze reactie wordt het koolstofatoom in methaan geoxideerd om CO2 te vormen, terwijl de waterstofatomen worden geoxideerd om H2O te vormen. De reactie is zeer exotherm, wat betekent dat er een grote hoeveelheid warmte-energie vrijkomt. Daarom wordt methaan gebruikt als brandstof voor verwarming en koken.
De aanwezigheid van Ni in de afgassen zou ongebruikelijk zijn en zou erop kunnen wijzen dat er bij het verbrandingsproces een katalysator op nikkelbasis is gebruikt. Het is echter onwaarschijnlijk dat significante hoeveelheden Ni in de afgassen aanwezig zouden zijn. De aanwezigheid van methaan in de afgassen zou erop wijzen dat het verbrandingsproces onvolledig was en dat een deel van het methaan niet werd omgezet in CO2 en H2O. Dit kan te wijten zijn aan een gebrek aan zuurstof in het verbrandingsproces, maar ook aan het gebruik van brandstof van slechte kwaliteit.
 Wat is reactiever natrium of zwavel?
Wat is reactiever natrium of zwavel?  Nieuwe methode om adsorbentia te recyclen bij de behandeling van afvalwater
Nieuwe methode om adsorbentia te recyclen bij de behandeling van afvalwater  Hoe kunnen vormen en volume worden gebruikt om materialen te classificeren?
Hoe kunnen vormen en volume worden gebruikt om materialen te classificeren?  Nieuwe techniek om supersponzen te maken is een game changer
Nieuwe techniek om supersponzen te maken is een game changer Onderzoekers ontwikkelen op smartphone gebaseerde ovulatietest
Onderzoekers ontwikkelen op smartphone gebaseerde ovulatietest
 Zeespiracy:Hoe de visserij duurzamer te maken door bijvangst aan te pakken
Zeespiracy:Hoe de visserij duurzamer te maken door bijvangst aan te pakken  Onderzoekers geven geïntegreerde dataset vrij van hydrologische en thermische vervorming in de technische corridor van Qinghai-Tibet
Onderzoekers geven geïntegreerde dataset vrij van hydrologische en thermische vervorming in de technische corridor van Qinghai-Tibet Het belang van de Rode Zee in het oude Egypte
Het belang van de Rode Zee in het oude Egypte  Aanpassing van een Opossum
Aanpassing van een Opossum  In kaart brengen van micro naar macro:landschappen uit het verleden observeren via teledetectie
In kaart brengen van micro naar macro:landschappen uit het verleden observeren via teledetectie
Hoofdlijnen
- Earth Microbiome Project:het microbioom van... alles in kaart brengen
- Hoe u uw gazon het hele jaar door natuurvriendelijk kunt maken:tips van een ecoloog
- Wat gebeurt er als een kind wordt geboren met een extra chromosoom in het 23e paar?
- Wijzigingen in de Amerikaanse importregels voor honden:wat ze zijn en waarom belangrijk voor hondenmensen
- Wat betekenen de bloedgroepletters?
- Reacties van zaadeigenschappen op extreme droogte impliceren sterke relaties met droogtegevoeligheid
- Een ellebooggewricht bouwen Model
- Mobiele genetische elementen die de functie van nabijgelegen genen veranderen
- Wat zijn de drie stadia van cellulaire ademhaling in volgorde?
- Video:Welke van deze paddenstoelen zou je kunnen doden?

- Onderzoekers ontdekken dat sommige cidermakers onnodige suiker toevoegen

- Eerste 3D-geprinte proton-geleidende membraan effent de weg voor op maat gemaakte energieopslagapparaten

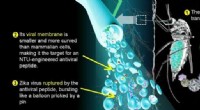
- Peptide maakt misbruik van achilleshiel van Zika-virus
- Kathodedefecten verbeteren de batterijprestaties

 Belle en het beest:waarom beide kunnen winnen bij social selling
Belle en het beest:waarom beide kunnen winnen bij social selling  Hoe automotoren werken
Hoe automotoren werken  Kan koper elektriciteit in vaste toestand geleiden?
Kan koper elektriciteit in vaste toestand geleiden?  Hoe bouw je een Egg Drop Container met rietjes
Hoe bouw je een Egg Drop Container met rietjes  Het Amerikaanse leger lanceerde een geheime anti-vax-campagne op de Filippijnen. Dit is de reden waarom een onderzoeker niet verrast is
Het Amerikaanse leger lanceerde een geheime anti-vax-campagne op de Filippijnen. Dit is de reden waarom een onderzoeker niet verrast is  Google waarschuwt u wanneer uw wachtwoorden te eenvoudig te raden zijn en te vaak worden gebruikt
Google waarschuwt u wanneer uw wachtwoorden te eenvoudig te raden zijn en te vaak worden gebruikt Dieren in het regenwoud die strijden om hetzelfde voedsel
Dieren in het regenwoud die strijden om hetzelfde voedsel Europese tornado's vormen een niet-erkende bedreiging, zeggen Britse meteorologen
Europese tornado's vormen een niet-erkende bedreiging, zeggen Britse meteorologen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

