
Wetenschap
Een monster van 10,0 ml waterig hcl heeft 26,13 ml 0,108 m naoh nodig om het eindpunt te bereiken. Wat is de molaire concentratie hcl?
De uitgebalanceerde chemische vergelijking voor de reactie tussen HCl en NaOH is:
$$HCl + NaOH \rechterpijl NaCl + H_2O$$
Uit de vergelijking kunnen we zien dat 1 mol HCl reageert met 1 mol NaOH. Daarom kan het aantal mol HCl in het monster van 10,0 ml als volgt worden berekend:
$$mol HCl =(26,13 ml)(0,108 M) =2,812 \maal 10^{-3} mol$$
De molaire concentratie HCl in het oorspronkelijke monster kan worden berekend door het aantal mol HCl te delen door het volume van het monster in liters:
$$molariteit van HCl =\frac{2,812 \times 10^{-3} mol}{10,0 \times 10^{-3} L} =0,2812 M$$
Daarom is de molaire concentratie HCl in het oorspronkelijke monster 0,2812 M.
 Wanneer methanol wordt verbrand en een fysieke of chemische verandering achterlaat?
Wanneer methanol wordt verbrand en een fysieke of chemische verandering achterlaat?  Webgebaseerd open-sourceprogramma bepaalt eiwitstructuren
Webgebaseerd open-sourceprogramma bepaalt eiwitstructuren Natuurkundigen decoderen de dynamische interactie tussen moleculaire machines in metaal-organische raamwerken
Natuurkundigen decoderen de dynamische interactie tussen moleculaire machines in metaal-organische raamwerken Hoe het Doppler-effect werkt
Hoe het Doppler-effect werkt  Wat is een formule voor Californië?
Wat is een formule voor Californië?
 Netwerkanalyse toepassen op natuurlijke historie:techniek gepopulariseerd via sociale media rangschikt impact van uitsterven
Netwerkanalyse toepassen op natuurlijke historie:techniek gepopulariseerd via sociale media rangschikt impact van uitsterven Met DISCO kunnen wetenschappers zeer reactief superoxide op koraalriffen meten
Met DISCO kunnen wetenschappers zeer reactief superoxide op koraalriffen meten Wordt de behendigheid van een dier beïnvloed door de stand van zijn ogen?
Wordt de behendigheid van een dier beïnvloed door de stand van zijn ogen?  Is Afrika de bakermat van de mensheid?
Is Afrika de bakermat van de mensheid?  Mijnbouwactiviteiten blijven zwarte families in Zuid-Afrika onteigenen
Mijnbouwactiviteiten blijven zwarte families in Zuid-Afrika onteigenen
Hoofdlijnen
- Wat gebeurt er als je hersenen niet kunnen bepalen welke kant op is?
- Hoe rifvissen de cyclus van de maan kunnen gebruiken om het geslacht van hun nakomelingen te manipuleren
- Wat is de functie van mannose?
- Studie biedt een model om te voorspellen hoe microbiomen op veranderingen kunnen reageren
- Commerciële voorouderstests kunnen onthullen hoeveel Neanderthaler-DNA u heeft
- Nieuwe gorilla in Audubon Zoo mag nog even binnen blijven
- Nieuw onderzoek dat kankerremmende eiwitten koppelt aan celantennes
- Zijn religies ontstaan uit ons verkeerde begrip van het menselijk bewustzijn?
- Cat Chromosome-informatie
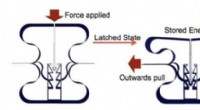
- Wetenschappers ontwerpen materiaal dat energie kan opslaan als een adelaarsgreep
- Techniekteam maakt monitoringtoolkit om de productie van biologische medicijnen te versnellen

- Interdisciplinaire samenwerking levert de moeilijkste, dunste coatings tot nu toe ontdekt

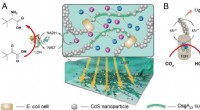
- Bacteriële biofilms vergemakkelijken biocompatibele bio-abiotische interfaces voor semi-kunstmatige fotosynthese
- Snelle detectie van toxische verbindingen
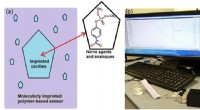
 Het onzichtbare zien - een nieuw gasbeeldvormingssysteem
Het onzichtbare zien - een nieuw gasbeeldvormingssysteem Broedkolonies van koningspinguïns zijn gestructureerd als vloeistoffen
Broedkolonies van koningspinguïns zijn gestructureerd als vloeistoffen Kristallen snel maken
Kristallen snel maken Vijvers kunnen meer koolstof opnemen dan bossen. Zo bestrijden ze de klimaatverandering in uw tuin
Vijvers kunnen meer koolstof opnemen dan bossen. Zo bestrijden ze de klimaatverandering in uw tuin  Asymmetrische structuur in het superzware zwarte gat in het centrum van de melkweg
Asymmetrische structuur in het superzware zwarte gat in het centrum van de melkweg Frances door orkaan getroffen St. Maarten op wacht voor gezondheidsbedreigingen
Frances door orkaan getroffen St. Maarten op wacht voor gezondheidsbedreigingen Waarom de zeeën sneller stijgen dan voorspeld
Waarom de zeeën sneller stijgen dan voorspeld  Een nieuwe draai aan de oorsprong van het leven?
Een nieuwe draai aan de oorsprong van het leven?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

