
Wetenschap
Wat is de sterkste koolstof-koolstof enkele binding, dubbele of drievoudige binding?
De sterkte van een koolstof-koolstofbinding wordt bepaald door de bindingsvolgorde, die verwijst naar het aantal elektronenparen dat tussen de atomen wordt gedeeld. Hoe hoger de obligatievolgorde, hoe sterker de binding.
Van de enkele, dubbele en drievoudige koolstof-koolstofbindingen is de drievoudige binding de sterkste. Dit komt omdat een drievoudige binding bestaat uit drie elektronenparen gedeeld door de koolstofatomen, terwijl een dubbele binding uit twee elektronenparen bestaat en een enkele binding uit slechts één elektronenpaar bestaat. Het grotere aantal elektronenparen in een drievoudige binding resulteert in een sterkere binding.
De bindingssterkten van enkele, dubbele en drievoudige koolstof-koolstofbindingen zijn respectievelijk ongeveer 348 kJ/mol, 611 kJ/mol en 839 kJ/mol.
 Onderzoekers observeren het oplossen van zout op atomair niveau
Onderzoekers observeren het oplossen van zout op atomair niveau  Welke wasmachineinstellingen kan ik gebruiken om mijn kleding langer mee te laten gaan?
Welke wasmachineinstellingen kan ik gebruiken om mijn kleding langer mee te laten gaan?  Hoe de dichtheid van benzine te meten
Hoe de dichtheid van benzine te meten  Op welke manier kan de reactiesnelheid tussen zwavelzuur en calciumcarbonaat worden gevolgd?
Op welke manier kan de reactiesnelheid tussen zwavelzuur en calciumcarbonaat worden gevolgd?  Zeewater thuis repliceren
Zeewater thuis repliceren
Hoofdlijnen
- Lichamelijke afbraak uitgelegd:hoe celdifferentiatiepatronen de somatische evolutie onderdrukken
- Onderzoekers stemmen af op eiwitparen:team kwantificeert hoe mutaties celsignalerende bacteriën beïnvloeden
- Het grootste onderzoek naar de groei van de dinosauruspopulatie ooit laat zien hoe Maiasaura leefde en stierf
- Nieuw onderzoeksmodel maakt duidelijk hoe organen met elkaar communiceren
- Kun jij een paar haren van een renpaard stelen en je eigen haren klonen?
- Wat zou er gebeuren als de cel geen DNA had?
- Wat zijn de sleutelwoorden voor oplossing in de wetenschap?
- Wat is een vetzuur? | Hoe dingen werken
- Onderzoek naar eiwitassemblage toont aan dat moleculaire worp van de dobbelstenen winnende combinaties oplevert
- De kans op succes in de synthetische chemie vergroten
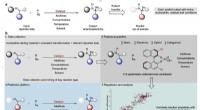
- Onderzoeksconsortium produceert 3D-kaart met hoge resolutie van GLP-1R
- Ingenieurs ontdekken nieuwe rol van water bij productie van hernieuwbare brandstoffen
- Feedback van duizenden ontwerpen kan eiwittechnologie transformeren
- Kwantumchemici toveren recept om goud te veranderen, zilver en koper in vaten van groene energie
 Waterafstotend materiaal werpt af als een slang bij beschadiging
Waterafstotend materiaal werpt af als een slang bij beschadiging Een kwantumgolf in twee kristallen
Een kwantumgolf in twee kristallen Waarom verliezen we Louisiana?
Waarom verliezen we Louisiana?  Astronauten arriveren voor NASA's eerste thuislancering in tien jaar
Astronauten arriveren voor NASA's eerste thuislancering in tien jaar Kleine deeltjes, grote bevindingen:het maximaliseren van de energiewinst van kleine nanodeeltjes
Kleine deeltjes, grote bevindingen:het maximaliseren van de energiewinst van kleine nanodeeltjes Hoe te controleren of een diode slecht is
Hoe te controleren of een diode slecht is  Grootste estuarium van het land met toenemend verzuringsrisico
Grootste estuarium van het land met toenemend verzuringsrisico Volgen sterrenstelsels de Darwinistische evolutie?
Volgen sterrenstelsels de Darwinistische evolutie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

