
Wetenschap
Wat gebeurt er als ijzersulfaat sterk wordt verwarmd?
2FeSO4 (s) → Fe2O3 (s) + SO2 (g) + SO3 (g)
Bij deze reactie valt ijzersulfaat uiteen in drie producten:ijzer(III)oxide (Fe2O3), zwaveldioxide (SO2) en zwaveltrioxide (SO3).
- IJzer(III)oxide (Fe2O3) :Dit is een roodbruine vaste stof die algemeen bekend staat als roest. Het is het hoofdbestanddeel van roest dat zich vormt op ijzeren voorwerpen wanneer ze worden blootgesteld aan zuurstof en water.
- Zwaveldioxide (SO2) :Dit is een giftig gas met een scherpe geur. Het komt in de atmosfeer terecht als gevolg van verschillende industriële processen, zoals de verbranding van fossiele brandstoffen. Zwaveldioxide kan bijdragen aan milieuproblemen zoals zure regen en aandoeningen van de luchtwegen.
- Zwaveltrioxide (SO3) :Dit is een zeer reactief gas dat met water kan reageren en zwavelzuur (H2SO4) vormt. Zwaveltrioxide wordt gebruikt bij de productie van verschillende industriële chemicaliën, zoals meststoffen, explosieven en kleurstoffen.
Het is belangrijk op te merken dat de thermische ontleding van ferrosulfaat een proces bij hoge temperaturen is en dat er aanzienlijke verwarming nodig is om op gang te komen. De specifieke temperatuur waarbij de ontleding plaatsvindt, kan variëren afhankelijk van de experimentele omstandigheden.
 Onderzoekers ontwerpen een nieuwe Cu-penetratie-elektrode met holle vezels voor efficiënte CO₂-elektroreductie
Onderzoekers ontwerpen een nieuwe Cu-penetratie-elektrode met holle vezels voor efficiënte CO₂-elektroreductie  Waarom mag een koortsthermometer niet in kokend water worden gesteriliseerd?
Waarom mag een koortsthermometer niet in kokend water worden gesteriliseerd?  Zelfherstellende katalysatoren maken het gemakkelijker om zonne-energie op te slaan met water
Zelfherstellende katalysatoren maken het gemakkelijker om zonne-energie op te slaan met water Chemici tonen aan dat het katalytische bereik van enzymen kan worden vergroot
Chemici tonen aan dat het katalytische bereik van enzymen kan worden vergroot Onderzoekers kapen zonneceltechnologie om een eenvoudige spuittest voor lood te ontwikkelen
Onderzoekers kapen zonneceltechnologie om een eenvoudige spuittest voor lood te ontwikkelen
Hoofdlijnen
- Voorbeelden van sensorische adaptatie
- Leef snel, sterf jong:signaaldetectietheorie bijwerken
- Wat eten we? Snel identificeren van onbeschreven soorten in een commercieel schimmelpakket
- Mariene microplastics:hoe de verspreiding van watermassa de transporttrajecten beïnvloedt
- Hoe verschillen schimmelsporen van bacteriële endosporen?
- Saoedi-Arabische rotskunst toont riemen op prehistorische honden
- Wat is de subeenheid van DNA genaamd?
- Hoe de kleine verandering van een eiwit tot grote problemen voor cellen leidt
- Onderzoekers identificeren combinatie van factoren voor biologische cacaoopbrengst
- Op polymeer gebaseerde coatings op metalen implantaten verbeteren de integratie van bot-implantaten
- Onderzoeksteams ontdekken buitengewone eigenschappen van strontiumniobaat

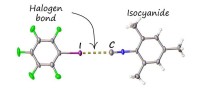
- Nieuwe niet-covalente binding blokkeert de afstotende geur van isocyaniden
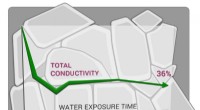
- Wetenschappers tonen aan dat een veelbelovende vaste elektrolyt hydrofoob is
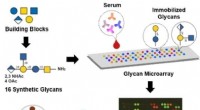
- Wetenschappers identificeren potentieel vaccindoelwit voor steeds meer bacteriestammen
 Zullen aardbevingen ooit voorspelbaar zijn?
Zullen aardbevingen ooit voorspelbaar zijn?  Lastig terrein:helpen om een veilige landing van de rover te verzekeren
Lastig terrein:helpen om een veilige landing van de rover te verzekeren Moet je bij warm weer lichtgekleurde kleding dragen om koel te blijven?
Moet je bij warm weer lichtgekleurde kleding dragen om koel te blijven?  Wat zijn vijf veel voorkomende stoffen die worden beschouwd als organische chemicaliën?
Wat zijn vijf veel voorkomende stoffen die worden beschouwd als organische chemicaliën?  Is jouw paard normaal? Nu is daar een app voor
Is jouw paard normaal? Nu is daar een app voor  Hoe lang duurt het voordat de hechtingen zijn opgelost?
Hoe lang duurt het voordat de hechtingen zijn opgelost?  Superzware binaire zwarte gatenjager:SKA pulsar timing array
Superzware binaire zwarte gatenjager:SKA pulsar timing array Wat gebeurt er tijdens de G1-fase?
Wat gebeurt er tijdens de G1-fase?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

