
Wetenschap
Waarom verandert warmte vloeibare H2O in gas?
Hier is een meer gedetailleerde uitleg van het proces:
1. Kinetische energie neemt toe :Wanneer warmte wordt toegevoegd aan vloeibaar water, krijgen de moleculen kinetische energie en bewegen ze sneller. Deze verhoogde kinetische energie zorgt ervoor dat de moleculen vaker en met grotere kracht met elkaar botsen.
2. Waterstofbruggen verbreken :De watermoleculen worden bij elkaar gehouden door waterstofbruggen, dit zijn intermoleculaire krachten die ontstaan tussen een waterstofatoom en een zeer elektronegatief atoom zoals zuurstof of stikstof. Naarmate de moleculen sneller bewegen en vaker met elkaar botsen, beginnen de waterstofbruggen daartussen te breken.
3. Ontsnap uit de vloeistof :Naarmate er steeds meer waterstofbruggen worden verbroken, kunnen de moleculen uit de vloeistof naar de gasfase ontsnappen. Dit proces wordt verdamping genoemd.
4. Koken :Het kookpunt van water is de temperatuur waarbij de dampspanning van de vloeistof gelijk is aan de druk rondom de vloeistof. Bij deze temperatuur hebben de watermoleculen voldoende energie om de atmosferische druk te overwinnen en in grote aantallen uit de vloeistof te ontsnappen. Er wordt gezegd dat het water kookt.
 Snelle tests voor vroege diagnose van hartaanvallen en identificatie van sepsis
Snelle tests voor vroege diagnose van hartaanvallen en identificatie van sepsis Waarom de commercialisering van koolstofafvang en -vastlegging heeft gefaald, hoe het kan werken
Waarom de commercialisering van koolstofafvang en -vastlegging heeft gefaald, hoe het kan werken  Nieuwe MD-simulatie werpt licht op het mysterie van de structuur van gehydrateerde elektronen
Nieuwe MD-simulatie werpt licht op het mysterie van de structuur van gehydrateerde elektronen Wat gebeurt er als een base wordt toegevoegd aan een bufferoplossing?
Wat gebeurt er als een base wordt toegevoegd aan een bufferoplossing?  Forensisch chemicus kan de leeftijd van bloedvlekken nu tot twee jaar voorspellen
Forensisch chemicus kan de leeftijd van bloedvlekken nu tot twee jaar voorspellen
 Hoe een slang te identificeren
Hoe een slang te identificeren  Terugtrekking Antarctische ijskap kan kettingreactie veroorzaken
Terugtrekking Antarctische ijskap kan kettingreactie veroorzaken 6 tools voor het voorspellen van sneeuwstormen om deze winter te gebruiken
6 tools voor het voorspellen van sneeuwstormen om deze winter te gebruiken Van chaos naar orde:hoe mieren het zoeken naar voedsel optimaliseren
Van chaos naar orde:hoe mieren het zoeken naar voedsel optimaliseren  Wetenschappers ontdekken dat modellen met grove resolutie toekomstige Mei-yu-regenval onderschatten
Wetenschappers ontdekken dat modellen met grove resolutie toekomstige Mei-yu-regenval onderschatten
Hoofdlijnen
- Nieuw onderzoek laat zien hoe complex bonobo-communicatie vergelijkbaar is met die van menselijke baby's
- Herbivoren helpen ecosystemen te beschermen tegen klimaatverandering
- Kan de behandeling van hondendementie aanwijzingen opleveren voor de ziekte van Alzheimer bij mensen?
- Nieuwe methode maakt het vinden van vleermuisverblijven gemakkelijker voor natuurbeschermers
- Ervaren dieren geluk?
- Helder en fotostabiel groen fluorescerend eiwit afgeleid van Japanse kwallen
- Starfish onthult evolutionaire geschiedenis van puberteitshormoon
- Opnieuw beoordelen wat we van peptiden kunnen verwachten bij de detectie van ziekten
- Wetenschappers ontdekken dat darmbacteriën in bijen antibioticaresistente genen naar elkaar verspreiden
- De spanning van een cel meten met een molecuul
- Lasers gebruiken om moleculaire mysteries in onze atmosfeer te visualiseren

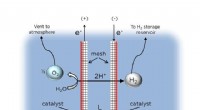
- Ingenieurs ontwikkelen drijvende boorinstallatie voor zonne-energie voor elektrolyse van zeewater
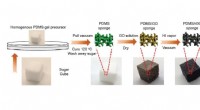
- Rekbare natrium-ion batterij-elektroden gemaakt van suikerklontjes
- Doorbraak in onderzoek naar schone diesel

 Het meten van de hoeveelheid pesticiden alleen bepaalt het risico niet
Het meten van de hoeveelheid pesticiden alleen bepaalt het risico niet Hoge druk is essentieel voor betere optische vezels
Hoge druk is essentieel voor betere optische vezels Tijdelijke gewasdiversiteit stabiliseert de landbouwproductie
Tijdelijke gewasdiversiteit stabiliseert de landbouwproductie Help een betere landkaart te maken met de NASA-app
Help een betere landkaart te maken met de NASA-app Kwetsbaarheid in software voor gepersonaliseerde geneeskunde ontdekt door Sandia-onderzoekers
Kwetsbaarheid in software voor gepersonaliseerde geneeskunde ontdekt door Sandia-onderzoekers De grootste maan van Saturnus kan de sleutel zijn tot schonere motoren
De grootste maan van Saturnus kan de sleutel zijn tot schonere motoren Wat zou er gebeuren als de aarde zou stoppen met draaien?
Wat zou er gebeuren als de aarde zou stoppen met draaien?  Wat zijn de planeten van het zonnestelsel in volgorde?
Wat zijn de planeten van het zonnestelsel in volgorde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

