
Wetenschap
Hoe röntgenstralen in de materie genetischtoxische elektronen met lage energie creëren
Samenvatting , hoewel een hoogenergetisch (≳34 eV) primair elektron gegenereerd door straling of door foto-emissie een grote kans heeft om DNA-basisbeschadigingsproducten zoals thymineglycol en zijn dimeer te vormen door directe Coulombische afstotende krachten wanneer het een snelle vertraging ondergaat [15–19] , het primaire elektron met lagere energie doet dit met veel verminderde efficiëntie via indirecte schade via de productie van hydroxylradicalen door excitatie van water en door een klein effect als gevolg van waterstofabstractie en door toevoeging aan thymidine. Aan de andere kant kunnen elektronen met lage energie (≤34 eV) gegenereerd via het subexcitatieproces inderdaad substantiële niveaus van strengbreuken (en gerelateerde laesies) veroorzaken, maar alleen die welke efficiënt resoneren met specifieke onbezette, zwak antibindende π* elektronische staten. Omdat laagenergetische elektronenvorming een aanzienlijk grotere dwarsdoorsnede heeft dan directe dubbelstrengsbreuken, kan laagenergetische elektronenbeschadiging bij omgevingsblootstelling en bij stralingstherapie-doses concurrerend worden met hoogenergetische, door elektronen gemedieerde dubbelstrengsbreuken.
 Energiebronnen verstopt terwijl de vulkaan van Hawaï lava in de buurt stuurt (update)
Energiebronnen verstopt terwijl de vulkaan van Hawaï lava in de buurt stuurt (update) Filipijnen heropenen beerput Boracay na opruiming
Filipijnen heropenen beerput Boracay na opruiming Wat is het effect van geografie op het klimaat?
Wat is het effect van geografie op het klimaat?  Mondiaal oppervlak van rivieren en beken is 45 procent groter dan eerder werd gedacht
Mondiaal oppervlak van rivieren en beken is 45 procent groter dan eerder werd gedacht Bosbranden die Brits-Columbia nog steeds teisteren, Canada
Bosbranden die Brits-Columbia nog steeds teisteren, Canada
Hoofdlijnen
- Hoe beïnvloeden wilde varkens oeversystemen?
- Je microben leven voort nadat je sterft – een microbioloog legt uit hoe je necrobioom het lichaam recycleert
- Welke invloed heeft CO2 op het openen van huidmondjes?
- Wanneer een levende plantencel water verliest door osmose, treedt er samentrekking van de inhoud op, weg van de muur. Hoe heet dit fenomeen?
- Mesozoïsche zoogdieren:wat weten we van China?
- Hoe het menselijk geheugen werkt
- Milieu op basis van evolutie indelen in twee categorieën?
- Lijst van aseksueel reproducerende organismen
- Welke enzymen verteren koolhydraten?
- De thermische geleidbaarheid van polymeren regelen met licht

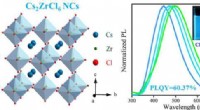
- Wetenschappers synthetiseren loodvrije op zirkonium gebaseerde vacature-geordende dubbele perovskiet nanokristallen
- Een groene benadering van het maken van ammoniak kan de wereld helpen voeden

- Van één uur tot één minuut:nieuwe analysetechniek vereenvoudigt het proces om bisfenol A-verontreinigingen te detecteren

- Wetenschappers ontwikkelen open-source software om de economie van biobrandstoffen te analyseren, bioproducten

 Hoe lang kan een dolfijn zijn adem inhouden?
Hoe lang kan een dolfijn zijn adem inhouden?  De effecten van niet recycleren
De effecten van niet recycleren Eerste metalen nanodeeltjes die bestand zijn tegen extreme hitte
Eerste metalen nanodeeltjes die bestand zijn tegen extreme hitte Vage orbitaal puin dat een gevaar vormt voor satellieten die niet nauw genoeg worden gevolgd, waarschuw astronomen
Vage orbitaal puin dat een gevaar vormt voor satellieten die niet nauw genoeg worden gevolgd, waarschuw astronomen Welke reactant geeft de laagste opbrengst bij een beperkte hoeveelheid product?
Welke reactant geeft de laagste opbrengst bij een beperkte hoeveelheid product?  Stoffige protoplanetaire schijven
Stoffige protoplanetaire schijven Welke soorten planten en dieren leven in de regio Moskou, Rusland?
Welke soorten planten en dieren leven in de regio Moskou, Rusland?  Mechanische ingenieurs ontwikkelen manieren om de productiviteit van windmolenparken te verbeteren
Mechanische ingenieurs ontwikkelen manieren om de productiviteit van windmolenparken te verbeteren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

