
Wetenschap
Verhelderend hoe stikstofase ammoniak maakt
Het stikstofase-enzymcomplex bestaat uit twee metallo-enzymen:het molybdeen-ijzer (MoFe) eiwit en het ijzer-zwavel (FeS) eiwit. Het MoFe-eiwit herbergt de actieve plaats waar N2-reductie plaatsvindt, terwijl het FeS-eiwit dient als elektronendonor en ATP-hydrolyserende eenheid.
Stikstofbinding:
1. Substraattoegang: De actieve plaats van stikstofase ligt diep begraven in het MoFe-eiwit, waardoor een beschermende omgeving ontstaat voor het delicate N2-reductieproces. Een reeks aminozuurresiduen en een molybdeencofactor (MoFe7S9C-homocitraat) vormen de "FeMo-cofactor", die dient als bindingsplaats voor N2.
2. Zwakke binding: Stikstof bindt zich reversibel aan de FeMo-cofactor via een "zijwaartse" interactie, waarbij de N-N drievoudige binding parallel loopt aan het FeMo-cluster. Deze zwakke binding zorgt voor de noodzakelijke mobiliteit en activering van N2.
Stikstofreductie:
1. ATP-hydrolyse: Het FeS-eiwit hydrolyseert ATP om energie te leveren voor het stikstofreductieproces. Deze hydrolyse genereert een hoogenergetisch elektron dat wordt overgebracht naar het MoFe-eiwit.
2. Elektronenoverdracht: Het hoogenergetische elektron reduceert een reeks ijzer-zwavelclusters binnen het MoFe-eiwit, waardoor het elektron uiteindelijk wordt afgeleverd aan de FeMo-cofactor.
3. Protonatie en reductieve splitsing: De gereduceerde FeMo-cofactor interageert met protonen (H+) uit de omgeving. Deze protonen nemen, samen met de elektronen, deel aan een reeks protonatie-reductiestappen die leiden tot de splitsing van de N-N drievoudige binding. Dit proces resulteert in de vorming van twee NH3-moleculen.
Het stikstofasemechanisme omvat meerdere cycli van ATP-hydrolyse, elektronenoverdracht en protonatie-reductiereacties. Elke cyclus brengt N2 dichter bij volledige reductie, wat uiteindelijk twee moleculen ammoniak oplevert. Het enzymcomplex ondergaat ook een reeks conformationele veranderingen tijdens de katalytische cyclus, die substraatbinding, elektronenoverdracht en productafgifte vergemakkelijken.
Ondanks de aanzienlijke vooruitgang die is geboekt bij het begrijpen van stikstofase, zijn er nog steeds aspecten van het mechanisme die nog volledig moeten worden opgehelderd. Verder onderzoek heeft tot doel een gedetailleerder verslag te geven van de ingewikkelde stappen die betrokken zijn bij stikstofreductie en de regulering van de stikstofase-activiteit, en draagt bij aan ons begrip van dit vitale biologische proces.
 Californië ziet af van milieuregels voor voorbereiding op brandseizoen
Californië ziet af van milieuregels voor voorbereiding op brandseizoen Top 10 inzichten in klimaatwetenschap in 2020 geselecteerd door 57 toonaangevende wereldwijde onderzoekers
Top 10 inzichten in klimaatwetenschap in 2020 geselecteerd door 57 toonaangevende wereldwijde onderzoekers VS zet zich schrap voor grote orkaan Florence
VS zet zich schrap voor grote orkaan Florence Onderzoekers onderzoeken hoe zoetwaterdiatomeeën in het licht blijven
Onderzoekers onderzoeken hoe zoetwaterdiatomeeën in het licht blijven  De verschillen tussen noordelijk en zuidelijk halfrond
De verschillen tussen noordelijk en zuidelijk halfrond
Hoofdlijnen
- Welke drie dingen helpen bloed door aderen te duwen?
- Het grootste onderzoek naar de groei van de dinosauruspopulatie ooit laat zien hoe Maiasaura leefde en stierf
- Lijst en beschrijf de vier hoofdklassen van moleculen
- Zeg vaarwel tegen knoflookadem met geurvrije zwarte knoflook
- Studie onthult het geheim van langlevende stamcellen
- Hoe elektroconvulsietherapie werkt
- Wetenschappers zouden supermodelbouwers moeten zijn
- Hoe de varkensgriep werkt
- rRNA: Wat is het?
- Nieuw inzicht in een kankerbeschermend eiwit kan leiden tot een nieuwe generatie kankerbehandelingen
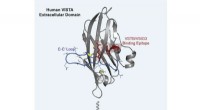
- Een gestroomlijnde benadering voor het bepalen van thermische eigenschappen van kristallijne vaste stoffen en legeringen

- Wetenschappers breken de structuur van tuberculose af
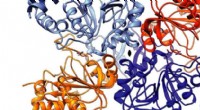
- Biomimetische chemie - DNA-nabootser is viraal enzym te slim af
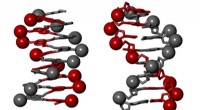
- Oppervlakte-oxygenaatsoorten verbeteren de door kobalt gekatalyseerde Fischer-Tropsch-synthese

 DNA vouwt zich in een slimme nanocapsule voor medicijnafgifte
DNA vouwt zich in een slimme nanocapsule voor medicijnafgifte Scholen gebruiken gezichtsherkenningstechnologie om de veiligheid te vergroten
Scholen gebruiken gezichtsherkenningstechnologie om de veiligheid te vergroten ESA-astronaut Alexander Gerst keert terug naar ISS voor Horizons-missie in 2018
ESA-astronaut Alexander Gerst keert terug naar ISS voor Horizons-missie in 2018 Op Kevlar gebaseerd kunstmatig kraakbeen bootst de magie van het echte werk na
Op Kevlar gebaseerd kunstmatig kraakbeen bootst de magie van het echte werk na Inleiding tot Febot
Inleiding tot Febot  NASA-wetenschappers maken zich op voor zonnestormen op Mars
NASA-wetenschappers maken zich op voor zonnestormen op Mars  Studie wijst op evolutie van peer review in academische publicaties, problemen en alternatieven
Studie wijst op evolutie van peer review in academische publicaties, problemen en alternatieven Hoe wetenschap, wiskunde en technologie zwemmers naar nieuwe hoogten kunnen stuwen
Hoe wetenschap, wiskunde en technologie zwemmers naar nieuwe hoogten kunnen stuwen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

