
Wetenschap
Chemici produceren een nieuw natuurenzym dat boor bevat
Boronzuur wordt al tientallen jaren in de organische chemie gebruikt, ook al is het in geen enkel organisme aanwezig. “Het geeft aanleiding tot andere chemische reacties dan we in de natuur aantreffen”, legt Gerard Roelfes, hoogleraar Biomoleculaire Chemie &Katalyse aan de Rijksuniversiteit Groningen uit.
Zijn groep creëerde een enzym met boorzuur als reactief centrum en gebruikte vervolgens gerichte evolutie om het selectiever te maken en zijn katalytische kracht te verbeteren. Bovendien zijn enzymatische reacties duurzamer dan klassieke chemische reacties, omdat ze plaatsvinden bij lage temperaturen en zonder giftige oplosmiddelen. Het onderzoek werd online gepubliceerd in het tijdschrift Nature op 8 mei.
De toepassing van boor in de organische chemie dateert al zo'n zeventig jaar en werd in 1979 bekroond met de Nobelprijs voor de Scheikunde. De laatste jaren is de belangstelling voor boor als katalysator gegroeid, maar het gebruik ervan in de chemische industrie is vooralsnog beperkt.
Roelfes legt uit:‘Tot nu toe is boorkatalyse te langzaam en niet erg geschikt voor enantioselectieve reacties. Dit soort reacties worden gebruikt om chirale moleculen te creëren, die in twee versies kunnen bestaan die spiegelbeelden van elkaar zijn, zoals een linker en een rechterhand.
"Bij veel medicijnen kunnen beide handen een verschillend effect hebben. Het is daarom belangrijk om selectief de juiste hand te produceren, vooral voor de farmaceutische industrie."
Uitgebreide genetische code
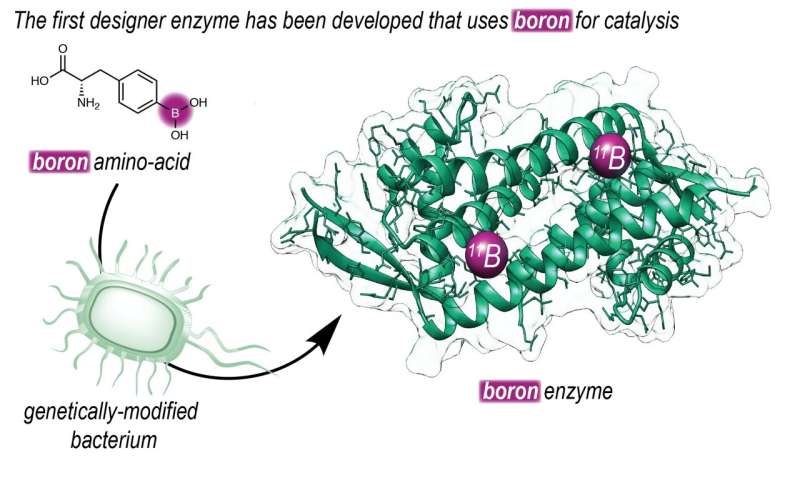
“Om dit mogelijk te maken, wilden we boor in een enzym introduceren. Onze groep heeft een lange geschiedenis in het ontwerpen van enzymen die in de natuur niet voorkomen”, zegt Roelfes. De Roelfes-groep gebruikte een uitgebreide genetische code om een niet-natuurlijk aminozuur dat een reactieve boorzuurgroep bevat, in een enzym te introduceren. “Met deze techniek kunnen we op DNA-niveau bepalen waar we het aminozuur in een eiwit plaatsen.”
Toen ze eenmaal een enzym hadden gemaakt met boorzuur in het reactieve centrum, konden ze gerichte evolutie gebruiken om de efficiëntie ervan te vergroten, wat resulteerde in een snellere katalyse. Roelfes voegt hieraan toe:‘Bovendien konden we door het boorzuur in de chirale context van een enzym te plaatsen een zeer enantioselectieve katalyse bereiken. De beschreven reactie is een proof-of-principle en toont de weg naar het benutten van de katalytische kracht van boor in enzymen."
Biokatalyse
Het gebruik van enzymen om organische verbindingen te maken is belangrijk voor de farmaceutische industrie. "In hun streven naar groenere en duurzamere manieren om medicijnen te produceren, kijken ze naar biokatalyse om conventionele chemische reacties te vervangen", zegt Roelfes.
Aan de Rijksuniversiteit Groningen wordt hier hard aan gewerkt. Roelfes concludeert:"We hebben een aantal onderzoeksgroepen aan de Faculteit Science and Engineering die zich bezighouden met dit soort werk, waarbij ze verschillende benaderingen gebruiken om biokatalytische oplossingen voor de chemische industrie te creëren."
In deze context zullen Roelfes en zijn team doorgaan met het ontwikkelen van hun boorzuurenzymen en andere, van dit soort nieuw-voor-de-natuur-enzymen.