
Wetenschap
Theoretisch perspectief op C-H/O-H activering door Cu-O in biologische en synthetische systemen
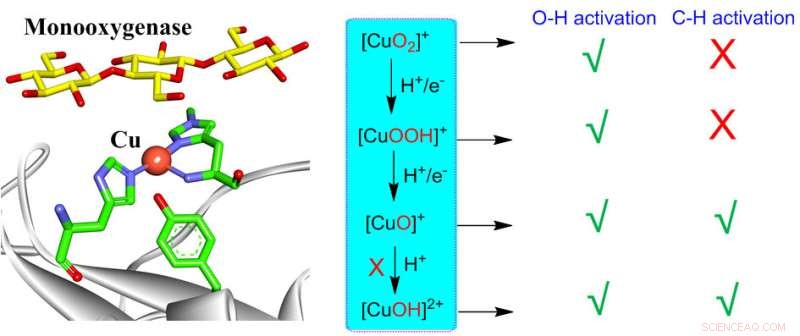
Dizuurstofactivering door mononucleair koper in biologische en synthetische systemen kan verschillende koper-zuurstoftussenproducten genereren, waaronder [CuO2 ] + , [CuOOH] + , [CuO] + , [CuOH] 2+ . Al deze soorten kunnen OH-activering uitvoeren, terwijl alleen [CuO] + en [CuOH] 2+ zijn reactief voor C-H-activering. Echter, de vorming van [CuOH] 2+ is zeer ongunstig in monooxygenases, waardoor [CuO] + als het enige actieve tussenproduct dat verantwoordelijk is voor CH-activering in mono-oxygenasen. Deze inzichten kunnen consistent inzicht verschaffen in de reactiviteiten van verschillende koper-zuurstof-actieve soorten in biologische en synthetische systemen. Krediet:Chinese Journal of Catalysis
Dizuurstofactiveringen vormen een van de kernproblemen bij koperafhankelijke metallo-enzymen. Op O2 activering zijn koperafhankelijke metallo-enzymen, waaronder deeltjesvormige methaanmono-oxygenasen (pMMO's), lytische polysacharide-mono-oxygenasen (LPMO's) en binucleaire koperenzymen PHM en DBM, in staat om uitdagende C-H/O-H-bindingsactiveringen uit te voeren.
Ondertussen zijn koper-zuurstofkern-bevattende complexen gesynthetiseerd om de actieve soorten metallo-enzymen na te bootsen. Dizuurstofactivering door mononucleaire koper actieve site kan koper-zuurstof tussenproducten genereren, waaronder Cu(II)-superoxo, Cu(II)-hydroperoxo, Cu(II)-oxyl evenals de Cu(III)-hydroxide soorten.
Intrigerend genoeg zijn al deze soorten ingeroepen als de potentiële actieve tussenproducten voor C-H/O-H-activeringen in biologische of synthetische systemen. Vanwege het slechte begrip van de reactiviteiten van het koper-zuurstofcomplex, is de aard van actieve soorten in zowel biologische als synthetische systemen zeer controversieel.
Onlangs heeft een onderzoeksteam onder leiding van Prof. Binju Wang van de Universiteit van Xiamen, China, de reactiviteiten van verschillende mononucleaire koper-zuurstofsoorten in zowel biologische als synthetische systemen beoordeeld. Het onderzoek toont aan:
- (a) de MN15-functionaliteit is zeer nauwkeurig voor mononucleaire koper-zuurstofcomplexen, waarin de experimentele kinetiek van verschillende C-H/O-H-activeringen goed kan worden gereproduceerd met MN15.
- (b) Cu(II)-superoxo vertoont de consistente reactiviteiten in zowel biologische als synthetische systemen:het is zeer reactief voor activeringen van O-H-bindingen, maar vertoont lage reactiviteiten voor activeringen van C-H-bindingen. Cu(II)-superoxo zou dus niet de actieve soort kunnen zijn voor C-H-activeringen in zowel biologische als synthetische systemen.
- (c) Cu(II)-hydroperoxo is inert voor activeringen van C-H-bindingen, maar zijn radicale karakter op de proximale O stelt het in staat om HAA uit te voeren van matige O-H-bindingen of te koppelen met een ander Cu(I) om de dinucleaire kopersoort te vormen . Cu(II)-hydroperoxo vertegenwoordigt dus een belangrijk tussenproduct langs de O2 activeringsroutes in plaats van een oxidatiemiddel voor CH-activering in zowel biologische als synthetische systemen.
- (d) Cu(II)-oxyl is zeer reactief voor activeringen van C-H-bindingen en zou dus verantwoordelijk kunnen zijn voor C-H-activering in mononucleaire kopermonoxygenasen.
- (e) Hoewel de hoge reactiviteit van koper(III)-hydroxide ten aanzien van activeringen van C-H-bindingen goed is vastgesteld, is de vorming van dergelijke soorten in monoxygenasen thermodynamisch zeer ongunstig.
Deze inzichten zullen naar verwachting een consistent begrip opleveren van de reactiviteiten van verschillende koper-zuurstof-actieve soorten in zowel biologische als synthetische systemen.
De recensie is gepubliceerd in het Chinese Journal of Catalysis . + Verder verkennen
Wetenschappers onthullen mechanisme van dizuurstofactivering
 Eigenschappen van Heat Absorption van Salt
Eigenschappen van Heat Absorption van Salt Norovirusstructuren kunnen helpen bij het ontwikkelen van behandelingen voor voedselvergiftiging
Norovirusstructuren kunnen helpen bij het ontwikkelen van behandelingen voor voedselvergiftiging Nieuw materiaal kan de productie van plastic energiezuiniger maken
Nieuw materiaal kan de productie van plastic energiezuiniger maken Onderzoekers ontwikkelen duurzaam katalyseproces
Onderzoekers ontwikkelen duurzaam katalyseproces Wetenschappers onthullen stapsgewijze hydratatiemotieven van zwaveldioxide
Wetenschappers onthullen stapsgewijze hydratatiemotieven van zwaveldioxide
 We moeten de transities voor duurzaamheid en klimaatverandering versnellen, deskundigen zeggen
We moeten de transities voor duurzaamheid en klimaatverandering versnellen, deskundigen zeggen In de Rode Zee, koraalriffen kunnen de hitte van klimaatverandering aan
In de Rode Zee, koraalriffen kunnen de hitte van klimaatverandering aan Veel laaggelegen atoleilanden zouden tegen het midden van de 21e eeuw onbewoonbaar kunnen zijn
Veel laaggelegen atoleilanden zouden tegen het midden van de 21e eeuw onbewoonbaar kunnen zijn Hoe stroomt energie door een voedselketen?
Hoe stroomt energie door een voedselketen?  De diepe oceaan warmt langzaam op, maar er zijn dramatische veranderingen op komst
De diepe oceaan warmt langzaam op, maar er zijn dramatische veranderingen op komst
Hoofdlijnen
- Wat zijn de rollen van chlorofyl A & B?
- Veranderen met de leeftijd:naarmate vleermuizen ouder worden, verschillen hun immuuncellen
- Celstructuren en hun drie belangrijkste functies
- Natuurlijke selectie: definitie, Darwins-theorie, voorbeelden en feiten
- Een fosfolipideroute van planten naar parasieten
- Zilte zwembadbacteriën kunnen opruimen en opstarten
- Wat is een regeling in de microbiologie?
- Onderzoekers beschrijven een belangrijk onderdeel in het energievoorzieningsmechanisme van het lichaam
- Hoe cellen onafhankelijk worden en functies reguleren
- Het onthullen van de nanostructuur van hout zou kunnen helpen de hoogtelimieten voor houten wolkenkrabbers te verhogen

- Een zeer gevoelige nieuwe bloedtest kan zeldzame kankereiwitten detecteren
- Runderembryo regenereert placenta-vormende cellen volledig

- Onderzoekers bedenken proces om duurzaam rubber te maken, kunststoffen

- Radicale stappen naar schone inkapseling
 Levenscyclus van een duizendpoot
Levenscyclus van een duizendpoot  Hoe de RPM op stappenmotoren te bepalen
Hoe de RPM op stappenmotoren te bepalen Typen elektrisch lassen
Typen elektrisch lassen Oude site op de Westelijke Jordaanoever trekt christenen, en controverse
Oude site op de Westelijke Jordaanoever trekt christenen, en controverse Operaties met robotgereedschap brengen tanken in de ruimte dichter bij de realiteit
Operaties met robotgereedschap brengen tanken in de ruimte dichter bij de realiteit Zeespiegelstijging gekoppeld aan hogere grondwaterstanden langs de kust van Californië
Zeespiegelstijging gekoppeld aan hogere grondwaterstanden langs de kust van Californië Hoe werken luchtkerntransformatoren?
Hoe werken luchtkerntransformatoren?  Hoe het netwerk van mannen en vrouwen hun arbeidsmarktprestaties beïnvloedt
Hoe het netwerk van mannen en vrouwen hun arbeidsmarktprestaties beïnvloedt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

