
Wetenschap
Microfluïdisch apparaat simuleert kankerbehandeling net zo effectief als proefdieren
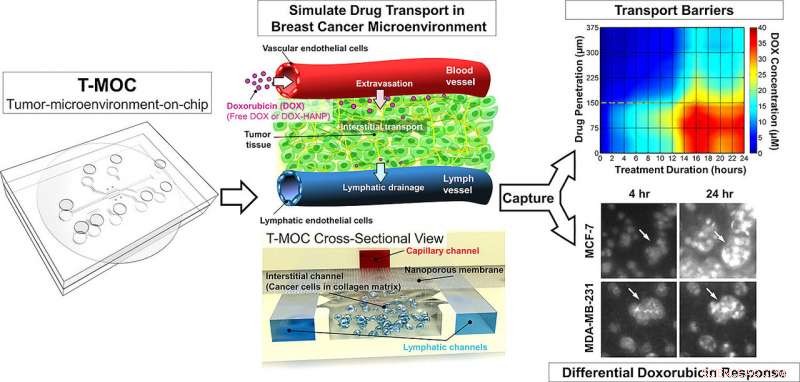
Deze afbeelding toont de werking van een nieuwe technologie die is ontwikkeld aan de Purdue University en die tumoren simuleert. Credit:Purdue University-foto / Altug Ozcelikkale
Het is aangetoond dat een nieuwe technologie die tumoren simuleert even goed presteert als proefdieren bij het testen van chemotherapiemedicijnen, wat een potentieel hulpmiddel is voor het screenen van geneesmiddelen voordat een patiënt wordt behandeld.
Een langetermijndoel is om biopsie van kankercellen van patiënten op te nemen en de effectiviteit van verschillende medicijnen op de van de patiënt afgeleide cellen te testen, zei Bumsoo Han, een Purdue University hoogleraar mechanische en biomedische technologie.
"Er zijn veel verschillende soorten chemotherapiemedicijnen, zodat clinici mogelijk kunnen bepalen welke waarschijnlijk effectiever zijn dan andere, " zei hij. "Succesvolle medicijnafgifte en het overwinnen van medicijnresistentie zijn de primaire klinische uitdagingen voor het beheer en de behandeling van kanker. Om dit probleem aan te pakken, we hebben de tumor-micro-omgeving-on-chip (T-MOC) ontwikkeld."
Het apparaat is ongeveer 4,5 centimeter in het vierkant en bevat "microfluïdische" kanalen waar kankercellen worden gekweekt in een driedimensionale "extracellulaire matrix, " een steigerachtig materiaal gevonden tussen cellen in levend weefsel. De experimenten bevatten ook "interstitiële vloeistof, " die in tumoren wordt gevonden en waarvan wordt gedacht dat het een barrière vormt voor de toediening van medicijnen.
Een dergelijk instrument zou kunnen worden gebruikt voor "precisiegeneeskunde, " waarbij medicamenteuze behandeling is afgestemd op individuele patiënten en bepaalde soorten kanker. Geneesmiddelresistentie en verschillende subtypes van tumoren vormen cruciale knelpunten voor effectieve chemotherapie. Kankercellen produceren multiresistente eiwitten die de geneesmiddelen tegen kanker uit de cellen pompen, hen te helpen de chemotherapiebehandeling te overleven.
Het onderzoek heeft tot doel een screeningplatform voor geneesmiddelen te ontwikkelen om deze mechanismen van meervoudige resistentie tegen geneesmiddelen na te bootsen. en om de bevindingen te valideren tegen de huidige gouden standaard, onderzoek met kleine dieren, zei Han.
Nieuwe onderzoeksresultaten werden gedetailleerd in een paper dat in november in de Tijdschrift voor gecontroleerde afgifte . De hoofdauteur van het artikel is Purdue, postdoctoraal onderzoeksmedewerker Altug Ozcelikkale.
De onderzoekers gebruikten het gebruikelijke chemotherapie-medicijn doxorubicine en testten ook het verschil tussen doxorubicine in conventionele vorm versus een formulering voor medicijnafgifte door nanodeeltjes.
Het papier is co-auteur van onderzoekers verbonden aan Purdue's School of Mechanical Engineering, Afdeling Vergelijkende Pathobiologie, Centrum voor Kankeronderzoek, Weldon School of Biomedical Engineering en Birck Nanotechnology Center; Afdeling Farmacologie en Toxicologie van de Indiana University; en het Biomedical Research Institute van het Korea Institute of Science and Technology. Een lijst van co-auteurs is opgenomen in het abstract.
De onderzoekers toonden eerder aan dat het T-MOC-apparaat verschillende soorten kankercellen kon onderscheiden. In de nieuwe bevindingen het team toonde aan dat de T-MOC net zo goed presteerde als onderzoeksmuizen bij het testen van de effectiviteit van geneesmiddelen tegen kanker op twee soorten borstkankercellen, genaamd MCF-7 en MDA-MB-231. Bovendien, het moleculaire mechanisme van doxorubicineresistentie was consistent met dat van muizen, zei Han.
De bevindingen toonden ook aan dat de T-MOC in staat is om "plasmaklaring, " een lichaamsreactie waarbij geneesmiddelen tegen kanker worden gefilterd door de lever en de nieren, waardoor slechts een kleine hoeveelheid de tumor kan bereiken.
Beide cellijnen gekweekt op de T-MOC vertoonden een verhoogde resistentie tegen de geneesmiddelen in vergelijking met cellen gekweekt op een standaard platte petrischaalcultuur, het matchen van de resultaten met muizen en het suggereren van een meer levensecht resultaat.
"Dit bevestigt het voorspellende vermogen van T-MOC voor in vivo medicijnrespons, "Zei Han. "Deze aanvankelijke karakterisering van T-MOC wijst op zijn transformatieve potentieel voor het testen van drugeffectiviteit."
Toekomstig werk zal het onderzoek naar verschillende soorten kanker uitbreiden, waaronder pancreas- en prostaatkanker.
 Chemicaliën kunnen hun identiteit veranderen, dankzij de vloeistoffen waar ze zich bevinden
Chemicaliën kunnen hun identiteit veranderen, dankzij de vloeistoffen waar ze zich bevinden Wat is een calorimeter en wat zijn de beperkingen?
Wat is een calorimeter en wat zijn de beperkingen?  Minimalisering van blootstelling aan schadelijke vlamvertragende chemicaliën in afvalschuim en kunststoffen
Minimalisering van blootstelling aan schadelijke vlamvertragende chemicaliën in afvalschuim en kunststoffen Een stap in de richting van metaal-organische raamwerksynthese
Een stap in de richting van metaal-organische raamwerksynthese Chemici bepalen hoe bijproducten bij de synthese van perovskieten kunnen worden vermeden
Chemici bepalen hoe bijproducten bij de synthese van perovskieten kunnen worden vermeden
Hoofdlijnen
- Wat zijn de zes soorten bindweefsel in de biologie?
Bindweefsel is een van de vier belangrijkste weefseltypen bij zoogdieren, de andere zijn zenuwweefsel, spierweefsel en epitheel of oppervlakteweefsel. Epitheliaal weefsel ligt op bindweefsel terwi
- De voor- en nadelen van mutatie
- Twee eiwitten behouden de pluripotentie van embryonale stamcellen op verschillende manieren
- Antibioticaresistentie:slapende bacteriën die medicamenteuze behandeling kunnen overleven geïdentificeerd
- Wanneer is lachen een medisch symptoom?
- Wat zijn organellen in een prokaryotische cel?
- Wildlife betaalt de prijs van illegale begrazing in Kenia
- Twee neuropeptiden in zebravissen geven aanwijzingen voor de complexe neurale mechanismen die ten grondslag liggen aan slaap
- Onderzoekers vinden dat er minstens 14, 003 plantensoorten in het Amazonebekken
- Forensische onderzoekers vinden een nauwkeurigere manier om de leeftijd van overledenen te schatten

- Nieuwe ontdekking kan nauwkeurige voorspelling van kankerverspreiding mogelijk maken voordat kanker zich ontwikkelt
- Enzym uit zilte diep herrezen in het lab

- Bouwstenen van DNA en RNA hadden samen kunnen verschijnen voordat het leven op aarde begon
- Onderzoekers maken theoretische voorspelling van 2-D halfgeleider tindioxide
 Dieren & hun aanpassingen in het naaldbos
Dieren & hun aanpassingen in het naaldbos  Koraalrifoases bieden een sprankje hoop
Koraalrifoases bieden een sprankje hoop Team verbetert detectie op afstand van gevaarlijke radioactieve stoffen
Team verbetert detectie op afstand van gevaarlijke radioactieve stoffen Kan een stad ooit echt CO2-neutraal zijn?
Kan een stad ooit echt CO2-neutraal zijn? Receptortyrosinekinasen regelen mechanosensoren
Receptortyrosinekinasen regelen mechanosensoren Krachtig grafeen hybride materiaal voor zeer efficiënte supercondensatoren
Krachtig grafeen hybride materiaal voor zeer efficiënte supercondensatoren Hoe beïnvloedt klimaatverandering bergachtige stroomgebieden die water leveren?
Hoe beïnvloedt klimaatverandering bergachtige stroomgebieden die water leveren? Hoe radialen om te zetten in graden
Hoe radialen om te zetten in graden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Swedish | German | Dutch | Danish | Norway | Portuguese |

-
Wetenschap © https://nl.scienceaq.com

