
Wetenschap
Oncogenen:hoe gemuteerde genen de celdeling van kanker stimuleren
Oncogenen zijn gemuteerde versies van normale genen die overmatige celdeling bevorderen. Terwijl gezonde cellen een strak gereguleerde cyclus doorlopen, kunnen oncogenen deze waarborgen terzijde schuiven, wat leidt tot ongecontroleerde groei en tumorvorming.
Proto-Oncogenen en normale celregulatie
Proto-oncogenen zijn de normale, functionele genen die de groei aansturen wanneer een cel zich moet delen, bijvoorbeeld tijdens weefselherstel of embryonale ontwikkeling. Tumor-suppressorgenen werken als remmen en voorkomen deling wanneer deze niet gerechtvaardigd is. Het evenwicht tussen deze twee krachten houdt de celproliferatie onder controle.
Wanneer een proto-oncogen wordt gemuteerd – door een enkele baseverandering, amplificatie of chromosomale herschikking – kan het een oncogen worden. Het veranderde gen blijft óf constitutief actief, óf geeft de cel het signaal agressiever te delen, zelfs als er geen externe signalen zijn.
Normale celcyclus en controlepunten
Bij gezonde cellen omvat de celcyclus mitose gevolgd door interfase, waarin de cel zich voorbereidt op de volgende deling of de rustige GO-fase ingaat. Gedurende de interfase beoordelen drie kritische controlepunten de DNA-integriteit, de voedingsstatus en de mitotische spoelvorming.
Elke afwijking die bij deze controlepunten wordt gedetecteerd, stopt doorgaans de cyclus. DNA-schade activeert reparatiemechanismen; als de schade onherstelbaar is, ondergaat de cel apoptose om de verspreiding van fouten te voorkomen.
Oncogenen verstoren de celcycluscontrole
Oncogenen interfereren met controlepuntsignalering. Een gemuteerd proto-oncogen kan waarschuwingen voor DNA-schade negeren en reparatie en apoptose omzeilen. Als gevolg hiervan blijven cellen met defect DNA zich delen, waardoor een verzameling afwijkende nakomelingen ontstaat die extra mutaties kunnen accumuleren.
Impact op DNA-integriteit en celdood
Tijdens de G2/M-transitie verifieert de cel dat de DNA-replicatie volledig en nauwkeurig is. Oncogene signalering kan de arrestatie opheffen die normaal gesproken zou optreden als replicatiefouten of -breuken worden gedetecteerd, waardoor progressie naar mitose met aangetast genetisch materiaal mogelijk wordt.
Op dezelfde manier kunnen oncogenen apoptose remmen. Door pro-apoptotische routes te onderdrukken, maken deze genen het overleven van beschadigde cellen mogelijk, waardoor de expansie van een kwaadaardige kloon wordt bevorderd.
Van ongecontroleerde deling tot tumorvorming
Initiële klonale expansie levert een gelokaliseerde massa abnormale cellen op:een vroege tumor. Deze tumor heeft geen speciale bloedtoevoer en is niet in staat tot uitzaaiing totdat aanvullende factoren ingrijpen.
Het verlies van tumorsuppressorgenen en de activering van oncogenen stimuleren samen angiogenese, de vorming van nieuwe bloedvaten die de groeiende massa voeden. Verbeterde vascularisatie zorgt ervoor dat de tumor groter wordt en uiteindelijk omliggende weefsels infiltreert.
Metastase en door oncogenen aangedreven migratie
Bepaalde oncogenen, zoals die in de RAS-route, reguleren ook de cytoskeletdynamiek en celadhesie. Deze veranderingen zorgen ervoor dat tumorcellen zich kunnen losmaken, de bloedbaan kunnen binnendringen en verre organen kunnen koloniseren – een kenmerk van uitgezaaide kanker.
Belangrijke Oncogen-voorbeelden
- TRK (tropomyosinereceptorkinase) – Mutaties of fusies activeren signalen die de proliferatie en beweeglijkheid in neurale weefsels bevorderen.
- RAS – Constitutieve activering stimuleert groei-, differentiatie- en overlevingssignalen, die vaak voorkomen bij pancreas-, colorectale en longkanker.
- ERK (extracellulair signaalgereguleerd kinase) – Hyperactieve ERK-signalering verbetert de DNA-replicatie en ondersteunt oncogene RAS-routes.
- MYC – Overexpressie versterkt de transcriptie van genen die de celgroei, het metabolisme en de ribosoombiogenese reguleren, wat bijdraagt aan de tumorigenese bij veel soorten kanker.
Progressie naar kwaadaardige kanker
De convergentie van oncogene activering, verlies van tumorsuppressoren en het ontwijken van apoptose leidt tot een zichzelf in stand houdende, invasieve tumor. Naarmate de kwaadaardige kloon zich uitbreidt, vestigt deze zijn eigen vasculaire netwerk en krijgt hij het vermogen om te metastaseren, wat resulteert in een wijdverspreide ziekte.
Incidentie van kanker bij de mens en moderne therapieën
Veelvoorkomende vormen van kanker – long-, borst-, colorectale en prostaatkanker – worden vaak veroorzaakt door specifieke oncogene veranderingen. Gerichte therapieën die mutante eiwitten remmen, gecombineerd met traditionele chemotherapie en radiotherapie, hebben de overlevingskansen verbeterd en de toxiciteit verminderd.
Gepersonaliseerde geneeskunde, geleid door genomische profilering van individuele tumoren, stelt artsen in staat medicijnen te selecteren die de oncogene factoren die aanwezig zijn in de kanker van elke patiënt direct tegengaan, waardoor de werkzaamheid wordt vergroot en bijkomende schade wordt geminimaliseerd.
Lopend onderzoek naar remmers van immuuncontrolepunten, genbewerking en nieuwe remmers van kleine moleculen belooft verdere doorbraken in het terugdringen van door oncogenen veroorzaakte maligniteiten.
Ondanks de toenemende prevalentie van kanker hebben de vooruitgang op het gebied van vroege detectie, gerichte behandeling en preventieve strategieën de sterftecijfers wereldwijd gestaag verlaagd.
 Welke soorten transport verplaatst moleculen langs een concentratiegradiënt?
Welke soorten transport verplaatst moleculen langs een concentratiegradiënt?  Wat is de bindingshoek van het CS2 -molecuul?
Wat is de bindingshoek van het CS2 -molecuul?  Een organel die vrije radicalen ontgift, staat bekend als?
Een organel die vrije radicalen ontgift, staat bekend als?  Ontworpen moleculen verwijderen selectief ongewenste ionen uit complexe oplossingen voor energieproductie
Ontworpen moleculen verwijderen selectief ongewenste ionen uit complexe oplossingen voor energieproductie Hoe wordt de hoeveelheid oplosbaarheidszout opgeloste oplosbaarheid?
Hoe wordt de hoeveelheid oplosbaarheidszout opgeloste oplosbaarheid?
 Nieuw onderzoek kan helpen onze kwetsbare zeeën te beschermen
Nieuw onderzoek kan helpen onze kwetsbare zeeën te beschermen Hoe overleven reuzenpanda's?
Hoe overleven reuzenpanda's?  Gebaseerd op het concept van de ecologische voetafdruk, welke van de volgende landen heeft het grootste landoppervlak per persoon dat nodig is om hun levensstijl te ondersteunen?
Gebaseerd op het concept van de ecologische voetafdruk, welke van de volgende landen heeft het grootste landoppervlak per persoon dat nodig is om hun levensstijl te ondersteunen?  Palmolie niet de enige oorzaak van bosverlies in Indonesië
Palmolie niet de enige oorzaak van bosverlies in Indonesië Wetenschapsleiders roepen op tot empirisch onderbouwd beleid
Wetenschapsleiders roepen op tot empirisch onderbouwd beleid
Hoofdlijnen
- 3 Basiscomponenten van een nucleotide?
- Welk celproces gebruiken organismen wanneer ze seksueel reproduceren?
- Plantverdediging volgens het iron-maiden-principe
- Hoe biologische capsules reageren onder stress
- Wat is een product van de Calvin -cyclus?
- Nieuwe aquacultuurtechnologie kan de wereldwijde voedselcrisis helpen verlichten met verrijkt zeewier
- Welke rol speelde Xray -foto van DNA in de ontdekkingsstructuur?
- Wat doet een endoplasmatisch reticulum in de dierencel?
- Gefaciliteerde diffusie over een biologisch membraan vereist wat?
- Een nieuwe manier om feromonen te produceren als gewasbeschermingsmiddel
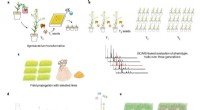
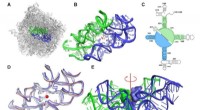
- De oorsprong van het leven in een RNA-pocket
- Zijn linkshandigen beter in sport?

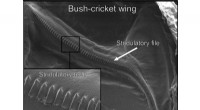
- Vleugelstructuur van vitaal belang bij het produceren van een reeks tonen bij paringsoproepen van bush-cricket
- Vijf invasieve soorten die de biodiversiteit van Californië bedreigen

 Laagfrequente ruis elimineren met een chirale metabeam
Laagfrequente ruis elimineren met een chirale metabeam Hoe heet een paar overeenkomstige chromosomen?
Hoe heet een paar overeenkomstige chromosomen?  Wat is een synoniem voor het woord?
Wat is een synoniem voor het woord?  Koelsnelheid berekenen
Koelsnelheid berekenen  Feiten over de chromosfeer van de zon
Feiten over de chromosfeer van de zon  Wat is de sterkste aardbeving in Alaska in de maand maart?
Wat is de sterkste aardbeving in Alaska in de maand maart?  Maakt Hubble Space Telescope foto's van kwik?
Maakt Hubble Space Telescope foto's van kwik?  Welk gas verwijderen dieren uit de lucht?
Welk gas verwijderen dieren uit de lucht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

