
Wetenschap
Wat zijn alle factoren die de enzymactiviteit beïnvloeden, behalve voor temperatuur en pH?
1. Substraatconcentratie:
* Lage substraatconcentratie: Bij lage substraatconcentraties neemt de enzymactiviteit evenredig toe met de substraatconcentratie. Meer substraat betekent meer enzym-substraatcomplexen vormen, wat leidt tot een hogere reactiesnelheid.
* Hoge substraatconcentratie: Bij zeer hoge substraatconcentraties wordt het enzym verzadigd. Alle actieve locaties zijn bezet en de reactiesnelheidsplateaus, die zijn maximale snelheid (VMAX) bereiken.
2. Enzymconcentratie:
* Verhoogde enzymconcentratie: Meer enzymmoleculen betekenen meer actieve locaties die beschikbaar zijn, wat leidt tot een snellere reactiesnelheid.
* Verminderde enzymconcentratie: Minder enzymmoleculen resulteren in een langzamere reactiesnelheid.
3. Remmers:
* Competitieve remmers: Binden aan de actieve plaats van het enzym, concurrerend met het substraat. Ze vertragen de reactiesnelheid, maar kunnen worden overwonnen door de substraatconcentratie te verhogen.
* Niet-competitieve remmers: Bind aan een plaats op het enzym anders dan de actieve plaats, verandert de vorm van het enzym en vermindert de activiteit. Ze kunnen niet worden overwonnen door de substraatconcentratie te verhogen.
* niet -concurrerende remmers: Binden aan het enzym-substraatcomplex, waardoor de vorming van het product wordt voorkomen.
4. Activatoren:
* Cofactors: Anorganische ionen (zoals magnesium, zink) die nodig zijn voor enzymactiviteit.
* Co -enzymen: Organische moleculen (zoals NAD+, FAD) die enzymen helpen bij katalyse.
5. Productconcentratie:
* Productremming: Sommige enzymen worden geremd door het product van de reactie. Dit kan fungeren als een feedbackmechanisme om enzymactiviteit te reguleren.
6. Allosterische regelgeving:
* Allosterische enzymen: Heb een allosterische plaats waar andere moleculen dan het substraat kunnen binden. Deze binding kan de activiteit van het enzym van het enzym activeren of remmen, wat de conformatie en functie ervan beïnvloedt.
7. Modificatie:
* fosforylering: Het toevoegen van een fosfaatgroep kan een enzym activeren of deactiveren.
* Glycosylatie: Het toevoegen van een suikergroep kan de stabiliteit en activiteit van enzym beïnvloeden.
8. Eiwitstructuur:
* denaturatie: Veranderingen in eiwitstructuur (bijvoorbeeld vanwege warmte, extreme pH of chemicaliën) kunnen de actieve plaats verstoren en het enzym inactief maken.
* Conformationele veranderingen: Zelfs subtiele veranderingen in enzymconformatie kunnen de katalytische efficiëntie beïnvloeden.
Onthoud: Hoewel temperatuur en pH cruciaal zijn voor enzymactiviteit, is het essentieel om te erkennen dat deze andere factoren ook belangrijke rollen spelen. Het gecombineerde effect van al deze factoren bepaalt de totale snelheid van een enzymatische reactie.
 Nieuwe strategie om de verspreiding van zuurplaatsen in zeolieten te beheersen
Nieuwe strategie om de verspreiding van zuurplaatsen in zeolieten te beheersen Lithiumionen stromen door vast materiaal
Lithiumionen stromen door vast materiaal Maken of breken:nieuwe omkeerbare techniek produceert acylfluoride met behulp van zeldzaam metaal
Maken of breken:nieuwe omkeerbare techniek produceert acylfluoride met behulp van zeldzaam metaal Onderzoekers bedenken goedkopere, snellere manier om continu amines te produceren
Onderzoekers bedenken goedkopere, snellere manier om continu amines te produceren Hoe ethyleengas te maken
Hoe ethyleengas te maken
Hoofdlijnen
- Wat maakt DNA uniek?
- Wat is DNA -splitsing?
- Wat is de betekenis van bio-intensief?
- Wat is een neerslag in de wetenschap?
- Wordt een drievoudige RNA -nucleotiden bekend als codon?
- Wat is de uitgedrukte wanneer geen van beide kopie van een allel volledig maskeert, anders dan in plaats daarvan allelen worden gezien?
- Studie:Hoe een unieke familie bacteriën zich verbergt voor het immuunsysteem
- Werken interferonen tegen alle pathogenen?
- Het type celverbinding dat de inhoud voorkomt maag of urineblaas om in omliggende weefsels te lekken?
- Onderzoekers meten de bereidheid van kleinschalige vissers om vaartuigvolgsystemen te gebruiken

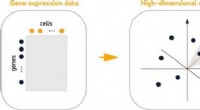
- Hoe markergenen in celclusters te vinden
- Waarom maakt het hebben van te veel opties het moeilijker om te kiezen?

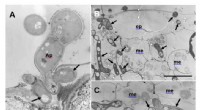
- Afwijkende hyfen veroorzaakt door immuunreacties van de gastheer op plantpathogene schimmel
- Hoe orang-oetanmoeders communiceren met hun kroost

 Afrika doelwit van door Rusland geleide desinformatiecampagne:Facebook
Afrika doelwit van door Rusland geleide desinformatiecampagne:Facebook Welke soorten dingen vervuilen water?
Welke soorten dingen vervuilen water?  Hoefijzerkrabben bedreigd door biomedische bloedvergieten
Hoefijzerkrabben bedreigd door biomedische bloedvergieten  Nanokristallen uit gerecycled houtafval maken koolstofvezelcomposieten sterker
Nanokristallen uit gerecycled houtafval maken koolstofvezelcomposieten sterker Groene waterstof klinkt als een overwinning voor ontwikkelingslanden. Maar kosten en transport zijn problemen
Groene waterstof klinkt als een overwinning voor ontwikkelingslanden. Maar kosten en transport zijn problemen Welk van de volgende kan niet worden geclassificeerd als een stikstof van de stikstof van de stofluchtvaarttafel?
Welk van de volgende kan niet worden geclassificeerd als een stikstof van de stikstof van de stofluchtvaarttafel?  Een kwantumsprong voor ultranauwkeurige metingen en informatiecodering?
Een kwantumsprong voor ultranauwkeurige metingen en informatiecodering?  Onderzoekers werken aan een beter begrip van hydrodynamische instabiliteiten in NIF, astrofysica
Onderzoekers werken aan een beter begrip van hydrodynamische instabiliteiten in NIF, astrofysica
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

