
Wetenschap
Gouden nanodeeltje gebruikt om virus te vervangen in nieuwe CRISPR-aanpak
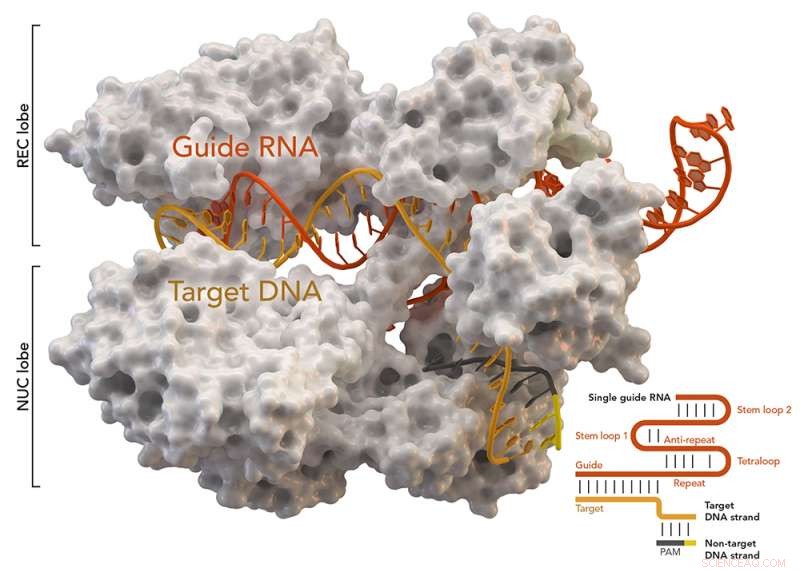
CRISPR-geassocieerd eiwit Cas9 (wit) van Staphylococcus aureus op basis van Protein Database ID 5AXW. Krediet:Thomas Splettstoesser (Wikipedia, CC BY-SA 4.0)
(Phys.org) - Een team van onderzoekers van de Universiteit van Californië en de Universiteit van Tokio heeft een manier gevonden om de CRISPR-genbewerkingstechniek te gebruiken die niet afhankelijk is van een virus voor levering. In hun artikel gepubliceerd in het tijdschrift Natuur Biomedische Technologie , de groep beschrijft de nieuwe techniek, hoe goed het werkt en verbeteringen die moeten worden aangebracht om het een levensvatbaar hulpmiddel voor het bewerken van genen te maken.
CRISPR-Cas9 is de laatste tijd veel in het nieuws, omdat het onderzoekers in staat stelt genen direct te bewerken – door ongewenste delen uit te schakelen of helemaal te vervangen. Maar ondanks vele succesverhalen, de techniek lijdt nog steeds aan een groot gebrek dat verhindert dat het als een echt medisch hulpmiddel wordt gebruikt - het maakt soms fouten. Die fouten kunnen kleine of grote problemen veroorzaken voor een host, afhankelijk van wat er mis gaat. Voorafgaand onderzoek heeft gesuggereerd dat de meeste fouten te wijten zijn aan leveringsproblemen, wat betekent dat een vervanging voor het virusgedeelte van de techniek nodig is. In deze nieuwe poging de onderzoekers melden dat ze net zo'n vervanging hebben ontdekt, en het werkte zo goed dat het een genmutatie in een Duchenne spierdystrofie muismodel kon repareren. Het team heeft de nieuwe techniek CRISPR-Gold genoemd, omdat een gouden nanodeeltje werd gebruikt om de genbewerkingsmoleculen af te leveren in plaats van een virus.
Het nieuwe pakket is gemaakt door een stukje DNA te modificeren om ervoor te zorgen dat het aan een gouden nanodeeltje blijft kleven en vervolgens een Cas9-eiwit en ook een RNA-gids. Het pakket werd vervolgens gecoat met een polymeer dat diende als een insluitingshuls - een die ook endocytose (een vorm van celtransport) veroorzaakte en de moleculen hielp ontsnappen uit endosomen eenmaal in de doelcellen. De moleculen gingen toen aan het werk - de Cas9 sneed de doel-DNA-streng door, het gids-RNA liet zien wat er moest gebeuren en er werd een DNA-streng geplaatst waar een mutatie had bestaan. Het resultaat was een gen dat vrij is van een mutatie die de spierdystrofie van Duchenne veroorzaakt.
Er is nog een groot probleem te overwinnen met de techniek, het werkt echter alleen in gelokaliseerde toepassingen. Ideaal, een massa pakjes zou in de bloedbaan worden geïnjecteerd, waardoor alle celtypen kunnen worden gerepareerd, zoals spieren die zijn aangetast door een gemuteerd gen.
© 2017 Fys.org
 Maïs met een laag gras:de beste combinatie vinden voor maïs op biobrandstof, bodembescherming
Maïs met een laag gras:de beste combinatie vinden voor maïs op biobrandstof, bodembescherming Papier weggooien zodat het kan worden gerecycled
Papier weggooien zodat het kan worden gerecycled  Wormen, watervlooien en bacteriën kunnen schoon water naar afgelegen gebieden brengen
Wormen, watervlooien en bacteriën kunnen schoon water naar afgelegen gebieden brengen Is ondergronds vervoer slechter voor je gezondheid?
Is ondergronds vervoer slechter voor je gezondheid? Rapport over seismische contextmetingen voor geïnduceerde seismiciteit
Rapport over seismische contextmetingen voor geïnduceerde seismiciteit
Hoofdlijnen
- Vissen reageren op aanvallen van roofdieren door de groeisnelheid te verdubbelen
- 10 fascinerende feiten over de nieuwe levensboom-evolutiekaart
- Uitvindingen in 1947
- Hoe hoge bomen suikers verplaatsen
- Ecologische onderzoeksmethoden: observeren, experimenteren en modelleren
- Kan een hersenscan je vertellen of je een crimineel gaat worden?
- Wat doet de temporale kwab?
- Hoe Dopamine sommige voedingsmiddelen verslavend maakt
- Crowdsourced spel is bedoeld om oplossingen te vinden voor aflatoxine
- De afnemende populaties van koninginnenschelpen zijn gefragmenteerd en dat verandert het natuurbeschermingsspel

- Wat zit er in je tarwe? Wetenschappers voegen het genoom van de meest voorkomende broodtarwe samen

- Wanneer vissen:Timing is belangrijk voor vissen die migreren om zich voort te planten

- Met extra suiker, bladeren worden ook dik

- Als uw nieuwjaarsresolutie is om fit te worden, uw hond kan uw perfecte trainingspartner zijn

 Uitstromend gas in ultralichte sterrenstelsels
Uitstromend gas in ultralichte sterrenstelsels Informele straffen in verband met de voorwaardelijke vrijlating vergroten de kans op gevangenisstraffen
Informele straffen in verband met de voorwaardelijke vrijlating vergroten de kans op gevangenisstraffen Nieuwe radiotelescoop in Brookhaven ziet de ruimte in een ander licht
Nieuwe radiotelescoop in Brookhaven ziet de ruimte in een ander licht Met hoofdletsel montage, zullen steden hun voeten neerleggen bij elektrische scooters?
Met hoofdletsel montage, zullen steden hun voeten neerleggen bij elektrische scooters? Een chemische aanwijzing voor hoe het leven op aarde begon
Een chemische aanwijzing voor hoe het leven op aarde begon Dit bazige bureau bepaalt wanneer je opstaat en gaat zitten
Dit bazige bureau bepaalt wanneer je opstaat en gaat zitten  Hoe werkt een Demagnetizer?
Hoe werkt een Demagnetizer?  Een nieuwe benadering voor het ontwerpen en implementeren van een hybride systeemtaal
Een nieuwe benadering voor het ontwerpen en implementeren van een hybride systeemtaal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Portuguese | Swedish | German | Dutch | Danish | Norway | Spanish |

-
Wetenschap © https://nl.scienceaq.com

