Wetenschap
Een nieuwe strategie voor de elektrochemische reductie van nitraat tot ammoniak
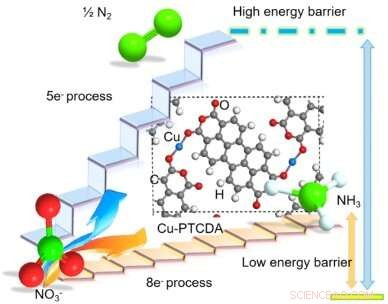
Voorgestelde structuur van Cu-opgenomen PTCDA en schematisch diagram dat het voordeel illustreert van het selectief reduceren van NO3− tot NH3 via directe 8-elektronenoverdracht. Rood, wit, grijs, briljant-blauw, en groene bollen vertegenwoordigen de O, H, C, Cu, en N-atomen, respectievelijk. Krediet:Chen et al.
Ammoniak (NH 3 ) is een kleurloze, gasvormige en in water oplosbare verbinding die in verschillende sectoren wordt gebruikt, inclusief landbouw, de energiesector, en een verscheidenheid aan industrieën. Voor meer dan een eeuw, de belangrijkste manier om grote hoeveelheden ammoniak te produceren was via het Haber-Bosch-proces, waarbij hoge druk wordt gebruikt om een chemische reactie te produceren die de directe synthese van ammoniak uit waterstof en stikstof mogelijk maakt.
Terwijl het Haber-Bosch-proces de massaproductie van ammoniak mogelijk maakt, het is bekend dat het schadelijk is voor zowel mens als milieu, omdat het het verbruik van fossiele brandstoffen met zich meebrengt en dus het broeikaseffect verergert. Door deze ongewenste effecten onderzoekers hebben gezocht naar alternatieve methoden voor het produceren van ammoniak via N 2 H 2 O chemische reacties onder omgevingsomstandigheden, waarvan sommige gebruik maken van hernieuwbare energiebronnen.
Sommige van deze nieuwe technieken voor de productie van ammoniak zijn effectief en relatief goedkoop gebleken. Niettemin, ze lieten onderzoekers doorgaans slechts beperkte hoeveelheden ammoniak produceren en vertoonden een slechte selectiviteit, vanwege de inerte N≡N-binding en de ultralage oplosbaarheid van N 2 in water.
Onderzoekers van de South China University of Technology en Argonne National Laboratory hebben onlangs een nieuwe elektrochemische strategie bedacht om ammoniak te produceren door nitraat te verminderen. hun methode, geïntroduceerd in een paper gepubliceerd in Natuur Energie , is gebaseerd op het gebruik van een kopermoleculaire vaste katalysator.
"NH . verkrijgen 3 rechtstreeks van niet−N 2 bronnen wordt beschouwd als een revolutionaire strategie om de problemen aan te pakken die verband houden met eerdere ammoniakproductieprocessen, "Haihui Wang, een van de onderzoekers die het onderzoek heeft uitgevoerd, vertelde Phys.org. "In de zoektocht naar andere stikstofhoudende alternatieven dan N 2 NH . synthetiseren 3 , het nitraatanion (NO 3 - ) valt op door het feit dat de lagere dissociatie-energie van N=O binding (204 kJ mol -1 ) vergeleken met N-N drievoudige binding (941 kJ mol -1 ), en de verrijking van NO 3 - in waterbronnen veroorzaakte milieuvervuiling en bedreigt de menselijke gezondheid."
Selectief omzetten van NO 3 - naar NH 3 onder omgevingsomstandigheden en in een H 2 O-gebaseerd systeem zou een groener alternatief kunnen zijn voor de massaproductie van NH 3 . Deze alternatieve conversie zou de milieuproblemen verlichten die gepaard gaan met de huidige methoden om op grote schaal ammoniak te produceren, terwijl ook het energieverbruik wordt verminderd.
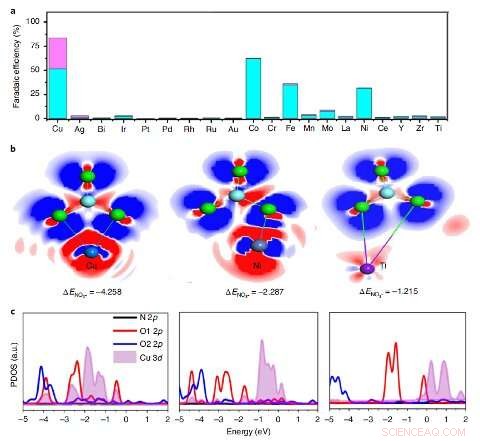
Screening van het element met de hoogste activiteit. een, De Faraday-efficiëntie van NH3 (blauw) en NO2− (mauve) van verschillende elementen opgenomen in PTCDA onder een potentiaal van −0,4 V versus RHE. B, De EDD van NO3– op 1Cu–PTCDA(¬103) (links), 1Ni-PTCDA(¬103) (midden) en 1Ti-PTCDA(¬103) (rechts). Blauw, donkerblauw, paars, hemelsblauwe en groene bollen vertegenwoordigen de Cu, nee, Ti, N- en O-atomen, respectievelijk. De blauwe elektronische wolk geeft de accumulatie van lading aan en de rode elektronische wolk geeft de uitputting van de lading aan. C, De geprojecteerde toestandsdichtheid (PDOS) van *NO3 op 1Cu–PTCDA (¬103) (links), 1Ni-PTCDA(¬103) (midden) en 1Ti-PTCDA(¬103) (rechts). Krediet:Chen et al.
"NEEN converteren" 3 - in NH 3 verre van een gemakkelijke taak, omdat het een overdrachtsreactie van acht elektronen vereist, evenals een iets lagere reactiepotentiaal (d.w.z. 1,20 V versus de omkeerbare waterstofelektrode of RHE) dan die van de vijf-elektronenomzetting van NO 3 - naar N 2 (1,25 V versus RHE), " legde Wang uit. "Verschillende elektrokatalytische systemen met verschillende heterogene katalysatoren (zoals Cu, ag, au, enzovoort) in het verleden zijn voorgesteld, maar de meeste van hen hebben de neiging om N . te produceren 2 via vijf-elektronenreductie van NO 3 - in plaats van de gewenste acht-elektronenreductie."
Het praktische potentieel van het omzetten van NO 3 - naar NH 3 lager is dan wat bekend staat als de waterstofevolutiereactie (HER) potentiaal, wat leidt tot het genereren van H 2 . Dit kan de algehele efficiëntie van de productie van NH . verminderen 3 .
In hun studie hebben Wang en zijn collega's waren in staat om de directe acht-elektronenreductie van NO . te bereiken 3 - naar NH 3, gekatalyseerd door Cu-opgenomen kristallijn 3, 4, 9, 10-peryleentetracarbonzuurdianhydride (PTCDA) met een laag-energetische barrière. De katalysator die ze gebruikten vertoonde een hoge opbrengst en uitstekende selectiviteit, effectief HER onderdrukken.
"We hebben katalysatoren gescreend met de bereiding van een reeks metalen opgenomen in PTCDA, zoals Cu, ag, au, Ru, Rh, Ir, pd, punt, Bi, Ti, kr, mn, Fe, Co, nee, ja, Zr, ma, La en Ce, Wang legde uit. "We ontdekten dat de hoge prestaties van onze katalysator kunnen worden toegeschreven aan de unieke elektronenconfiguratie van Cu 3 NS orbitaal met verhoogde overlap met nitraat O 2 P orbitalen om ladingsoverdracht te verbeteren, evenals de structuur van PTCDA, wat helpt om de overdracht van protonen en elektronen naar de actieve Cu-centra te reguleren en vervolgens HER te remmen en H-N-binding te bevorderen."
De elektrochemische methode die door Wang en zijn collega's is geïntroduceerd, zou de uitdagingen kunnen aanpakken die momenteel worden geassocieerd met massale NH 3 productie. Bij de eerste testen deze methode behaalde Faraday-efficiënties tussen 60% en 86% en NH 3 productiesnelheden tussen ongeveer 400 en 900 g h –1 cm –2 bij toegepaste potentialen van −0,4 tot −0,6 V versus RHE.
De resultaten zijn aanzienlijk beter dan die bereikt met andere methoden voor de elektrochemische reductie van N 2 naar NH 3 . Bijvoorbeeld, door lithium gemedieerde methoden, die het meest bekend zijn voor het bereiken van relatief hoge opbrengstpercentages bij de elektroreductie van N 2 -naar-NH 3 , bereikte een productiesnelheid van minder dan 36 μg h -1 cm.
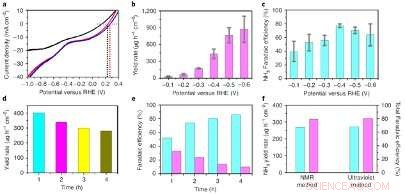
Elektrokatalytische prestaties van O-Cu-PTCDA. een, Lineaire sweep-voltammetriecurves van O-Cu-PTCDA getest in 0,1 M PBS (zwart), 0,1 M PBS met NO2− (rood) en 0,1 M PBS met NO3− (blauw). B, NH3-opbrengstsnelheid bij verschillende potentialen op het tweede uur. C, NH3 Faraday-efficiëntie bij verschillende potentialen op het tweede uur. NS, NH3-opbrengst op verschillende tijdstippen bij −0,4 V versus RHE tot 4 uur. e, NH3 (blauw) en NO2− (paars) Faraday-efficiëntie op verschillende tijdstippen bij −0,4 V versus RHE tot 4 uur. F, De totale NH3-opbrengst (blauw) en de totale Faraday-efficiëntie (mauve) gedetecteerd door 1H NMR-spectroscopie en een indofenolblauw-methode na het experiment van 4 uur. Krediet:Chen et al.
The recent study by Wang and his colleagues also opens up new possibilities for the recycling of nitrogen (NO 3 - ) in wastewater. Voor meerdere jaren, NEE 3 - was considered to be a toxic water contaminant and was usually transferred into gaseous nitrogen and returned to the air. Recent studies, echter, suggest that the high amount of nitrogen in wastewater could in fact be recycled for fertilization.
"The total nitrogen discharged into the water per year is 14.5 ± 3.1 million tons in China, which is about 50% of the annual consumption of synthetic nitrogen (300.5 million tons in 2016), " Wang said. "In 2016, the United States planted 94 million acres of corn, using about 8.9 billion kilograms of nitrogen annually, which accounts for 40% of the annual nitrogen use in the United States. Echter, it is worth noting that 2.4 billion kilograms of nitrogen is available in wastewater each year. The statistics prove that nitrogen in wastewaters could be a valuable resource."
In addition to allowing the large-scale production of ammonia in ways that are more environmentally friendly, the recent work by Wang and his colleagues could pave the way toward the development of wastewater management systems with nitrogen conversion capabilities. These systems would enable the recycling of large quantities of nitrogen, ultimately optimizing the use of global resources and protecting the environment.
While the results are promising, the researchers still need to overcome two technical challenges before their method can be applied in real-world settings. These challenges will be the main focus of their next set of studies.
"Aan de ene kant, our future studies will be aimed at enhancing the catalyst's structure to further improve its long-term stability, " Wang said. "In this work, the NH 3 yield rate decreased from 337.8 μg h -1 cm -2 to 140.3 μg h -1 cm -2 after 15 hours, after which it was substantially stable and maintained an NH 3 yield rate of 130.8 μg h -1 cm -2 after 40 hours. Anderzijds, we will work on the large-scale application of NH 3 electrosynthesis, developing an electric-driving flow device for the direct and continuous mass production of high-purity liquid ammonia or ammonium salt. We plan to devise a simple method for the direct purification and collection of the products, which removes the need for additional purification, transportation and other procedures."
© 2020 Wetenschap X Netwerk
 Team ontdekt dat polymorfe selectie tijdens kristalgroei thermodynamisch kan worden aangestuurd
Team ontdekt dat polymorfe selectie tijdens kristalgroei thermodynamisch kan worden aangestuurd Onderzoekers reproduceren Great Wave-schilderij op microschaal met inktloze technologie
Onderzoekers reproduceren Great Wave-schilderij op microschaal met inktloze technologie Wetenschappers analyseren de chemische bindingen die eiwitten vormen
Wetenschappers analyseren de chemische bindingen die eiwitten vormen Nieuw protocol voor organische synthese met organoboorverbindingen en zichtbaar licht
Nieuw protocol voor organische synthese met organoboorverbindingen en zichtbaar licht Hoe Thermokoppelgevoeligheid te berekenen
Hoe Thermokoppelgevoeligheid te berekenen
 Puntpatronen helpen aardverschuivingen te voorspellen
Puntpatronen helpen aardverschuivingen te voorspellen NASA kijkt naar regenval in tropische cycloon Yvette
NASA kijkt naar regenval in tropische cycloon Yvette NASA vangt orkaan Dora op maximale sterkte, voordat de verzwakking begon
NASA vangt orkaan Dora op maximale sterkte, voordat de verzwakking begon De overstromingen in Queensland zijn zo groot dat je ze alleen vanuit de ruimte kunt volgen
De overstromingen in Queensland zijn zo groot dat je ze alleen vanuit de ruimte kunt volgen Risicovolle strategie voor de planeet kunstmatig koelen, nieuw onderzoek toont aan
Risicovolle strategie voor de planeet kunstmatig koelen, nieuw onderzoek toont aan
Hoofdlijnen
- Campylobacter gebruikt andere organismen als Trojaans paard om nieuwe gastheren te infecteren
- Hoe toont hemoglobine de vier niveaus van eiwitstructuur?
- Genexpressie in Prokaryotes
- Een DNA-model maken met behulp van pijpreinigers
- Hoe maak je een 3D-model van de dikke darm
- S-fase: wat gebeurt er tijdens deze subfase van de celcyclus?
- Moet je intelligent zijn om slecht te zijn?
- Wetenschap zet nog een stap in het wissen van pijnlijke herinneringen
- Hoe pest werkt
 Fiscale prikkels kunnen de CO2-uitstoot in ontwikkelingslanden helpen verminderen
Fiscale prikkels kunnen de CO2-uitstoot in ontwikkelingslanden helpen verminderen Nieuwe soorten oviraptorosauriër ontdekt in Mongolië
Nieuwe soorten oviraptorosauriër ontdekt in Mongolië Oorzaak van E. coli strandsluitingen? Meeuwen
Oorzaak van E. coli strandsluitingen? Meeuwen Hoe veilig te blijven tijdens een bliksemstorm
Hoe veilig te blijven tijdens een bliksemstorm  Vox Media en eigenaar van New York magazine gaan fuseren
Vox Media en eigenaar van New York magazine gaan fuseren De landschapsmarkt heeft een categorie voor elk activiteitenniveau
De landschapsmarkt heeft een categorie voor elk activiteitenniveau Waarom beïnvloedt suiker het vriespunt van water?
Waarom beïnvloedt suiker het vriespunt van water?  Samsung onthult AI-aangedreven digitale avatar
Samsung onthult AI-aangedreven digitale avatar
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | German | Dutch | Danish | Norway | Swedish |

-
Wetenschap © https://nl.scienceaq.com