
Wetenschap
Hoe voorkomt elektrostatische krachten de nanodeeltjes om te aggregeren?
1. Oppervlaktelading: Nanodeeltjes bezitten meestal een oppervlaktelading. Deze lading kan voortkomen uit verschillende factoren:
* ionisatie: Oppervlakteatomen kunnen ioniseren, waardoor een netto positieve of negatieve lading ontstaat.
* adsorptie: Ionen van het omringende medium kunnen adsorberen op het deeltjesoppervlak, wat bijdraagt aan de algehele lading ervan.
* Chemische aanpassing: Opzettelijke chemische modificaties kunnen geladen groepen in het deeltjesoppervlak introduceren.
2. Elektrostatische afstoting: Wanneer nanodeeltjes dezelfde oppervlaktelading hebben (allemaal positief of allemaal negatief), ervaren ze elektrostatische afstoting. Stel je twee magneten voor met dezelfde polen tegenover elkaar; Ze duwen weg. Deze afstoting voorkomt dat de deeltjes dichtbij genoeg komen om permanente aggregaten te vormen.
3. De debye -laag: Het geladen oppervlak van een nanodeeltje bestaat niet afzonderlijk. Het trekt ionen van tegengestelde lading van het omliggende medium aan en vormt een elektrische dubbele laag die bekend staat als de Debye -laag. Deze laag helpt de oppervlaktelading te beschermen en beïnvloedt de sterkte van de elektrostatische afstoting.
4. Balancing de krachten:
* stabilisatie: Sterke elektrostatische afstoting (vanwege hoge oppervlaktelading en een dikke Debye -laag) houdt nanodeeltjes verspreid en voorkomt aggregatie.
* aggregatie: Als de elektrostatische afstoting zwak is (lage oppervlaktelading of dunne Debye -laag), kunnen aantrekkelijke krachten zoals van der Waals -krachten de afstoting overwinnen, wat leidt tot aggregatie.
5. Controlerende aggregatie:
* pH: De pH van de oplossing kan de oppervlaktelading van nanodeeltjes aanzienlijk beïnvloeden, wat hun stabiliteit beïnvloedt.
* ionensterkte: Het verhogen van de ionsterkte van het medium (meer zout toevoegen) comprimeert de Debye -laag, waardoor de elektrostatische afstoting wordt verminderd en de kans op aggregatie wordt vergroot.
* Oppervlakte -modificatie: Het wijzigen van het deeltjesoppervlak met geladen groepen kan de oppervlaktelading regelen en de stabiliteit verbeteren.
Voorbeelden:
* colloïdale gouden nanodeeltjes: Gouden nanodeeltjes worden vaak gecoat met negatief geladen citraationen om aggregatie te voorkomen.
* Systemen voor medicijnafgifte: Door de oppervlaktelading van nanodeeltjes zorgvuldig aan te passen, kunnen ze worden ontworpen om specifieke cellen of weefsels voor medicijnafgifte te richten.
In wezen zijn elektrostatische krachten als onzichtbare "schilden" die voorkomen dat nanodeeltjes samen klonten. Door de oppervlaktelading en de omliggende omgeving te manipuleren, kunnen wetenschappers de stabiliteit van nanodeeltjes regelen en ze aanpassen voor specifieke toepassingen.
 Hoe het zure regeneffect de natuur?
Hoe het zure regeneffect de natuur?  Wat gebeurt er met dampdruk als suiker een oplossing wordt toegevoegd?
Wat gebeurt er met dampdruk als suiker een oplossing wordt toegevoegd?  Onderzoeken hoe oppervlakken veranderen in contact met reactieve gasfasen onder verschillende omstandigheden
Onderzoeken hoe oppervlakken veranderen in contact met reactieve gasfasen onder verschillende omstandigheden  Rollen van chemie in uw samenleving?
Rollen van chemie in uw samenleving?  Wat bestaat uit 5 koolstofatomen die in een ring zijn?
Wat bestaat uit 5 koolstofatomen die in een ring zijn?
 De afgelopen 12.000 jaar laten een complexere klimaatgeschiedenis zien dan eerder werd gedacht
De afgelopen 12.000 jaar laten een complexere klimaatgeschiedenis zien dan eerder werd gedacht  Van overstromingen in Brazilië en Houston tot brute hitte in Azië:extreem weer lijkt bijna overal
Van overstromingen in Brazilië en Houston tot brute hitte in Azië:extreem weer lijkt bijna overal  Hoe beschrijft u bosbodem?
Hoe beschrijft u bosbodem?  Wie was 's werelds eerste koning?
Wie was 's werelds eerste koning?  Smeltend Noordpoolgebied stuurt een bericht:klimaatverandering is hier op een grote manier
Smeltend Noordpoolgebied stuurt een bericht:klimaatverandering is hier op een grote manier
Hoofdlijnen
- Waar trekt het drugsmetabolisme op?
- Voorbeelden van een recessief allel
- Wat zijn de beperkingen van wetenschappelijke modellen?
- Wat zijn Prions?
- Hoe noem je planten met dikke vlezige weefsels?
- Kunnen antibiotica naast bacteriële infecties ook ziekten bij de mens behandelen?
- Hoe hybride plantenrassen de uitdagingen van voedselzekerheid en klimaatverandering kunnen aanpakken
- Wat is de naam van de subeenheid die wordt gebruikt om DNA en RNA te bouwen?
- Wat waren Bastets fysieke eigenschappen?
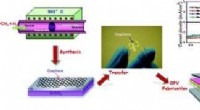
- Grafeen organische fotovoltaïsche, of, zullen joggers t-shirts op een dag hun mobiele telefoons van stroom voorzien?
- Gebruik maken van de diva's van de nanowereld

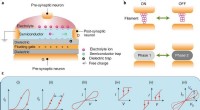
- Een overzicht van opkomende neuromorfe apparaten en architecturen die mogelijk worden gemaakt door nanomaterialen
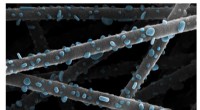
- Proces op nanoschaal kan de komst van goedkopere hi-tech producten versnellen
- Fijnafstemming van de twist tussen 2D-materialen in heterostructuren van van der Waals om elektronica van de volgende generatie te helpen versnellen

 Nachtvogels van Noord-Amerika
Nachtvogels van Noord-Amerika  Welk type axon verspreidt een actiepotentieel sneller?
Welk type axon verspreidt een actiepotentieel sneller?  Wat is het systeem om de ronde aarde in kaart te brengen op een plat oppervlak dat wordt genoemd?
Wat is het systeem om de ronde aarde in kaart te brengen op een plat oppervlak dat wordt genoemd?  Hoe laat stijgt de maan elke nacht?
Hoe laat stijgt de maan elke nacht?  Orde brengen in chaotische bubbels kan mijnbouw duurzamer maken
Orde brengen in chaotische bubbels kan mijnbouw duurzamer maken Wat is de kleur vorm hardheid chemische samenstelling diagnostische eigenschap streep glans breuk gebruik van mineralen?
Wat is de kleur vorm hardheid chemische samenstelling diagnostische eigenschap streep glans breuk gebruik van mineralen?  Als het loont om een eikel te zijn, waarom is dan niet iedereen zo? Een chimpanseestudie biedt inzicht
Als het loont om een eikel te zijn, waarom is dan niet iedereen zo? Een chimpanseestudie biedt inzicht  De normale kracht is dat een oppervlak uitoefent wanneer u een object erover beweegt, waar of onwaar?
De normale kracht is dat een oppervlak uitoefent wanneer u een object erover beweegt, waar of onwaar?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

