
Wetenschap
Intracellulaire nanothermometer heeft ongekende veelzijdigheid
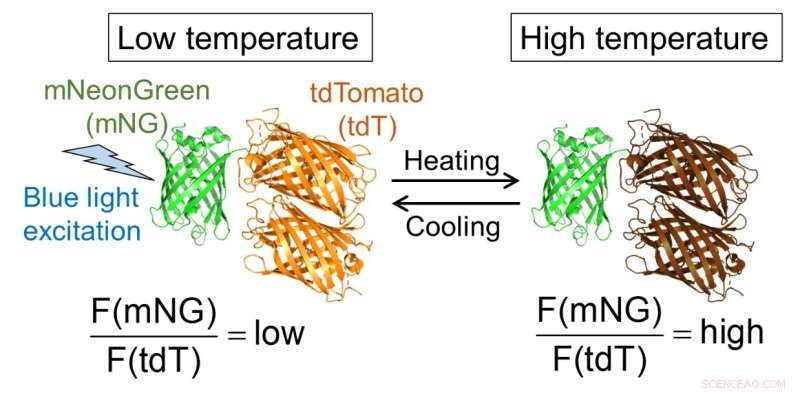
Figuur 1. Moleculair ontwerp van B-gTEMP en de verwachte fluorescentierespons op temperatuur. F(mNG) en F(tdT) zijn de fluorescentie-intensiteit van respectievelijk mNeonGreen en tdTomato. Krediet:Kai Lu et al.
Lichaamstemperatuur is een fundamentele indicator van gezondheid. Intracellulaire temperatuur is ook een basisindicator van cellulaire gezondheid; kankercellen zijn metabolisch actiever en kunnen dus een iets hogere temperatuur hebben dan gezonde cellen. Tot nu toe waren de beschikbare tools voor het testen van dergelijke hypothesen echter niet geschikt voor de taak. In een recent gepubliceerd onderzoek in Nano Letters , hebben onderzoekers van de Universiteit van Osaka en samenwerkende partners experimenteel temperatuurgradiënten in menselijke cellen gemeten en met ongekende precisie. Deze studie zal nieuwe wegen openen in de ontdekking van geneesmiddelen en medisch onderzoek.
Veel onderzoekers vermoeden dat voorbijgaande intracellulaire temperatuurgradiënten een breder effect hebben op de menselijke gezondheid dan algemeen wordt aangenomen, maar waren niet in staat hun hypothesen te testen vanwege de beperkingen van de beschikbare technologie. "De huidige intracellulaire thermische detectietechnologie heeft onvoldoende ruimtelijke, temporele en uitleesresolutie om een aantal al lang bestaande medische hypothesen te beantwoorden", legt Kai Lu, hoofdauteur uit, "maar ons onderzoek verandert dit. Onze genetisch gecodeerde fluorescente nanothermometer overwint eerdere technische hindernissen en zal zijn van onschatbare waarde voor het testen van dergelijke hypothesen."
De op eiwitten gebaseerde nanothermometer van de onderzoekers is gebaseerd op gemoduleerde fluorescentie-output die gevoelig is voor kleine veranderingen in temperatuur in cellen. De uitleessnelheid is minstens 39 keer sneller dan vergelijkbare technologie en duizend keer sneller dan een typisch oogwenk. Met de nanothermometer konden de onderzoekers ontdekken dat intracellulaire warmtediffusie meer dan 5 keer langzamer is dan warmtediffusie in water. Het toonde ook aan dat de uitleesresolutie slechts 0,042 graden Celsius is bij fysiologische temperatuur, wat een nog hogere resolutie is dan die in een vergelijkbare opstelling die duizenden keren langzamer is.
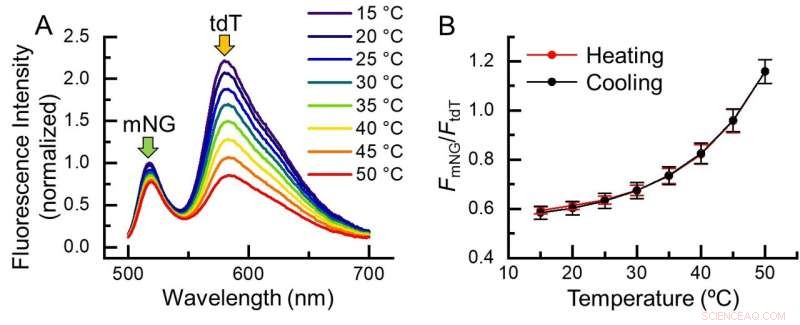
Fig. 2. Temperatuurrespons van B-gTEMP. (A) Fluorescentiespectrum van B-gTEMP bij verschillende temperaturen. mNG:mNeonGreen; tdT:tdTomaat. (B) Fluorescentie-intensiteitsverhouding van mNG tot tdT in reactie op temperatuur tijdens een cyclus van verwarming en koeling. Krediet:Kai Lu et al.
"We hebben de hypothese getest dat er een aanzienlijk temperatuurverschil is tussen de celkern en het cytoplasma", zegt Takeharu Nagai, senior auteur. "We hebben geen significant verschil gevonden, maar testomstandigheden die de typische fysiologie beter nabootsen, kunnen andere resultaten opleveren."
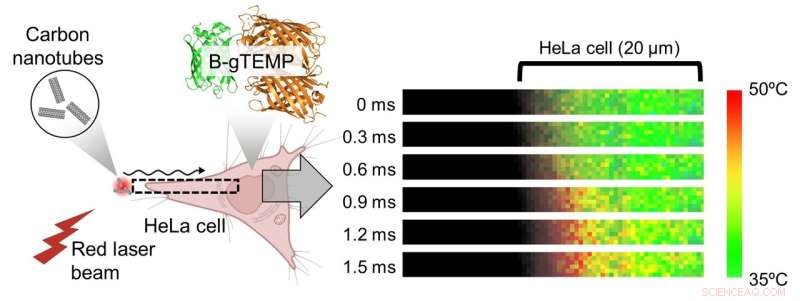
Fig. 3. Snel warmtetransport in cellen. Warmte werd gegenereerd door koolstofnanobuisjes te bestralen met een gefocusseerde rode laserstraal; de warmte verspreidde zich vervolgens in de aangrenzende HeLa-cel. Dit proces werd in realtime vastgelegd door kilohertz-temperatuurbeeldvorming met B-gTEMP. Krediet:Kai Lu et al.
Er zijn verschillende manieren om de functionaliteit van de nanothermometer van de onderzoekers te verbeteren. Een daarvan is om te verbeteren hoe lang het duurt onder microscopische verlichting. Een andere is om het opnieuw te ontwerpen zodat het gevoelig is voor rood of infrarood licht, en dus minder schadelijk is voor cellen voor langdurige beeldvorming. In de tussentijd hebben onderzoekers nu de technologie om intracellulaire temperatuurgradiënten realistisch te onderzoeken en de fysiologie bloot te leggen die aan deze gradiënten ten grondslag ligt. Misschien kunnen met deze kennis ooit medicijnen worden ontworpen om te profiteren van dit ondergewaardeerde aspect van celfysiologie. + Verder verkennen
Ultragevoelige nanothermometer onder omgevingsomstandigheden
 Onderzoekers bepalen de complexe structuur van de receptoren gerelateerd aan opioïdenverslaving
Onderzoekers bepalen de complexe structuur van de receptoren gerelateerd aan opioïdenverslaving Science Fair-project met Cupcakes
Science Fair-project met Cupcakes De architecturen van binnenste mitochondriale membraaneiwitten begrijpen
De architecturen van binnenste mitochondriale membraaneiwitten begrijpen Het produceren van ethaan uit methaan met behulp van een fotochemische lusstrategie
Het produceren van ethaan uit methaan met behulp van een fotochemische lusstrategie Organische fotovoltaïsche cel met 17% efficiëntie en superieure verwerkbaarheid voor coatings op grote oppervlakken
Organische fotovoltaïsche cel met 17% efficiëntie en superieure verwerkbaarheid voor coatings op grote oppervlakken
 Het verhaal van poollicht is zojuist veel groter geworden:onbekende magnetosferische mechanismen onthuld
Het verhaal van poollicht is zojuist veel groter geworden:onbekende magnetosferische mechanismen onthuld Sri Lanka beoordeelt milieuschade door olietankerbrand
Sri Lanka beoordeelt milieuschade door olietankerbrand Geavanceerd programma voor monitoring van droogte- en overstromingsrisico's voor ecologisch kwetsbare regio's
Geavanceerd programma voor monitoring van droogte- en overstromingsrisico's voor ecologisch kwetsbare regio's Tolwegen zijn goed voor het milieu, wetenschappers bevestigen
Tolwegen zijn goed voor het milieu, wetenschappers bevestigen Hoe lawines te voorkomen
Hoe lawines te voorkomen
Hoofdlijnen
- Wat zijn de functies van mRNA & tRNA?
- Wetenschapper roept publiek op om genen van bedreigde vleermuissoorten te ontsluiten
- Charles Lyell: Biography, Theory of Evolution & Facts
- Hoe een 3D-model van een plantencel te maken
- Het testen van chimpansees in Tanzania gedurende tientallen jaren suggereert dat persoonlijkheidstypes stabiel zijn
- Genomics onthult hoe concurrentie tussen bacteriën de impact van vaccinatie beïnvloedt
- Zes soorten neuroglia
- Onderzoek toont aan dat bodemradar fijne wortels in gewassen kan detecteren
- Waarom kunnen we de voetstappen van anderen horen,
- Geen kleine maatregel:onderzoek naar de mechanica van gouden contacten op nanoschaal
- Team realiseert sterke indirecte koppeling in verre nanomechanische resonatoren
- Hybride nanomaterialen zijn veelbelovend voor verbeterde keramische composieten
- Nieuwe ultradunne elektronische films hebben een grotere capaciteit

- Microkammen zorgt voor sterkere, meer geleidende koolstof nanobuisfilms
 Chemicus ontwikkelt nieuwe katalysator voor oxidatie en amidering
Chemicus ontwikkelt nieuwe katalysator voor oxidatie en amidering De temperatuur van het zeeoppervlak heeft een grote invloed op de overleving van koraal outplants
De temperatuur van het zeeoppervlak heeft een grote invloed op de overleving van koraal outplants Een klasse apart:nieuwe factoren sturen het eiwittransport van rode algen chloroplast
Een klasse apart:nieuwe factoren sturen het eiwittransport van rode algen chloroplast Hoe DC-offset te berekenen
Hoe DC-offset te berekenen  Genieten van het uitzicht? Hoe computerspellen kunnen helpen bij het evalueren van landschappen
Genieten van het uitzicht? Hoe computerspellen kunnen helpen bij het evalueren van landschappen Hoe u Joules of Heat te berekenen
Hoe u Joules of Heat te berekenen Baanbrekende toepassing van vochtvasthoudende film om hittestress te verminderen in persoonlijke beschermende pakken
Baanbrekende toepassing van vochtvasthoudende film om hittestress te verminderen in persoonlijke beschermende pakken Ideeën voor een Science Fair-project met behulp van Kool-Aid
Ideeën voor een Science Fair-project met behulp van Kool-Aid
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

