
Wetenschap
Nanomaterialen voor het eerst gebruikt als breedspectrum antimicrobiële middelen
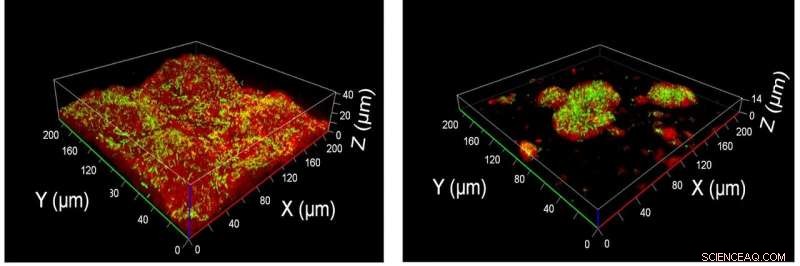
3D-beelden van bacteriën (groen) in een biofilmmatrix (rood) met behandeling met nanozym (rechts) en zonder behandeling met nanozym (links). Het nanozyme doodt de bacteriën en remt de vorming van biofilm Credit:Kritika Khulbe en Kapudeep Karmakar
In een belangrijke doorbraak in de strijd tegen antibioticaresistentie, een onderzoeksteam van het Indian Institute of Science (IISc) heeft een nanomateriaal gesynthetiseerd dat een enzym nabootst en de celmembranen van een reeks ziekteverwekkende bacteriën kan desintegreren. De studie, gepubliceerd in het tijdschrift ACS toegepaste biomaterialen, is een samenwerking tussen onderzoekers van de afdeling Anorganische en Fysische Chemie (IPC) en de afdeling Microbiologie en Celbiologie (MCB).
De ontdekking van antibiotica zorgde voor een revolutie op het gebied van geneeskunde. Tegen de jaren zestig, veel gezondheidsexperts waren zelfs van mening dat de strijd tegen infectieziekten zich in de eindfase bevond. Echter, de afgelopen decennia hebben we een nieuwe uitdaging gezien:de evolutie van resistentie tegen antibiotica bij pathogene bacteriën.
Antibiotica werken meestal door de cellulaire activiteiten van de bacteriën te verstoren. Gedurende vele generaties, grotendeels te danken aan misbruik en overmatig gebruik van antibiotica, verschillende bacteriën hebben resistentie ontwikkeld tegen antibiotica door hun eigen enzymen te produceren die zich op de medicijnen richten.
De celmembranen van alle organismen, inclusief bacteriën, hebben twee lagen lipiden die fosfaatmoleculen bevatten. "Fosfolipide is een essentieel onderdeel van het celmembraan, " legt Kapudeep Karmakar uit, een voormalig Ph.D. student aan MCB en de gezamenlijke eerste auteur van dit artikel samen met Kritika Khulbe, voormalig Ph.D. Student aan IPC. Daarom, de onderzoekers besloten zich op deze fosfolipiden te richten met behulp van nanomaterialen die de bindingen zouden verbreken die de membraandubbellaag bij elkaar houden. Deze nanomaterialen staan bekend als nanozymen. Volgens de auteurs is omdat de nanozymen zich direct richten op de chemische integriteit van de fosfolipiden om het celmembraan te vernietigen, bacteriën kunnen er minder snel resistentie tegen ontwikkelen.
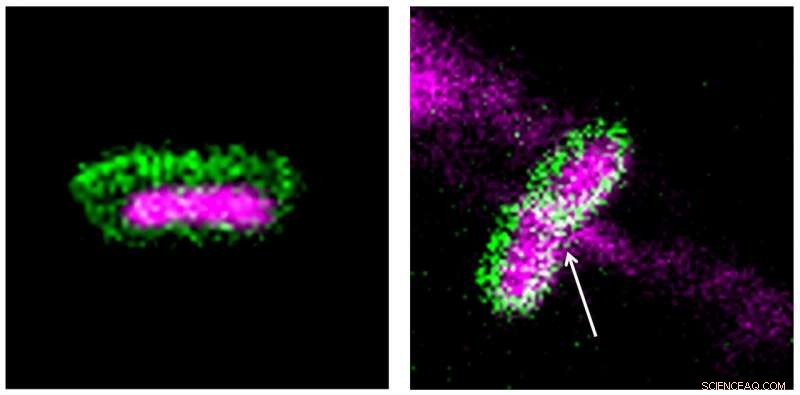
Confocale microscopiebeelden die bacterieel DNA (magenta) en celmembraan (groen) in normale bacteriële cel (links) tonen. DNA sijpelt uit bacteriële cellen wanneer het wordt behandeld met nanozyme (rechts) dat het celmembraan verstoort. Krediet:Kritika Khulbe en Kapudeep Karmakar
Om deze nieuwe verbinding te ontwikkelen, het team synthetiseerde een op ceriumoxide gebaseerd nanozym met behulp van wat bekend staat als een chemische co-precipitatiemethode. In de volgende stap, ze voerden een reactie uit tussen ceriumoxide en natriumpolyacrylaat in een basische oplossing om de nanodeeltjes te coaten met polymeren. De polymeercoating zorgt ervoor dat het nanozyme zich op elk oppervlak of materiaal kan verspreiden en verhoogt de activiteit ervan.
Het nanomateriaal werd vervolgens in het laboratorium getest op verschillende potentieel pathogene bacteriën zoals: Salmonella typhi, Shigella flexneri , Escherichia coli , Vibrio cholerae en Klebsiella pneumoniae , die tyfus veroorzaken, gastro-enteritis, dysenterie, respectievelijk cholera en longontsteking. Wat het team ontdekte, was dat het nanozym hun groei stopte en vervolgens de vorming van biofilm remde - een dicht opeengepakte gemeenschap van bacteriën.
"De meeste antibiotica kunnen niet door biofilms doordringen. Onze nanomaterialen konden zelfs een 10-daagse oude, goed ontwikkelde biofilm en vertoonde antibacteriële activiteit in de biofilm vanwege hun kleine formaat, ' zegt Khulbe.
De onderzoekers testten het nanozyme ook op urinekatheters. Deze medische hulpmiddelen zijn kwetsbaar voor de vorming van pathogene biofilm op hun oppervlak, leiden tot infecties bij patiënten. In een laboratoriumomgeving, het team ontdekte dat de bacteriële hechting aan het katheteroppervlak aanzienlijk vermindert bij behandeling met het nanozyme. Omdat het nanozyme geen onderscheid maakt tussen menselijke en microbiële cellen, de onderzoekers bedekten strategisch alleen het binnenoppervlak van de katheter om de microben te doden. Om hun nanomateriaal in andere medische hulpmiddelen te gebruiken, meer onderzoek zou nodig zijn om ervoor te zorgen dat er geen contact is tussen menselijke cellen en de nanozymen.
 Meteorietinslagen maakten leven op aarde mogelijk
Meteorietinslagen maakten leven op aarde mogelijk Tropische storm Cristobal nadert US Gulf Coast
Tropische storm Cristobal nadert US Gulf Coast Meerdere ecocrises kunnen leiden tot systemische ineenstorting:wetenschappers
Meerdere ecocrises kunnen leiden tot systemische ineenstorting:wetenschappers Natuurlijke hulpbronnen die door mannen en vrouwen verschillend worden gewaardeerd, studie toont
Natuurlijke hulpbronnen die door mannen en vrouwen verschillend worden gewaardeerd, studie toont Hoe Earthships de wederopbouw in bosbrandgebieden veiliger kunnen maken
Hoe Earthships de wederopbouw in bosbrandgebieden veiliger kunnen maken
Hoofdlijnen
- Science Fair-projecten met nagellak
- Wat zijn de leefgebieden van de zes koninkrijken?
- Ontdekking helpt de nauwkeurigheid van CRISPR-Cas9-genbewerking te verbeteren
- Poema's zijn socialer dan eerder werd gedacht
- Hoe de hormonen van de hypofyse te onthouden
- Benchmarking computationele methoden voor metanomen
- Hoe een mRNA-sequentie
- Chloroplast: definitie, structuur en functie (met diagram)
- Hoe een bloeiende legale marihuana-industrie de luchtkwaliteit kan schaden
- Nanotechnologen vormen bijna wrijvingsloos diamantmateriaal

- Team verandert nanostaafjes in multistate schakelaars met een elektronenstraal

- Elektrische velden verwijderen gemakkelijk nanodeeltjes uit bloed

- Nanokatalysator is een gas:nieuwe formule kan de brandstofproductie verbeteren, groener
- Kleine capsules bieden alternatief voor virale toediening van gentherapie
 Legale verkoop van marihuana veroorzaakt toenemende schade aan het milieu
Legale verkoop van marihuana veroorzaakt toenemende schade aan het milieu Nanodeeltjes herstarten de bloedstroom in de hersenen
Nanodeeltjes herstarten de bloedstroom in de hersenen Non-line-of-sight beeldvorming met picoseconde temporele resolutie
Non-line-of-sight beeldvorming met picoseconde temporele resolutie atomen vangen, geen ruimteschepen, met trekbalken
atomen vangen, geen ruimteschepen, met trekbalken China's Silk Road-project loopt in de schulden
China's Silk Road-project loopt in de schulden Leidinggevenden arresteren, veiligheidszorgen belemmeren Huawei's bereik
Leidinggevenden arresteren, veiligheidszorgen belemmeren Huawei's bereik Europa's toekomst is hernieuwbaar
Europa's toekomst is hernieuwbaar Inverse ontwerpsoftware automatiseert het ontwerpproces voor optische, nanofotonische structuren
Inverse ontwerpsoftware automatiseert het ontwerpproces voor optische, nanofotonische structuren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

