
Wetenschap
Vergelijking toont de waarde van DNA-barcodering bij het selecteren van nanodeeltjes
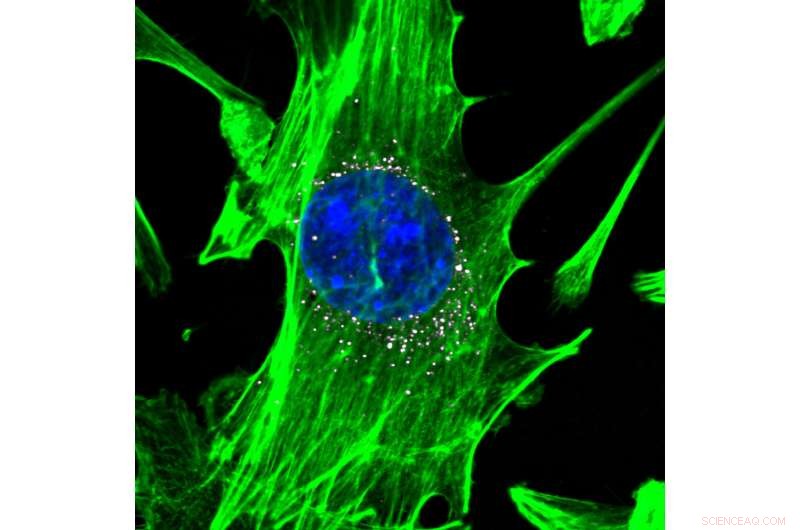
Cellen, gekleurd in groen met blauwe kernen, worden het doelwit van nanodeeltjes met DNA-barcodes (wit). De nanodeeltjes brengen hun DNA-lading efficiënt in de cellen. Krediet:Daryll A. Vanover, Kalina Paulovska, en Cory Sago bij Georgia Tech
De eerste directe vergelijking van in vitro en in vivo screeningtechnieken voor het identificeren van nanodeeltjes die kunnen worden gebruikt om therapeutische moleculen in cellen te transporteren, toont aan dat testen in laboratoriumschalen niet veel helpt om te voorspellen welke nanodeeltjes met succes de cellen van levende dieren zullen binnendringen.
De nieuwe studie toonde de voordelen aan van een in vivo DNA-barcoderingstechniek, die kleine stukjes DNA hecht aan verschillende op lipiden gebaseerde nanodeeltjes die vervolgens in levende dieren worden geïnjecteerd; meer dan honderd nanodeeltjes kunnen worden getest in een enkel dier. DNA-sequencingtechnieken worden vervolgens gebruikt om te identificeren welke nanodeeltjes de cellen van specifieke organen binnenkomen, het maken van de deeltjes kandidaten voor het transport van gentherapieën om moordenaars als hartziekte te behandelen, kanker en de ziekte van Parkinson.
De traditionele techniek om veelbelovende nanodeeltjes te identificeren, onderzoekt hoe de deeltjes levende cellen binnendringen die in laboratoriumschalen worden bewaard. Om de nieuwe en oude screeningstechnieken te vergelijken, de onderzoekers voegden streepjescode nanodeeltjes toe aan levende cellen in laboratoriumschalen, en geïnjecteerd identieke streepjescode nanodeeltjes in levende diermodellen. Ze vonden bijna geen correlatie tussen de nanodeeltjes die in de laboratoriumschaaltests als veelbelovend werden geïdentificeerd en de nanodeeltjes die het goed deden in de muizen.
"DNA-barcodering heeft het potentieel om de wetenschap van het selecteren van nanodeeltjes voor het leveren van gentherapieën vooruit te helpen. " zei James Dahlman, een assistent-professor in de Wallace H. Coulter afdeling Biomedical Engineering aan de Georgia Tech en Emory University en de hoofdonderzoeker van de studie. "Door deze techniek te gebruiken, bedrijven en academische laboratoria zouden veel efficiënter veelbelovende nanodeeltjes kunnen uitkiezen. Dat zou de snelheid kunnen versnellen waarmee op nanodeeltjes gebaseerde therapieën de kliniek binnenkomen, terwijl het aantal vereiste dierproeven wordt verminderd."
Het onderzoek, die wordt ondersteund door de National Institutes of Health, het Instituut voor Kankeronderzoek, Stichting Cystic Fibrosis en Stichting Ziekte van Parkinson, werd op 28 februari in het journaal gerapporteerd Nano-letters . Het onderzoek is uitgevoerd door wetenschappers van het Georgia Institute of Technology en Emory University.

Dit close-upbeeld toont een microfluïdische chip die wordt gebruikt om nanodeeltjes te fabriceren die kunnen worden gebruikt om therapeutische genen aan specifieke organen van het lichaam te leveren. Er zijn gekleurde vloeistoffen toegevoegd om de kanalen te markeren. Krediet:Rob Vilt, Georgië Tech
Genetische therapieën, zoals die gemaakt van DNA of RNA, geconfronteerd met uitdagingen vanwege de moeilijkheid om het nucleïnezuur aan de juiste cellen te leveren. De afgelopen twee decennia heeft wetenschappers hebben nanodeeltjes ontwikkeld die zijn gemaakt van een breed scala aan materialen en die verbindingen zoals cholesterol hebben toegevoegd om deze therapeutische middelen in cellen te helpen transporteren. Maar de ontwikkeling van dragers van nanodeeltjes is vertraagd door de uitdagingen om ze te testen, eerst in celcultuur om veelbelovende nanodeeltjes te identificeren, en later bij dieren. Met miljoenen mogelijke combinaties, het identificeren van de optimale nanodeeltjes om elk orgaan te targeten was overweldigend.
Door DNA-strengen van slechts 58 nucleotiden lang te gebruiken om elk deeltje uniek te identificeren, kunnen onderzoekers de celcultuurscreening helemaal overslaan - en honderd of meer verschillende soorten nanodeeltjes tegelijk testen in slechts een handvol dieren.
"Als je 200 nanodeeltjes op de traditionele manier wilt testen, je zou 600 muizen nodig hebben - drie voor elk type nanodeeltje, " zei Dahlman. "Met behulp van de DNA-barcoderingstechniek, die we Joint Rapid DNA Analysis of Nanoparticles (JORDAN) noemen, we zijn in staat om het testen in slechts drie dieren uit te voeren."
De studie onderzocht de binnenkomst van nanodeeltjes in endotheelcellen en macrofagen voor de in vitro studie, en hetzelfde type cellen uit de long, hart en beenmerg voor de in vivo component. De twee celtypen zijn belangrijk voor een breed scala aan orgaansystemen in het lichaam en spelen een actieve rol bij ziekten die doelwitten kunnen zijn voor nucleïnezuurtherapieën. De studie vergeleek hoe dezelfde 281 lipidenanodeeltjes de streepjescodes afleverden in laboratoriumschalen en levende dieren.
"Er was geen voorspellend vermogen tussen de laboratoriumschaaltests en de dierproeven, " zei Dahlman. "Als de in vitro tests goede voorspellers waren geweest, dan zouden deeltjes die het goed deden in de schaal het ook goed hebben gedaan in de dieren, en deeltjes die het slecht deden in de schaal, zouden het ook slecht hebben gedaan in de dieren. Dat hebben we helemaal niet gezien."

James Dahlman, een assistent-professor in de Wallace H. Coulter Department of Biomedical Engineering aan Georgia Tech en Emory University, bevat een microfluïdische chip die wordt gebruikt om nanodeeltjes te fabriceren die kunnen worden gebruikt om therapeutische genen af te leveren. Krediet:Rob Vilt, Georgië Tech
Het onderzoeksteam, onder leiding van co-eerste auteurs Kalina Paunovska en Cory D. Sago, bestudeerde ook hoe de levering van nanodeeltjes verandert met de micro-omgeving van specifieke weefseltypes. Daarom, ze kwantificeerden hoe 85 nanodeeltjes DNA-barcodes afleverden aan acht celpopulaties in de milt, en ontdekte dat celtypen afgeleid van myeloïde voorlopers de neiging hadden om het doelwit te zijn van vergelijkbare nanodeeltjes.
Onderzoekers zijn niet alleen geïnteresseerd in welke nanodeeltjes de therapieën het meest effectief leveren, maar ook die ze selectief kunnen afleveren aan specifieke organen. Therapeutica gericht op tumoren, bijvoorbeeld, mag alleen aan de tumor worden toegediend en niet aan de omliggende weefsels. Therapeutica voor hartaandoeningen moeten zich ook selectief in het hart ophopen.
De enkelstrengs DNA-barcodesequenties die in de techniek worden gebruikt, zijn ongeveer even groot als antisense-oligonucleotiden, microRNA en siRNA worden ontwikkeld voor mogelijke therapeutische toepassingen. Andere op genen gebaseerde therapieën zijn groter, en er zou aanvullend onderzoek nodig zijn om te bepalen of de techniek ermee zou kunnen worden gebruikt.
Zodra de veelbelovende nanodeeltjes zijn geïdentificeerd met de screening, ze zouden worden onderworpen aan aanvullende tests om hun vermogen om therapieën te leveren te verifiëren. Om te voorkomen dat nanodeeltjes samensmelten, alleen structuren die stabiel zijn in waterige omgevingen kunnen met deze techniek worden getest. Alleen niet-toxische nanodeeltjes kunnen worden gescreend, en onderzoekers moeten controleren op mogelijke ontstekingen die worden gegenereerd door het ingevoegde DNA.
"Nucleïnezuurtherapieën zijn veelbelovend voor de behandeling van een reeks ernstige ziekten, " zei Dahlman. "We hopen dat deze techniek op grote schaal in het veld zal worden gebruikt, en dat het uiteindelijk meer duidelijkheid zal brengen over hoe deze medicijnen cellen beïnvloeden - en hoe we ze op de juiste locaties in het lichaam kunnen krijgen."
 De effecten van water tijdens een titratie-experiment
De effecten van water tijdens een titratie-experiment Subtiele veranderingen in de chemische structuur kunnen de toxiciteit van geneesmiddelen beïnvloeden
Subtiele veranderingen in de chemische structuur kunnen de toxiciteit van geneesmiddelen beïnvloeden Hoe warmteopname berekenen
Hoe warmteopname berekenen
In het dagelijks leven gebruiken mensen de termen warmte en temperatuur onderling uitwisselbaar. Op het gebied van thermodynamica en fysica, echter, hebben de twee termen heel verschillende betekenissen. Als u wilt bereke
 Nieuw onderzoek toont de beperkingen van coördinatie in de chemie aan
Nieuw onderzoek toont de beperkingen van coördinatie in de chemie aan Kenmerken van een proton
Kenmerken van een proton
 De waarde van zeegras bij het veiligstellen van een duurzame planeet
De waarde van zeegras bij het veiligstellen van een duurzame planeet Om de luchtkwaliteit te bewaken, Wetenschappers jagen in het holst van de nacht op methaanpluimen
Om de luchtkwaliteit te bewaken, Wetenschappers jagen in het holst van de nacht op methaanpluimen NASA-NOAA satellietvolgsysteem tropische cycloon Kenanga
NASA-NOAA satellietvolgsysteem tropische cycloon Kenanga Vuurwerk op 4 juli veroorzaakte het op één na hoogste niveau van luchtvervuiling sinds de vakantie in Zuid-Californië in tien jaar
Vuurwerk op 4 juli veroorzaakte het op één na hoogste niveau van luchtvervuiling sinds de vakantie in Zuid-Californië in tien jaar NASA-NOAA-satelliet betrapt orkaan Nana die onder dekking van de nacht aan land komt
NASA-NOAA-satelliet betrapt orkaan Nana die onder dekking van de nacht aan land komt
Hoofdlijnen
- Grote katten in Groot-Brittannië - stedelijke mythe of wetenschappelijk feit?
- Computerprogramma detecteert verschillen tussen menselijke cellen
- Wat zijn de functies van glasplaat & dekglaasjes?
- Temperatuur kan de pollenkleur beïnvloeden
- Roadkill-pieken van fazanten in de herfst en late winter
- De geleidbaarheid van zenuwcellen in het centrale zenuwstelsel
- Hoeveel spieren heb je nodig om te glimlachen?
- Do All Cells Have Mitochondria?
- Verbeteringen in de cryo-elektronenmicroscopie brengen het leven op atomair niveau duidelijker in beeld
- Chemische ingenieurs ontwikkelen nieuwe theorie om verbeterde nanomaterialen te bouwen
- Onderzoek naar composieten van koolstofnanobuisjes voor structurele gezondheidsmonitoring

- Precisieregeling van complexe elektrochemische interfaces voor scheidingen

- Ontwerp van zelfassemblerende eiwit-nanomachines begint te klikken

- Team ontwikkelt nieuwe supergeleidende hybride kristallen

 Magnetische medicijnafgiftemethode kan de manier waarop diepe weefseltumoren en andere ziekten worden behandeld, veranderen
Magnetische medicijnafgiftemethode kan de manier waarop diepe weefseltumoren en andere ziekten worden behandeld, veranderen Wat is natriumbenzoaat?
Wat is natriumbenzoaat?  Supercomputers kunnen cyberdreigingen opsporen
Supercomputers kunnen cyberdreigingen opsporen Een snellere en betrouwbaardere methode om olijfolie te categoriseren is gevalideerd
Een snellere en betrouwbaardere methode om olijfolie te categoriseren is gevalideerd Wolachtig materiaal kan zich herinneren en van vorm veranderen
Wolachtig materiaal kan zich herinneren en van vorm veranderen IJsbindende moleculen stoppen ijsgroei, fungeren als natuurlijke antivries
IJsbindende moleculen stoppen ijsgroei, fungeren als natuurlijke antivries Snakes in Pinal County, Arizona
Snakes in Pinal County, Arizona  TESS levert nieuwe inzichten in een ultrahete wereld
TESS levert nieuwe inzichten in een ultrahete wereld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Portuguese | Swedish | German | Dutch | Danish | Norway | Spanish |

-
Wetenschap © https://nl.scienceaq.com

