
Wetenschap
Nanomedisch behandelconcept combineert NO-gastherapie met uithongering van tumorcellen
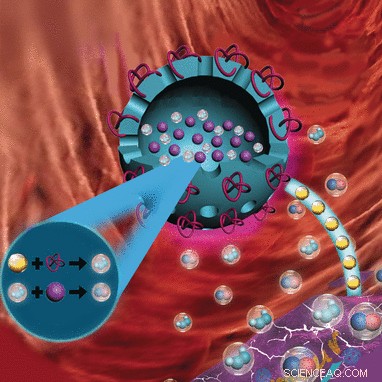
Krediet:Wiley
Biocompatibele nanocapsules, geladen met een aminozuur en uitgerust met een enzym combineren nu twee antitumorstrategieën in een synergetisch behandelconcept. Onderzoekers hopen dat dit de effectiviteit verhoogt en bijwerkingen vermindert. In het journaal Angewandte Chemie , de wetenschappers leggen het concept uit:tumorcellen worden beroofd van hun voedingsstof glucose omdat dit wordt omgezet in het giftige stikstofmonoxide (NO) en waterstofperoxide (H2O2).
NO is een giftig gas dat smog veroorzaakt. Echter, in lage concentraties in het lichaam is het een belangrijk boodschappermolecuul dat onder meer de bloedsomloop en het libido regelt. Het is ook een belangrijk fysiologisch verdedigingswapen tegen schimmels en bacteriën. In hogere concentraties, NO is in staat tumorcellen te doden en de effectiviteit van fotodynamische en radiologische behandelingen te vergroten. Voor klinisch gebruik, NO moet worden vrijgegeven in het doelgebied van een biocompatibele voorloper.
Het natuurlijke aminozuur L-arginine (L-Arg) kan in een dergelijk systeem nuttig zijn, omdat het natieve enzym-induceerbare NO-synthase (iNOS) NO maakt uit L-Arg. NO wordt ook gevormd wanneer L-Arg wordt geoxideerd door H2O2. Dit is interessant omdat de micro-omgeving rond tumoren rijk is aan H2O2. Deze benadering van NO-gastherapie wordt gevolgd door onderzoekers van de Universiteit van Shenzhen (China), de National Institutes of Health (Bethesda, VS), en de Universiteit van Maryland (College Park, VS). Hun speciale draai is om deze gastherapie te combineren met een methode om kankercellen uit te hongeren in een synergetische behandeling.
In plaats van een tumor uit te hongeren door de bloedvaten te blokkeren die hem voeden, de onderzoekers willen de glucose die de tumor nodig heeft voor voeding verwijderen door het te consumeren in een stofwisselingsreactie:het enzym glucose-oxidase (GOx) zet de glucose om in gluconzuur en H2O2. De verhoogde H2O2-concentratie is een nuttige bijwerking, omdat H2O2 zowel cytotoxisch is als de afgifte van NO uit L-Arg versnelt. Een ander nuttig neveneffect is dat H2O2 en NO reageren om zeer giftige peroxynitrieten te vormen die de tumorcellen beschadigen.
Het onderzoeksteam onder leiding van Peng Huang, Tianfu Wang, en Xiaoyuan Chen heeft nu een belangrijke mijlpaal bereikt in de ontwikkeling van dit concept. Ze hebben biocompatibele, biologisch afbreekbaar, poreuze nanocapsules gemaakt van organosilicaten die GOx en L-Arg gelijktijdig in tumorcellen transporteren. GOx is gebonden aan het oppervlak; L-Arg wordt in de capsule bewaard. Terwijl de GOx direct na injectie van de nanocapsules in de tumor actief is, L-Arg wordt beetje bij beetje vrijgegeven, eerst door de capsuleporiën, dan als de capsule uiteenvalt. Door hun grote holte kunnen de capsules ook dienen als ultrasoon contrastmateriaal voor een betere lokalisatie van de tumor.
Experimenten met zowel celculturen als muizen hebben het significante synergetische effect van deze combinatietherapie aangetoond, die met succes de celgroei remt, initieert celdood, en krimpt de tumoren bij muizen.
 Batterijen voor elektrische auto's inspireren veiliger, goedkopere manier om verbindingen te maken die in medicijnen worden gebruikt
Batterijen voor elektrische auto's inspireren veiliger, goedkopere manier om verbindingen te maken die in medicijnen worden gebruikt Betere thermo-elektrische eigenschappen bereikt in n-type composiet
Betere thermo-elektrische eigenschappen bereikt in n-type composiet Dynamische hydrogel die wordt gebruikt om zachte robotcomponenten en LEGO-achtige bouwstenen te maken
Dynamische hydrogel die wordt gebruikt om zachte robotcomponenten en LEGO-achtige bouwstenen te maken Innovatie kan de detectie van COVID-19-infecties verbeteren
Innovatie kan de detectie van COVID-19-infecties verbeteren De juiste formule voor het opschalen van de productie van veelbelovend materiaal om water te decontamineren
De juiste formule voor het opschalen van de productie van veelbelovend materiaal om water te decontamineren
 Aswolken van Antarctische vulkanen kunnen het luchtverkeer op het zuidelijk halfrond verstoren
Aswolken van Antarctische vulkanen kunnen het luchtverkeer op het zuidelijk halfrond verstoren Welke aanpassingen zorgen ervoor dat Toco Toucans tot leven komen?
Welke aanpassingen zorgen ervoor dat Toco Toucans tot leven komen?  NASA's terra-satelliet vangt de ondergang van post-tropische cycloon Marco
NASA's terra-satelliet vangt de ondergang van post-tropische cycloon Marco Sterke aardbeving schudt het Indonesische eiland Sulawesi door elkaar
Sterke aardbeving schudt het Indonesische eiland Sulawesi door elkaar Kenmerken van een Flood Plain
Kenmerken van een Flood Plain
Hoofdlijnen
- Maken regenachtige dagen je echt down?
- U kunt gecodeerde woorden lezen - onder bepaalde omstandigheden
- Functies van menselijke organen
- We kregen te maken met misbruik omdat we mensen vroegen om wespen te doden voor de wetenschap - hier is waarom het de moeite waard was
- Onderzoekers bestuderen de pathobiologie van antibiotische nevenreacties
- Gezondheidsonderzoekers visualiseren een leven in silico
- Voeding door mensen verandert het gedrag en de fysiologie van groene schildpadden op de Canarische Eilanden
- Nieuwe high-throughput sequencing-technologieën onthullen een wereld van op elkaar inwerkende micro-organismen
- M-fase: wat gebeurt er in deze fase van de celcyclus?
- DNA-schade over een cellulaire barrière hangt af van de dikte van de barrière

- Realtime beeldvorming van celcomponenten inclusief DNA

- Antilichamen inhuren als bouwers van nanotechnologie

- Onderzoekers ontwikkelen kwantumdot-smartphoneapparaat om COVID-19 te diagnosticeren en te volgen

- Nanodeeltjessysteem legt biomarker voor hartaandoeningen vast uit bloed voor diepgaande analyse
 Carbonitride-aerogels bemiddelen de fotokatalytische omzetting van water
Carbonitride-aerogels bemiddelen de fotokatalytische omzetting van water Hoe maak je een 3D-model van het spierenstelsel voor een wetenschapsklasse
Hoe maak je een 3D-model van het spierenstelsel voor een wetenschapsklasse Wat is latente warmteoverdracht?
Wat is latente warmteoverdracht?  Arctisch zee-ijsverlies en de Euraziatische trend van winterkoeling:is er een verband?
Arctisch zee-ijsverlies en de Euraziatische trend van winterkoeling:is er een verband? Nieuw onderzoek toont aan dat de groei van de Oost-Antarctische ijskap minder was dan eerder werd gesuggereerd
Nieuw onderzoek toont aan dat de groei van de Oost-Antarctische ijskap minder was dan eerder werd gesuggereerd Protostar vertoont een vreemde geometrie
Protostar vertoont een vreemde geometrie Doorbraak in de digitale chemie verandert woorden in moleculen
Doorbraak in de digitale chemie verandert woorden in moleculen De versnelde uitdijing van het heelal verklaren zonder donkere energie
De versnelde uitdijing van het heelal verklaren zonder donkere energie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Portuguese | Swedish | Dutch | Danish | Norway | Italian | German |

-
Wetenschap © https://nl.scienceaq.com

