
Wetenschap
Koolstofnanobuisjes gebruiken voor medicijnafgifte
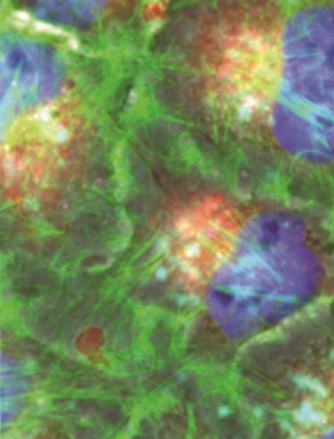
Cellen met miljoenen nanobuisjes omhuld met eiwit. Het actine-cytoskelet is groen, de kern is in blauw, de intracellulaire lipideblaasjes zijn rood, en de nanobuisjes zijn in cyaan. Krediet:Carnegie Mellon University Materials Science and Engineering
Koolstof nanobuisjes, of kleine holle cilinders van één atoom dikke koolstofplaten, hebben een ongelooflijk potentieel voor een breed scala aan toepassingen vanwege hun sterkte, flexibiliteit, en andere unieke krachtige eigenschappen. Ze zijn vooral veelbelovend in nanotechnologie en elektronicatoepassingen, maar Kris Dahl en Mohammad Islam van de Carnegie Mellon University zijn op een interdisciplinaire missie om deze koolstofnanobuisjes een nieuw gebruik te geven - in de geneeskunde.
Door hun respectieve expertises te combineren, Dahl, een universitair hoofddocent Chemische Technologie en Biomedische Technologie, en de islam, een universitair hoofddocent Materials Science and Engineering, werken al jaren samen om veel vragen te beantwoorden met betrekking tot het gebruik van op koolstof nanobuisjes gebaseerde structuren voor medicijnafgifte.
Door de jaren heen, Dahl en Islam hebben aanzienlijke vooruitgang geboekt in het biomedische onderzoek naar koolstofnanobuisjes - alleen in 2016, ze hebben al twee artikelen gepubliceerd waarin hun onderzoek wordt beschreven met betrekking tot technische eiwitten die zich om specifieke soorten medicijnen wikkelen, zodat ze effectiever kunnen worden toegediend. De drugs, wanneer het wordt afgeleverd aan de lichaamscellen, op het oppervlak van de koolstofnanobuisjes zitten, worden dan bedekt door eiwitten.
Foto een hond een pil voeren. Om dat te kunnen doen, men zou het in kaas wikkelen om het medicijn te maskeren en het aantrekkelijker te maken. In een vergelijkbare ader, om de medicijnafgifte te verbeteren, Dahl en Islam hebben eiwitten ontwikkeld die zich om de met medicijnen beklede koolstofnanobuisjes wikkelen. de cellen, die van deze eiwitten houden, nemen het medicijn gemakkelijker op - net zoals een hond de met kaas omhulde pil gemakkelijker zou eten.
"Het mooie van het gebruik van koolstofnanobuisjes om medicijnen af te leveren, is dat, wetenschappelijk, ze zijn gewoon koolstof, " legt Dahl uit. "Ze lijken op grafiet in potloden, diamant, of char - ze zijn gewoon op een andere manier georganiseerd. Maar omdat ze op deze bepaalde manier van tralies zijn voorzien, cellen breken ze niet af. Een ander voordeel van deze methode van medicijnafgifte is het feit dat deze nanobuisjes bijna volledig inert zijn voor de cel. Je kunt er tientallen miljoenen in de cel krijgen voordat er een echte impact op de cel is. en dat betekent dat je een enorme hoeveelheid van een medicijn kunt afgeven en dat het de cellen niet echt verstoort."
De twee artikelen die dit jaar zijn gepubliceerd, getiteld "Verbeterde intracellulaire levering van kleine moleculen en geneesmiddelen via niet-covalente ternaire dispersies van enkelwandige koolstofnanobuisjes" en "Het leveren van enkelwandige koolstofnanobuizen aan de kern met behulp van gemanipuleerde nucleaire eiwitdomeinen, " zijn een enorme stap in de vooruitgang van dit veld. Als cellen meer kans hebben om grote hoeveelheden van het medicijn dat wordt afgeleverd te absorberen, dan neemt de werkzaamheid van het medicijn aanzienlijk toe.
De volgende vraag om aan te pakken? Hoe specifieke cellen te targeten.
"Nu we begrijpen hoe we koolstofnanobuisjes kunnen verspreiden, hoe de toxiciteit te beheersen, hoe ze aan de cellen te leveren, hoe ze te detecteren of te identificeren waar ze zich in de cel bevinden - nu zijn we op een plek waar we kunnen beginnen met het richten op specifieke cellen, ", zegt Islam. "Omdat koolstofnanobuisjes zo'n groot oppervlak hebben en ze met miljoenen de cel in gaan, je kunt een zeer hoge efficiëntie van levering aan een specifieke cel hebben."
In juni, Dahl en Islam zullen elk aspecten van dit werk presenteren op het Carbon Nanostructures in Medicine and Biology Symposium van de Electrochemical Society-conferentie, een ontmoetingsplaats waar leiders in het veld al lang de vooruitgang in nanomateriaaltechnologie en -wetenschap hebben besproken. Dahl en Islam zijn trots dat hun samenwerking innovatie mogelijk heeft gemaakt op het gebied van bionanomedicine en medicijnafgifte, belichaamt de Carnegie Mellon-geest van interdisciplinair onderzoek.

Kris Dahl (Associate Professor of Chemical Engineering and Biomedical Engineering aan Carnegie Mellon University) en Mohammad Islam (Associate Research Professor of Materials Science and Engineering aan Carnegie Mellon University)
 Een nieuwe katalysator voor energierijke aluminium-luchtstroombatterijen
Een nieuwe katalysator voor energierijke aluminium-luchtstroombatterijen Het meest nauwkeurige beeld van Zika tot nu toe creëert potentieel voor therapieën
Het meest nauwkeurige beeld van Zika tot nu toe creëert potentieel voor therapieën Stabiliserende zilverfilms voor zeer efficiënte brandstofcellen
Stabiliserende zilverfilms voor zeer efficiënte brandstofcellen De geboorte van een nieuw eiwit
De geboorte van een nieuw eiwit Nieuwe methode voor het identificeren van koolstofverbindingen afkomstig van fossiele brandstoffen
Nieuwe methode voor het identificeren van koolstofverbindingen afkomstig van fossiele brandstoffen
 Aanpasbaar, schaalbare en kosteneffectieve lokale oplossing voor de preventie van stedelijke overstromingen
Aanpasbaar, schaalbare en kosteneffectieve lokale oplossing voor de preventie van stedelijke overstromingen Overstromingen sluiten luchthaven in Indiase toeristische hotspot van Kerala
Overstromingen sluiten luchthaven in Indiase toeristische hotspot van Kerala Hittegolf Canberra breekt records te midden van bosbranden
Hittegolf Canberra breekt records te midden van bosbranden Maleisië laat het regenen terwijl Indonesische smog de lucht vervuilt
Maleisië laat het regenen terwijl Indonesische smog de lucht vervuilt Rapportkaarten op zeeniveau in de VS:gegevens uit 2019 dragen bij aan de trend in versnelling
Rapportkaarten op zeeniveau in de VS:gegevens uit 2019 dragen bij aan de trend in versnelling
Hoofdlijnen
- Soorten menselijke schedelvormen
- Wat is de relatie tussen een chromosoom en een allel?
- "DNA Model Project Ideas
- Het mysterie van pollenbuisgeleiding ontrafelen
- Een nieuwe kijk op toerisme en zijn bijdrage aan natuurbehoud in Nieuw-Zeeland
- Over leverfuncties in het menselijk lichaam
- In het verleden werpen helpt de toekomst van de visserij te onthullen
- Hoe spreken felle kleuren kinderen aan?
- Hoe werkt ADP naar ATP?
- Nieuwe spectroscopiemethode kan leiden tot betere optische apparaten
- Koelhout:Ingenieurs creëren sterk, duurzame oplossing voor passieve koeling

- Trojaanse paardenproteïnen zijn een stap voorwaarts voor therapeutische benaderingen op basis van nanodeeltjes tegen kanker en dementie
- Controle van de laadtoestand van kwantumstippen van organische moleculen in een 2D-nanoarray

- Nanobuis-groeitheorie experimenteel bevestigd

 Twijfels over veiligheid Flints water 6 jaar na crisis
Twijfels over veiligheid Flints water 6 jaar na crisis Zwitserse rechtbank verklaart chauffeur Uber-medewerker
Zwitserse rechtbank verklaart chauffeur Uber-medewerker Zwaartekrachtgolven laten een waarneembaar merkteken achter, natuurkundigen zeggen:
Zwaartekrachtgolven laten een waarneembaar merkteken achter, natuurkundigen zeggen: Technologie kan bodemherstel na olielozingen helpen versnellen
Technologie kan bodemherstel na olielozingen helpen versnellen Hoge gehalten aan geneesmiddelen in het Humber-estuarium
Hoge gehalten aan geneesmiddelen in het Humber-estuarium Hoe het magneto-elastische effect de magnetische eigenschappen van nano-elementen kan regelen
Hoe het magneto-elastische effect de magnetische eigenschappen van nano-elementen kan regelen Slechts zeven fotonen kunnen zich gedragen als miljarden
Slechts zeven fotonen kunnen zich gedragen als miljarden Very Large Telescope ziet ster dansen rond superzwaar zwart gat bewijst Einstein gelijk
Very Large Telescope ziet ster dansen rond superzwaar zwart gat bewijst Einstein gelijk
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | German | Dutch | Danish | Swedish | Norway |

-
Wetenschap © https://nl.scienceaq.com

