
Wetenschap
RNA gedragen door nieuwe nanodeeltjes kan genen in veel organen tot zwijgen brengen, kan worden ingezet om kanker te behandelen
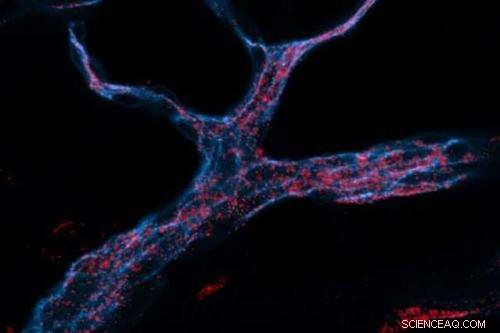
MIT-ingenieurs ontwierpen RNA-dragende nanodeeltjes (rood) die kunnen worden opgenomen door endotheelcellen (blauw gekleurd). Krediet:Aude Thiriot/Harvard
RNA-interferentie (RNAi), een techniek die specifieke genen in levende cellen kan uitschakelen, heeft een groot potentieel voor de behandeling van vele ziekten die worden veroorzaakt door slecht werkende genen. Echter, het was voor wetenschappers moeilijk om veilige en effectieve manieren te vinden om genblokkerend RNA aan de juiste doelen te leveren.
Tot dit punt, onderzoekers hebben de beste resultaten behaald met RNAi gericht op leveraandoeningen, deels omdat het een natuurlijke bestemming is voor nanodeeltjes. Maar nu, in een studie die verschijnt in het nummer van 11 mei van Natuur Nanotechnologie , een door MIT geleid team meldt dat het tot nu toe de krachtigste RNAi-genuitschakeling heeft bereikt in niet-leverweefsels.
Met behulp van nanodeeltjes die zijn ontworpen en gescreend op endotheliale afgifte van korte strengen RNA, siRNA genaamd, de onderzoekers waren in staat om RNAi te richten op endotheelcellen, die de bekleding van de meeste organen vormen. Dit verhoogt de mogelijkheid om RNAi te gebruiken voor de behandeling van vele soorten ziekten, waaronder kanker en hart- en vaatziekten, zeggen de onderzoekers.
"Er is een groeiende hoeveelheid opwinding over de levering aan de lever in het bijzonder, maar om het brede potentieel van RNAi-therapeutica te bereiken, het is belangrijk dat we ook andere delen van het lichaam kunnen bereiken, " zegt Daniël Anderson, de Samuel A. Goldblith universitair hoofddocent chemische technologie, een lid van MIT's Koch Institute for Integrative Cancer Research en Institute for Medical Engineering and Science, en een van de senior auteurs van het papier.
De andere senior auteur van de krant is Robert Langer, de David H. Koch Institute Professor aan het MIT en een lid van het Koch Institute. Hoofdauteurs zijn MIT-student James Dahlman en Carmen Barnes van Alnylam Pharmaceuticals.
Gerichte levering
RNAi is een natuurlijk voorkomend proces, ontdekt in 1998, waardoor cellen hun genetische expressie kunnen controleren. Genetische informatie wordt normaal gesproken van DNA in de kern naar ribosomen getransporteerd, celstructuren waar eiwitten worden gemaakt. Korte strengen RNA, siRNA genaamd, binden aan het boodschapper-RNA dat deze genetische informatie draagt, voorkomen dat het het ribosoom bereikt.
Anderson en Langer hebben eerder nanodeeltjes ontwikkeld, nu in klinische ontwikkeling, dat siRNA kan afgeven aan levercellen die hepatocyten worden genoemd door de nucleïnezuren te coaten in vetachtige materialen die lipidoïden worden genoemd. Hepatocyten grijpen deze deeltjes vast omdat ze lijken op de vetdruppels die in het bloed circuleren nadat een vetrijke maaltijd is geconsumeerd.
"De lever is een natuurlijke bestemming voor nanodeeltjes, Anderson zegt. Dat betekent niet dat het gemakkelijk is om RNA aan de lever te leveren, maar het betekent wel dat als je nanodeeltjes in het bloed injecteert, ze zullen daar waarschijnlijk eindigen."
Wetenschappers hebben enig succes gehad met het afleveren van RNA aan niet-leverorganen, maar het MIT-team wilde een aanpak bedenken die RNAi kon bereiken met lagere doses RNA, wat de behandeling effectiever en veiliger zou kunnen maken.
De nieuwe MIT-deeltjes bestaan uit drie of meer concentrische bollen gemaakt van korte ketens van een chemisch gemodificeerd polymeer. RNA is verpakt in elke bol en wordt vrijgegeven zodra de deeltjes een doelcel binnenkomen.
Gen-uitschakeling
Een belangrijk kenmerk van het MIT-systeem is dat de wetenschappers in staat waren om een "bibliotheek" van veel verschillende materialen te creëren en snel hun potentieel als bezorgers te evalueren. Ze testten ongeveer 2, 400 varianten van hun deeltjes in baarmoederhalskankercellen door te meten of ze een gen konden uitschakelen dat codeert voor een fluorescerend eiwit dat aan de cellen was toegevoegd. Vervolgens testten ze de meest veelbelovende daarvan in endotheelcellen om te zien of ze konden interfereren met een gen genaamd TIE2. die bijna uitsluitend tot expressie wordt gebracht in endotheelcellen.
Met de best presterende deeltjes, de onderzoekers verminderden de genexpressie met meer dan 50 procent, voor een dosis van slechts 0,20 milligram per kilogram oplossing - ongeveer een honderdste van de hoeveelheid die nodig is met bestaande endotheliale RNAi-afgiftevehikels. Ze toonden ook aan dat ze tot vijf genen tegelijk konden blokkeren door verschillende RNA-sequenties af te leveren.
De beste resultaten werden gezien in longendotheelcellen, maar de deeltjes leverden ook met succes RNA aan de nieren en het hart, onder andere organen. Hoewel de deeltjes endotheelcellen in de lever binnendringen, ze kwamen niet in leverhepatocyten.
"Wat interessant is, is dat door de chemie van het nanodeeltje te veranderen, je de levering aan verschillende delen van het lichaam kunt beïnvloeden, omdat de andere formuleringen waaraan we hebben gewerkt zeer krachtig zijn voor hepatocyten, maar niet zo krachtig voor endotheelweefsels, ' zegt Anderson.
Om het potentieel voor de behandeling van longziekte aan te tonen, de onderzoekers gebruikten de nanodeeltjes om twee genen te blokkeren die betrokken zijn bij longkanker:VEGF-receptor 1 en Dll4, die de groei van bloedvaten bevorderen die tumoren voeden. Door deze in longendotheelcellen te blokkeren, de onderzoekers waren in staat om de groei van longtumoren bij muizen te vertragen en ook de verspreiding van uitgezaaide tumoren te verminderen.
Masanori Aikawa, een universitair hoofddocent geneeskunde aan de Harvard Medical School, beschrijft de nieuwe technologie als "een monumentale bijdrage" die onderzoekers zou moeten helpen nieuwe behandelingen te ontwikkelen en meer te leren over ziekten van endotheelweefsel zoals atherosclerose en diabetische retinopathie, die blindheid kan veroorzaken.
"Endothele cellen spelen een zeer belangrijke rol in meerdere stappen van vele ziekten, vanaf het begin tot het begin van klinische complicaties, " zegt Aikawa, die geen deel uitmaakte van het onderzoeksteam. "Dit soort technologie geeft ons een extreem krachtig hulpmiddel dat ons kan helpen deze verwoestende vaatziekten te begrijpen."
De onderzoekers zijn van plan om aanvullende potentiële doelen te testen in de hoop dat deze deeltjes uiteindelijk kunnen worden ingezet om kanker te behandelen, atherosclerose, en andere ziekten.
Dit verhaal is opnieuw gepubliceerd met dank aan MIT News (web.mit.edu/newsoffice/), een populaire site met nieuws over MIT-onderzoek, innovatie en onderwijs.
 Onderzoek geeft nieuw lichtpuntje voor zonnebrandstof
Onderzoek geeft nieuw lichtpuntje voor zonnebrandstof Hoe komt zure regen de watercyclus binnen?
Hoe komt zure regen de watercyclus binnen?  Een Bubble Gum Science-project maken
Een Bubble Gum Science-project maken Onderzoekers bewijzen dat water meerdere vloeibare toestanden heeft
Onderzoekers bewijzen dat water meerdere vloeibare toestanden heeft Door metaal gekatalyseerde reacties die enantioselectief zijn gemaakt met behulp van chiraal kation
Door metaal gekatalyseerde reacties die enantioselectief zijn gemaakt met behulp van chiraal kation
Hoofdlijnen
- Hoe extremofielen werken
- Verkoudheidsvirussen onthullen een van hun sterke punten
- Walviskarkas opgegraven van Australisch strand vanwege angst voor haaien
- Monniksparkieten vallen Mexico binnen
- VS keuren herstelplan voor Mexicaanse wolven goed
- Cat Chromosome-informatie
- Uitbreidingen van het cytoplasma
- Tabaksplanten als levensredders
- Linkshandige vis en asymmetrische hersenen
- Studie wijst op nieuw wapen in strijd tegen dodelijke schimmels

- Biofysici construeren complexe hybride structuren met behulp van DNA en eiwitten

- Mix van grafeen nanoribbons, polymeer heeft potentie voor auto's, Frisdrank, bier

- Verdere details onthuld over een zeer efficiënt medicijnafgiftesysteem tegen kanker
- Composiet organisch/anorganisch thermo-elektrisch is meer dan de som der delen
 Nieuwe milliseconde pulsar ontdekt
Nieuwe milliseconde pulsar ontdekt Nieuwe catastrofale veranderlijke ster ontdekt
Nieuwe catastrofale veranderlijke ster ontdekt Hoe maken planten hun eigen voedsel?
Hoe maken planten hun eigen voedsel?  Wat is het verschil tussen een transformator en een gelijkrichter?
Wat is het verschil tussen een transformator en een gelijkrichter?  Hoeveel chromosomen zijn er in cellen van het menselijk lichaam?
Hoeveel chromosomen zijn er in cellen van het menselijk lichaam?  Wat zijn de voor- en nadelen van doelgerichte voorbeelden?
Wat zijn de voor- en nadelen van doelgerichte voorbeelden?  Alodine Vs. anodiseren
Alodine Vs. anodiseren  Beheersing van stromen vloeibaar metaal bij kamertemperatuur
Beheersing van stromen vloeibaar metaal bij kamertemperatuur
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

