
Wetenschap
RNA-interferentie verbeteren
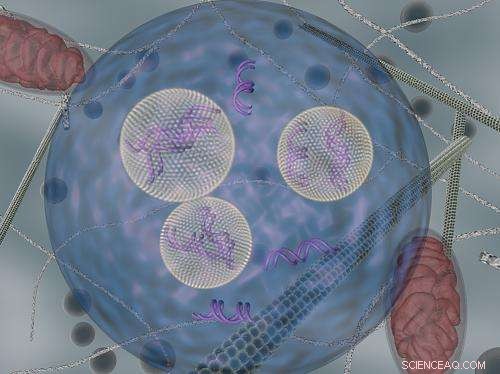
Lipide-nanodeeltjes (die siRNA dragen) worden getoond terwijl ze in cellen worden getransporteerd met behulp van endocytische blaasjes. Krediet:DARIA ALAKHOVA EN GAURAV SAHAY
Nanodeeltjes die korte strengen RNA afgeven, bieden een manier om kanker en andere ziekten te behandelen door slecht werkende genen uit te schakelen. Hoewel deze benadering enige belofte heeft getoond, wetenschappers weten nog steeds niet precies wat er met de nanodeeltjes gebeurt als ze eenmaal in hun doelcellen zijn gekomen.
Een nieuwe studie van MIT werpt licht op het lot van de nanodeeltjes en suggereert nieuwe manieren om de afgifte van de RNA-strengen die ze dragen te maximaliseren. bekend als kort interfererend RNA (siRNA).
"We hebben nanodeeltjes kunnen ontwikkelen die nuttige ladingen in cellen kunnen afleveren, maar we begrepen niet echt hoe ze het deden, " zegt Daniël Anderson, de Samuel Goldblith Associate Professor of Chemical Engineering aan het MIT. "Als je eenmaal weet hoe het werkt, er is potentieel dat je aan het systeem kunt sleutelen en het beter kunt laten werken."
Anderson, een lid van MIT's Koch Institute for Integrative Cancer Research en MIT's Institute for Medical Engineering and Science, is de leider van een onderzoeksteam dat wilde onderzoeken hoe de nanodeeltjes en hun nuttige lading van medicijnen worden verwerkt op cellulair en subcellulair niveau. Hun bevindingen verschijnen in het nummer van 23 juni van: Natuur Biotechnologie . Robert Langer, de David H. Koch Institute Professor aan het MIT, is ook auteur van het artikel.
Een RNA-afleveringsbenadering die bijzonder veelbelovend is gebleken, is het verpakken van de strengen met een lipideachtig materiaal; soortgelijke deeltjes zijn nu in klinische ontwikkeling voor leverkanker en andere ziekten.
Via een proces dat RNA-interferentie wordt genoemd, siRNA richt zich op boodschapper-RNA (mRNA), die genetische instructies van het DNA van een cel naar de rest van de cel draagt. Wanneer siRNA bindt aan mRNA, de boodschap die door dat mRNA wordt gedragen, wordt vernietigd. Door dat proces te benutten, kunnen wetenschappers genen uitschakelen waardoor kankercellen ongecontroleerd kunnen groeien.
Wetenschappers wisten al dat siRNA-dragende nanodeeltjes cellen binnendringen via een proces, endocytose genoemd, waardoor cellen grote moleculen opslokken. Het MIT-team ontdekte dat zodra de nanodeeltjes cellen binnenkomen, ze vast komen te zitten in bellen die bekend staan als endocytische blaasjes. Dit voorkomt dat het grootste deel van het siRNA zijn doel-mRNA bereikt, die zich in het cytosol van de cel (het hoofdlichaam van de cel) bevindt.
Dit gebeurt zelfs met de meest effectieve siRNA-afgiftematerialen, wat suggereert dat er veel ruimte is om het leveringspercentage te verbeteren, zegt Anderson.
"Wij geloven dat deze deeltjes efficiënter kunnen worden gemaakt. Ze zijn al zeer efficiënt, tot het punt waarop microgram geneesmiddel per kilogram dier kan werken, maar dit soort onderzoeken geven ons aanwijzingen over hoe we de prestaties kunnen verbeteren, ' zegt Anderson.
Moleculaire verkeersopstopping
De onderzoekers ontdekten dat zodra cellen de lipide-RNA-nanodeeltjes absorberen, ze worden binnen ongeveer een uur afgebroken en uit de cellen uitgescheiden.
Ze identificeerden ook een eiwit genaamd Niemann Pick type C1 (NPC1) als een van de belangrijkste factoren in het recyclingproces van nanodeeltjes. Zonder dit eiwit de deeltjes konden niet uit de cellen worden uitgescheiden, waardoor het siRNA meer tijd heeft om zijn doelen te bereiken. "In de afwezigheid van de NPC1, er is een verkeersopstopping, en siRNA krijgt meer tijd om uit die file te ontsnappen omdat er een achterstand is, " zegt Gaurav Sahay, een MIT-postdoc en hoofdauteur van het Nature Biotechnology-paper.
In studies van cellen die in het laboratorium zijn gekweekt zonder NPC1, de onderzoekers ontdekten dat het niveau van genuitschakeling bereikt met RNA-interferentie 10 tot 15 keer groter was dan dat in normale cellen.
Gebrek aan NPC1 veroorzaakt ook een zeldzame lysosomale stapelingsziekte die meestal fataal is in de kindertijd. De bevindingen suggereren dat patiënten met deze aandoening veel baat kunnen hebben bij mogelijke RNA-interferentietherapie die door dit type nanodeeltje wordt geleverd, zeggen de onderzoekers. Ze zijn nu van plan om de effecten te bestuderen van het uitschakelen van het NPC1-gen op de afgifte van siRNA bij dieren. met het oog op het testen van mogelijke siRNA-behandelingen voor de aandoening.
De onderzoekers zoeken ook naar andere factoren die betrokken zijn bij het recyclen van nanodeeltjes en die goede doelen kunnen zijn om het recyclingproces mogelijk te vertragen of te blokkeren, waarvan zij denken dat ze kunnen helpen om RNA-interferentiegeneesmiddelen veel krachtiger te maken. Mogelijke manieren om dat te doen, zijn onder meer het geven van een medicijn dat de recycling van nanodeeltjes verstoort, of het creëren van nanodeeltjesmaterialen die het recyclingproces effectiever kunnen omzeilen.
"Dit artikel beschrijft een nieuwe en zeer belangrijke manier om de potentie van siRNA-afgiftesystemen te verbeteren door eiwitten te remmen die geïmporteerd materiaal uit de cel recyclen, " zegt Pieter Cullis, een professor in biochemie en moleculaire biologie aan de Universiteit van British Columbia die geen deel uitmaakte van het onderzoeksteam. "Het is mogelijk dat deze benadering aanleiding zal geven tot de orde-van-grootte verbeteringen in potentie die nodig zijn voor op siRNA gebaseerde therapieën om meer in het algemeen effectieve middelen te zijn voor de behandeling van ziekten."
Dit verhaal is opnieuw gepubliceerd met dank aan MIT News (web.mit.edu/newsoffice/), een populaire site met nieuws over MIT-onderzoek, innovatie en onderwijs.
 Ontwikkeld materiaal dat tegelijkertijd warmte-isolerend en warmtegeleidend is
Ontwikkeld materiaal dat tegelijkertijd warmte-isolerend en warmtegeleidend is Een nieuwe benadering voor het versterken van DNA
Een nieuwe benadering voor het versterken van DNA Een nieuwe katalysator voor watersplitsing die het beste van twee werelden is
Een nieuwe katalysator voor watersplitsing die het beste van twee werelden is Video:De limoneenmythe
Video:De limoneenmythe Onderzoek met atoomsondetomografie onthult kieren in ijzerkristallen die kunnen genezen
Onderzoek met atoomsondetomografie onthult kieren in ijzerkristallen die kunnen genezen
 Toenemende trends van warme en natte extremen vertraagden in China tijdens de recente onderbreking van de opwarming van de aarde
Toenemende trends van warme en natte extremen vertraagden in China tijdens de recente onderbreking van de opwarming van de aarde Intensivering van Hurricane Lane onderzocht door GPM-satelliet
Intensivering van Hurricane Lane onderzocht door GPM-satelliet Hawaiian Airlines sluit zich aan bij internationaal onderzoek naar klimaatverandering
Hawaiian Airlines sluit zich aan bij internationaal onderzoek naar klimaatverandering Bodembiologisch onderzoek kan bijdragen aan een duurzamere toekomst
Bodembiologisch onderzoek kan bijdragen aan een duurzamere toekomst Hittegolf verbrak afgelopen week records in VS ergens anders
Hittegolf verbrak afgelopen week records in VS ergens anders
Hoofdlijnen
- Grootschalige aanpak onthult imperfecte actor in plantenbiotechnologie
- Centrosoom: definitie, structuur en functie (met diagram)
- Processen die ATP
- Genetische studie onderzoekt manieren om de productiviteit en malsheid van vlees te verhogen
- Wat is een prehistorische toolkit en hoe zou het de menselijke geschiedenis kunnen herschrijven?
- Wat is een markermolecuul?
- Hoe een zevende-graadsmodel van een dierencel te bouwen
- Roofzuchtige bacteriën die patrijspoorten maken en fresco's schilderen in schadelijke bacteriën
- Genomisch onderzoek onthult aanwijzingen voor het wilde verleden van druiven
- Grafeen kraakt het glascorrosieprobleem

- Onderzoek toont aan dat celverstoringssysteem medische toepassingen kan hebben

- Two-lock box levert kankertherapie

- Nanomachines gebruiken om de oorlog tegen diabetes te bestrijden

- Wetenschappers vinden voor het eerst symmetriebreking uit in een apparaat op nanoschaal dat het menselijk brein kan nabootsen

 Een functie plotten
Een functie plotten Het vinden van natuurkundigen kan een revolutie teweegbrengen in de informatieoverdracht
Het vinden van natuurkundigen kan een revolutie teweegbrengen in de informatieoverdracht Achtergrondinformatie over Egg Drop Experiments
Achtergrondinformatie over Egg Drop Experiments Wetenschappers laten zien hoe ze een katalysator kunnen beheersen die een broeikasgas in een brandstof of grondstof verandert
Wetenschappers laten zien hoe ze een katalysator kunnen beheersen die een broeikasgas in een brandstof of grondstof verandert Door de grenzen van het gezichtsvermogen te verleggen, kunnen verborgen werelden worden onthuld
Door de grenzen van het gezichtsvermogen te verleggen, kunnen verborgen werelden worden onthuld Nanolock detecteert kankermutatie; kan leiden tot een vroege diagnose, gepersonaliseerde therapieën
Nanolock detecteert kankermutatie; kan leiden tot een vroege diagnose, gepersonaliseerde therapieën Wereld rouwt om Britse wetenschapper en cultureel icoon Hawking
Wereld rouwt om Britse wetenschapper en cultureel icoon Hawking Ryanair keert zich tegen Polen, maar wordt geconfronteerd met grootste staking
Ryanair keert zich tegen Polen, maar wordt geconfronteerd met grootste staking
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Portuguese | Swedish | German | Dutch | Danish | Norway | Spanish |

-
Wetenschap © https://nl.scienceaq.com

