Wetenschap
Nickelblock:een haat-liefdeverhouding met batterij-elektroden
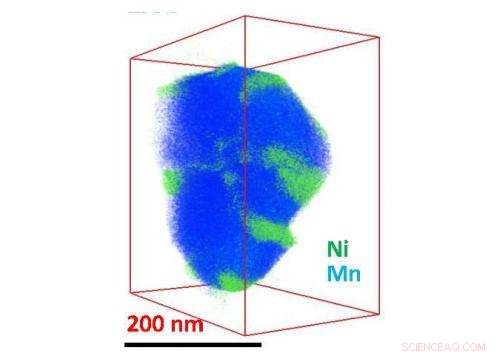
Terwijl mangaan (blauw) dit lithium-ion batterij nanodeeltje gelijkmatig vult, nikkel (groen) klontert in bepaalde regio's, interfereren met de soepele werking van het materiaal. Krediet:Chongmin Wang/PNNL
Iedereen die een elektronisch apparaat bezit, weet dat lithium-ionbatterijen beter zouden kunnen werken en langer mee zouden kunnen gaan. Nutsvoorzieningen, wetenschappers die batterijmaterialen op nanoschaal onderzoeken, onthullen hoe nikkel een fysieke barrière vormt die het pendelen van lithiumionen in de elektrode belemmert, verminderen hoe snel de materialen laden en ontladen. Vorige week gepubliceerd in Nano-letters , het onderzoek suggereert ook een manier om de materialen te verbeteren.
De onderzoekers, geleid door Chongmin Wang van het Pacific Northwest National Laboratory van het Department of Energy, 3D-beelden met hoge resolutie gemaakt van elektrodematerialen gemaakt van met lithium-nikkel-mangaanoxide gelaagde nanodeeltjes, het in kaart brengen van de afzonderlijke elementen. Deze kaarten lieten zien dat nikkel op bepaalde plekken in de nanodeeltjes klontjes vormde. Een hogere vergroting liet zien dat het nikkel de kanalen blokkeerde waardoor lithiumionen normaal gesproken reizen wanneer batterijen worden opgeladen en ontladen.
"We waren verrast om te zien dat het nikkel selectief segregeerde zoals het deed. Toen de bewegende lithiumionen de gescheiden nikkelrijke laag raakten, ze stuiten in wezen op een barrière die hen lijkt te vertragen, " zei Wang, een materiaalwetenschapper bij EMSL, het Environmental Molecular Sciences Laboratory, een DOE-gebruikersfaciliteit op de campus van PNNL. "Het blok vormt zich in het productieproces, en we willen graag een manier vinden om dit te voorkomen."
Lithiumionen zijn positief geladen atomen die tussen de negatieve en positieve elektroden bewegen wanneer een batterij wordt opgeladen of in gebruik is. Ze vangen of laten in wezen de negatief geladen elektronen los, wiens beweging door een apparaat zoals een laptop de elektrische stroom vormt.
In lithium-mangaanoxide-elektroden, de mangaan- en zuurstofatomen vormen rijen als een veld van maïsstengels. In de kanalen tussen de stengels, lithiumionen ritsen naar de elektroden aan beide uiteinden, de richting, afhankelijk van of de batterij wordt gebruikt of wordt opgeladen.
Onderzoekers weten al lang dat het toevoegen van nikkel de hoeveelheid energie die de elektrode kan vasthouden verbetert. batterijkwaliteiten bekend als capaciteit en spanning. Maar wetenschappers hebben niet begrepen waarom de capaciteit daalt na herhaald gebruik - een situatie die consumenten ervaren wanneer een stervende batterij zijn lading steeds minder lang vasthoudt.
Er achter komen, Wang, materiaalwetenschapper Meng Gu en hun medewerkers gebruikten elektronenmicroscopie bij EMSL en het National Center for Electron Microscopy in het Lawrence Berkeley National Laboratory om te zien hoe de verschillende atomen zijn gerangschikt in de elektrodematerialen geproduceerd door onderzoekers van Argonne National Laboratory. De elektroden waren gebaseerd op nanodeeltjes gemaakt met lithium, nikkel, en mangaanoxiden.
Eerst, het team nam afbeeldingen met een hoge resolutie die duidelijk rijen atomen lieten zien, gescheiden door kanalen gevuld met lithiumionen. Op het oppervlak, ze zagen de opeenhoping van nikkel aan de uiteinden van de rijen, in wezen blokkeren van lithium in en uit bewegen.
Om erachter te komen hoe de oppervlaktelaag is verdeeld over en binnen het hele nanodeeltje, het team gebruikte een techniek die driedimensionale compositietoewijzing wordt genoemd. Met behulp van een nanodeeltje van ongeveer 200 nanometer groot, ze namen 50 foto's van de afzonderlijke elementen terwijl ze het nanodeeltje onder verschillende hoeken kantelden. Het team reconstrueerde een driedimensionale kaart van de individuele elementaire kaarten, onthullende vlekken van nikkel op een achtergrond van lithium-mangaanoxide.
De driedimensionale verdeling van mangaan, zuurstof- en lithiumatomen langs het oppervlak en in het deeltje waren relatief gelijk. het nikkel, echter, parkeerde zichzelf in kleine gebieden op het oppervlak. intern, het nikkel klonterde aan de randen van kleinere regio's die korrels worden genoemd.
Om te onderzoeken waarom nikkel aggregeert op bepaalde oppervlakken, het team berekende hoe gemakkelijk nikkel en lithium door de kanalen reisden. Nikkel bewoog gemakkelijker op en neer door de kanalen dan lithium. Terwijl nikkel zich normaal gesproken in de mangaanoxide-cornrows bevindt, soms glijdt het uit in de kanalen. En wanneer het gebeurt, deze analyse toonde aan dat het veel gemakkelijker door de kanalen naar het einde van het veld stroomt, waar het zich ophoopt en een blok vormt.
De onderzoekers gebruikten verschillende methoden om de nanodeeltjes te maken. Wang zei dat hoe langer de nanodeeltjes tijdens de fabricage op hoge temperatuur bleven, des te meer nikkel scheidde en des te slechter de deeltjes presteerden bij laad- en ontlaadtests. Ze zijn van plan om nauwkeuriger gecontroleerde experimenten te doen om te bepalen of een bepaalde productiemethode een betere elektrode oplevert.
Dit werk werd ondersteund door het Chemical Imaging Initiative van PNNL.
 Wetenschappers ontwikkelen een cellulose-biosensormateriaal voor geavanceerde weefseltechnologie
Wetenschappers ontwikkelen een cellulose-biosensormateriaal voor geavanceerde weefseltechnologie Waterstof voedt raketten, maar hoe zit het met stroom voor het dagelijks leven? kwamen dichterbij
Waterstof voedt raketten, maar hoe zit het met stroom voor het dagelijks leven? kwamen dichterbij Hoe maak je een citroenzuurbufferoplossing
Hoe maak je een citroenzuurbufferoplossing Betere oplossingen voor het maken van waterstof liggen misschien net aan de oppervlakte
Betere oplossingen voor het maken van waterstof liggen misschien net aan de oppervlakte Hoe een badspons een biobased industrieel filter wordt
Hoe een badspons een biobased industrieel filter wordt
 Wat psychotherapie kan doen voor de klimaat- en biodiversiteitscrises?
Wat psychotherapie kan doen voor de klimaat- en biodiversiteitscrises? Kleine stroompjes in agrarische ecosystemen zijn zwaar vervuild met pesticiden
Kleine stroompjes in agrarische ecosystemen zijn zwaar vervuild met pesticiden Volgens de weersvoorspelling zou het 90 graden zijn. Dus waarom zegt je thermometer dat het 100 is?
Volgens de weersvoorspelling zou het 90 graden zijn. Dus waarom zegt je thermometer dat het 100 is? Efficiënte gebouwen kunnen elk jaar duizenden levens redden in de VS
Efficiënte gebouwen kunnen elk jaar duizenden levens redden in de VS Habitats van pijnbomen
Habitats van pijnbomen
Hoofdlijnen
- Chloroplast & Mitochondria: wat zijn de overeenkomsten en verschillen?
- Hypermutators zorgen ervoor dat pathogene schimmels sneller evolueren
- Profase: wat gebeurt er in dit stadium van mitose en meiose?
- Nieuwe gorilla in Audubon Zoo mag nog even binnen blijven
- Zijn linkshandigen beter in sport?
- Science Fair-projecten op handversmettingsmiddelen of vloeibare zeep voor het doden van bacteriën
- Griezelige bescherming:bedreigde diersoorten redden boven onze dode lichamen
- Wel of niet fokken? Trekkende vrouwelijke vlinders staan voor een moessondilemma
- Wat zijn de twee hoofdfasen van celdeling?
 Onderzoekers ontwikkelen de eerste in zijn soort, eenvoudige test voor het identificeren van giftige zilverionen
Onderzoekers ontwikkelen de eerste in zijn soort, eenvoudige test voor het identificeren van giftige zilverionen Techniek voorkomt fouten in kwantumcomputers
Techniek voorkomt fouten in kwantumcomputers AQM+:een nieuw model voor het genereren van visuele dialoogvragen
AQM+:een nieuw model voor het genereren van visuele dialoogvragen Apple-gegevens tonen dramatische impact van virus op beweging
Apple-gegevens tonen dramatische impact van virus op beweging Sneeuwvrij seizoen Alaska North Slope wordt langer
Sneeuwvrij seizoen Alaska North Slope wordt langer Socioloog legt uit hoe, waarom privilege een rol speelt in strafrechtbanken
Socioloog legt uit hoe, waarom privilege een rol speelt in strafrechtbanken Onderzoekers ontwikkelen methode voor inkjetprinten met hooggeleidende, buigbare lagen grafeen
Onderzoekers ontwikkelen methode voor inkjetprinten met hooggeleidende, buigbare lagen grafeen Ultrasnelle röntgenstraling geeft een nieuwe kijk op de afbraak van plasmaontladingen in water
Ultrasnelle röntgenstraling geeft een nieuwe kijk op de afbraak van plasmaontladingen in water
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com