
Wetenschap
De wet van behoud van massa begrijpen:gebalanceerde chemische vergelijkingen
Zo identificeert u een vergelijking die aan deze wet voldoet:
Zoek naar evenwichtige chemische vergelijkingen:
Een uitgebalanceerde chemische vergelijking heeft hetzelfde aantal atomen van elk element aan zowel de reactant- als de productzijde. Dit zorgt ervoor dat er tijdens de reactie geen atomen worden gecreëerd of vernietigd, wat voldoet aan het principe van behoud van massa.
Voorbeeld:
De verbranding van methaan:
* Onevenwichtig: CH₄ + O₂ → CO₂ + H₂O
* Evenwichtig: CH₄ + 2O₂ → CO₂ + 2H₂O
In de evenwichtige vergelijking hebben we:
* 1 koolstofatoom aan beide zijden
* 4 waterstofatomen aan beide zijden
* 4 zuurstofatomen aan beide zijden
Dit toont aan dat de massa van de reactanten (methaan en zuurstof) gelijk is aan de massa van de producten (kooldioxide en water).
Belangrijke opmerking: De wet van behoud van massa is alleen van toepassing op gesloten systemen, waar geen enkele materie naar binnen of naar buiten kan gaan. In open systemen kan massa verloren of gewonnen worden als gevolg van factoren zoals verdamping of verbranding.
Hoofdlijnen
- Welk fysiek kenmerk heeft de plantachtige Noctiluca en Animalle -Trypanosoma Gambienese gemeen?
- We kunnen allemaal stoppen met het misbruiken van deze psychologische termen
- Waar is wetenschappelijk denken op gebaseerd?
- Cilia en flagella zijn gemaakt van eiwitfilamenten genoemd?
- Hebben garnalen een zenuwstelsel?
- Wat zou een goede hypothese -verklaring zijn voor hoe dierlijke cellen verschillen van plantencellen?
- Hoe elektroconvulsietherapie werkt
- Overbevissing:Is er echt veel vis in de zee?
- Grote eiwitten kunnen uit de cel worden uitgescheiden met behulp van het proces van?
- Elektro-mechano-optische NMR-detectie

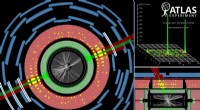
- Van supersymmetrie naar het standaardmodel:nieuwe resultaten van het ATLAS-experiment
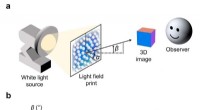
- 3D-printen op nanoschaal gebruiken om lichtveldafdrukken met hoge resolutie te maken
- Experiment maakt snapshots van licht, stopt licht, gebruikt licht om eigenschappen van materie te veranderen

- De voortgang van fusie-energie volgen door 60 jaar neutrale deeltjesanalyse

 Welke ster is grotere zon of betelgeuse?
Welke ster is grotere zon of betelgeuse?  Facebooks toenemende crisis over gebruikersgegevens
Facebooks toenemende crisis over gebruikersgegevens Waarom gammastraling uitgestoten in kern?
Waarom gammastraling uitgestoten in kern?  Wat zijn de belangrijkste lichamen van in het zonnestelsel?
Wat zijn de belangrijkste lichamen van in het zonnestelsel?  Hoe het luchtschip van CargoLifter zal werken
Hoe het luchtschip van CargoLifter zal werken  Wat is het molecuulgewicht van één mol H2CO3?
Wat is het molecuulgewicht van één mol H2CO3?  Wat is een gefossiliseerd merkteken dat gevormd is in zacht sediment door de beweging van een dier?
Wat is een gefossiliseerd merkteken dat gevormd is in zacht sediment door de beweging van een dier?  Wat heeft Ernest Rutherford geleerd van zijn experiment met goudfolie?
Wat heeft Ernest Rutherford geleerd van zijn experiment met goudfolie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


