
Wetenschap
Waarom is de beweging van een gasdeeltje onafhankelijk ander deeltje?
Waarom het onafhankelijk lijkt:
* Lage dichtheid: Gasdeeltjes liggen ver uit elkaar in vergelijking met hun grootte. Dit betekent dat botsingen tussen deeltjes relatief zeldzaam zijn.
* Kortlevende botsingen: Wanneer botsingen plaatsvinden, zijn ze kort en veranderen ze het algehele traject van de deeltjes niet significant.
* willekeurige beweging: Gasdeeltjes bewegen willekeurig in alle richtingen met een breed scala aan snelheden. Dit maakt het moeilijk om het exacte pad van elk individueel deeltje te voorspellen.
Waarom het niet helemaal onafhankelijk is:
* botsingen komen voor: Hoewel zeldzaam, gebeuren botsingen tussen deeltjes en beïnvloeden hun beweging. Deze botsingen brengen momentum en energie over en beïnvloeden de snelheid en richting van de botsende deeltjes.
* intermoleculaire krachten: Hoewel er zwakke, aantrekkelijke krachten bestaan tussen gasmoleculen, vooral bij hogere druk. Deze krachten kunnen deeltjesbeweging beïnvloeden, vooral bij lage temperaturen.
* Collectief gedrag: Het gedrag van veel gasdeeltjes samen creëert macroscopische eigenschappen zoals druk en temperatuur. Deze eigenschappen worden beïnvloed door de collectieve interacties van deeltjes, wat aangeeft dat hun beweging niet helemaal onafhankelijk is.
Het ideale gasmodel:
De ideale gaswet is een vereenvoudigd model dat veronderstelt dat gasdeeltjes puntmassa's zijn zonder volume en geen intermoleculaire krachten. Dit zorgt voor een eenvoudigere analyse van gasgedrag, uitgaande van perfect onafhankelijke deeltjesbeweging. Het is echter belangrijk om te onthouden dat het ideale gasmodel een vereenvoudiging is en niet perfect de ware aard van gasdeeltjes weerspiegelt.
Samenvattend:
Hoewel de beweging van een gasdeeltje onafhankelijk lijkt vanwege lage dichtheid en zeldzame botsingen, is de realiteit dat gasdeeltjes met elkaar interageren, zelfs als deze interacties kort en zeldzaam zijn. Deze interacties, samen met intermoleculaire krachten, maken de beweging van gasdeeltjes niet volledig onafhankelijk.
 Wanneer koolstof en zuurstof combineren, wat vormen ze dan?
Wanneer koolstof en zuurstof combineren, wat vormen ze dan?  Nieuwe technologie zet zonlicht, water en koolstofdioxide om in acetaat en zuurstof voor hoogwaardige brandstoffen en chemicaliën
Nieuwe technologie zet zonlicht, water en koolstofdioxide om in acetaat en zuurstof voor hoogwaardige brandstoffen en chemicaliën Hoeveel moleculen aceton zijn aanwezig in 0,435 g aceton?
Hoeveel moleculen aceton zijn aanwezig in 0,435 g aceton?  Een betere beoordeling van de gevoeligheid van bacteriën voor antibiotica kan de manier waarop medicijnen worden voorgeschreven veranderen
Een betere beoordeling van de gevoeligheid van bacteriën voor antibiotica kan de manier waarop medicijnen worden voorgeschreven veranderen Welk element komt voor als geel poeder?
Welk element komt voor als geel poeder?
 Welke continenten hebben gematigde naaldbouten?
Welke continenten hebben gematigde naaldbouten?  Winterstormen teisteren grote delen van de VS
Winterstormen teisteren grote delen van de VS Nieuwe bloedtest onthult vatbaarheid voor kostbare ziekten bij melkkoeien
Nieuwe bloedtest onthult vatbaarheid voor kostbare ziekten bij melkkoeien NASA krijgt een diepgaande kijk op de intensivering van de orkaan Harvey
NASA krijgt een diepgaande kijk op de intensivering van de orkaan Harvey Moet Ierland zijn elektriciteitscentrales van brandstof voorzien met hout dat uit Australië wordt verscheept?
Moet Ierland zijn elektriciteitscentrales van brandstof voorzien met hout dat uit Australië wordt verscheept?
Hoofdlijnen
- Erasmus Darwin -bijdrage op het gebied van biologie?
- Hoe zijn chromosomen geëvolueerd?
- Hoe dopamine helpt om sommige voedingsmiddelen verslavend te maken
- Een dicht gebied in een cel die nucleïnezuren bevat, is?
- In welk type levend organisme vindt ademhaling plaats?
- Onderzoekers observeren hoe de flexibiliteit van een eiwitscharnier cruciaal is voor de overdracht van celeiwitten
- Wat is de medische toepassing van acidose?
- Waarom gaan bacteriën naar de bodem van de bouilloncultuur?
- Waarom is het begrijpen van biogeochemische cycli belangrijk voor de milieuwetenschap?
- Onderzoekers ontwikkelen platte lens die duizend keer dunner is dan een mensenhaar

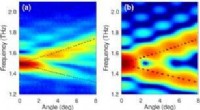
- Onderzoekers onderzoeken hoe terahertz-golven interageren met lenzen met schot in de roos
- Onderzoek onthult exotische kwantumtoestanden in dubbellaags grafeen
- Experimenten bij de temperatuur van de zon bieden oplossingen voor problemen met zonnemodellen

- Handgeschreven Einstein-biljet geveild in Jeruzalem

 Face-to-face astronomieconferentie draagt bij 3, 000 keer meer koolstofdioxide dan online conferentie
Face-to-face astronomieconferentie draagt bij 3, 000 keer meer koolstofdioxide dan online conferentie Waar bevindt zich de extreem hete laag die mantel wordt genoemd?
Waar bevindt zich de extreem hete laag die mantel wordt genoemd?  Welke richting werkt de zwaartekracht van de aarde?
Welke richting werkt de zwaartekracht van de aarde?  Is het correct om te zeggen wat een prachtig klimaat?
Is het correct om te zeggen wat een prachtig klimaat?  Hoe kun je een versnelling verdubbelen zonder de massa te veranderen?
Hoe kun je een versnelling verdubbelen zonder de massa te veranderen?  Actieve werkplekken op kantoor
Actieve werkplekken op kantoor Nostalgie beschermt tegen negatieve gevoelens
Nostalgie beschermt tegen negatieve gevoelens Is een ecosysteem groter of kleiner dan een bioom?
Is een ecosysteem groter of kleiner dan een bioom?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

