
Wetenschap
Wat is de definitie voor kwantummechanisch model?
Key Concepts:
* elektronen zijn niet beperkt tot banen: In plaats daarvan bestaan ze in regio's van de ruimte genaamd orbitalen , die worden gedefinieerd door hun vorm, grootte en energieniveau.
* orbitalen zijn probabilistisch: Het kwantummechanische model beschrijft de kans om een elektron op een specifiek punt in de ruimte te vinden. Dit wordt weergegeven door de elektronendichtheid , die hoger is in gebieden waar het elektron waarschijnlijker wordt gevonden.
* elektronen hebben dualiteit van golfdeeltjes: Elektronen vertonen zowel golfachtige als deeltjesachtige eigenschappen. Dit concept wordt vastgelegd in de Schrödinger -vergelijking , die het gedrag van elektronen in atomen beschrijft.
* Atomische orbitalen hebben specifieke vormen: Verschillende orbitalen hebben verschillende vormen, zoals bolvormige (s-orbitalen), haltervormig (p-orbitalen) en meer complexe vormen (D en F orbitalen). Deze vormen weerspiegelen de waarschijnlijkheidsverdeling van het elektron binnen het orbitaal.
* Gekwantiseerde energieniveaus: Elektronen kunnen alleen specifieke energieniveaus in een atoom bezetten. Deze energieniveaus zijn gekwantiseerd, wat betekent dat ze alleen kunnen bestaan op discrete waarden.
Samenvattend:
Het kwantummechanische model biedt een meer accurate en verfijnde beschrijving van het atoom in vergelijking met het Bohr -model. Het benadrukt de probabilistische aard van elektronengedrag en de golfachtige eigenschappen van elektronen, wat leidt tot een beter begrip van chemische binding en de reactiviteit van atomen.
 Wie schreef staat nog steeds open voor discussie of psychologie een natuurwetenschap is of het kan als überhaupt worden beschouwd?
Wie schreef staat nog steeds open voor discussie of psychologie een natuurwetenschap is of het kan als überhaupt worden beschouwd?  Wat is de Tree Equity-score van uw stad?
Wat is de Tree Equity-score van uw stad?  Typen door de mens veroorzaakte verontreinigende stoffen
Typen door de mens veroorzaakte verontreinigende stoffen  Sneeuw heeft mogelijk een aantal bloemen vertraagd voor de eerste dag van de lente
Sneeuw heeft mogelijk een aantal bloemen vertraagd voor de eerste dag van de lente Verschillende hydraulische systemen
Verschillende hydraulische systemen
Hoofdlijnen
- Wat kunnen wetenschappers leren van wormen die gloeien in het donker? De geheimen van regeneratie om te beginnen
- Wat is het verschil in levenswetenschappen en fysieke wetenschappen?
- Tot ziens 'Zweinstein dinosaurus'? Nieuwe analyses van de groei van dinosauriërs kunnen een derde van de soorten uitroeien
- Wat maakt een uitleg goed genoeg?
- Wie heeft zelfstandige naamwoorden uitgevonden?
- Welk type chromosomen vind je in fruitvliegjes?
- Wat is de gelijkenis tussen slijmlaag en capsulebacteriën?
- Welke verdeling brengt impulsen over van het centrale zenuwstelsel naar spieren of klieren?
- Is de celmeembraan in staat chemische signalen te ontvangen en te herkennen?
- Door licht geïnduceerde verdraaiing van Weyl-knooppunten schakelt gigantische elektronenstroom in

- Kwantummechanica zou kunnen verklaren waarom DNA spontaan kan muteren
- Nucleaire magische getallen vallen voorbij het dubbel magische nikkel 78

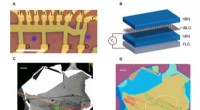
- Intrinsiek gekwantiseerd abnormaal Hall-effect in een moiré heterostructuur
- Lasergebaseerd systeem detecteert branden zelfs in stoffige, ruwe omgevingen

 Hebben enzymen in de dunne darm een zure omgevingsvolgorde nodig om te werken?
Hebben enzymen in de dunne darm een zure omgevingsvolgorde nodig om te werken?  In welke plaats zou je de minste organismen vinden?
In welke plaats zou je de minste organismen vinden?  Ruimtetoerisme zou wetenschappelijk en gezondheidsonderzoek een boost kunnen geven - hier hoe?
Ruimtetoerisme zou wetenschappelijk en gezondheidsonderzoek een boost kunnen geven - hier hoe? Wat doen micro -organismen die ervoor zorgen dat voedsel nodig is?
Wat doen micro -organismen die ervoor zorgen dat voedsel nodig is?  Kenmerken van een bosecosysteem
Kenmerken van een bosecosysteem Ryanairs Nederlands cabinepersoneel stak dinsdag
Ryanairs Nederlands cabinepersoneel stak dinsdag De overschrijdingskans berekenen
De overschrijdingskans berekenen Kabelbedrijf Altice USA schept streaming nieuwssite Cheddar . op
Kabelbedrijf Altice USA schept streaming nieuwssite Cheddar . op
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

