
Wetenschap
Welke intermoleculaire kracht is het zwakst?
Dit is waarom:
* ldfs zijn tijdelijke, zwakke attracties die voortvloeien uit de momentane fluctuaties in elektronenverdeling in moleculen. Ze zijn aanwezig in alle moleculen, maar zijn de enige kracht die aanwezig is in niet -polaire moleculen.
* dipole-dipole krachten zijn sterker dan LDF's omdat ze permanente dipolen in polaire moleculen met zich meebrengen, wat leidt tot een meer consistente aantrekkingskracht.
* Waterstofbindingen zijn het sterkste type intermoleculaire kracht, dat optreedt wanneer een waterstofatoom wordt gebonden aan een sterk elektronegatief atoom zoals zuurstof, stikstof of fluor. Dit creëert een zeer sterke dipool en aantrekkingskracht tussen moleculen.
Samenvattend neemt de sterkte van intermoleculaire krachten in het algemeen toe in deze volgorde:
London dispersie-krachten
 Om de toekomst van orkanen te begrijpen, kijk naar het verleden
Om de toekomst van orkanen te begrijpen, kijk naar het verleden Wat is het doel in een wetenschapsproject?
Wat is het doel in een wetenschapsproject?  Hoe het in kaart brengen van de Galápagos duurzamere steden kan creëren
Hoe het in kaart brengen van de Galápagos duurzamere steden kan creëren The Greenhouse Effect & Photosynthesis
The Greenhouse Effect & Photosynthesis  Nabijheid van land bepaalt hoe koraalrifgemeenschappen reageren op klimaatveranderingen
Nabijheid van land bepaalt hoe koraalrifgemeenschappen reageren op klimaatveranderingen
Hoofdlijnen
- Waarom moet een cel polymeren afbreken in monomeren?
- Kan iemand een kort verhaal schrijven met behulp van de woorden mitochondria cytoplasma chloroplast en chlorofyl nucleolus kernweefsel organen vacuole chromosoom?
- Wat zijn de 6 stappen van transcriptie?
- Welke organel absorbeert koolstofdioxide in planten?
- Wat is de juiste volgorde voor de volgorde van de meiose?
- Hoe heet een groep wormen?
- Hoe origami ziektediagnoses kan bepalen
- Een dierencel maken voor een wetenschapsproject
- Voor het eerst hebben wetenschappers levende bacteriën rechtstreeks waargenomen in poolijs en sneeuw
- Diamantspiegels voor krachtige lasers

- Met een nieuwe holografische microscoop kunnen wetenschappers door de schedel kijken en het muizenbrein in beeld brengen

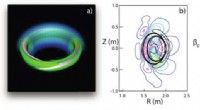
- Kleine instabiliteiten in tokamaks elimineren voordat ze verstoringen worden
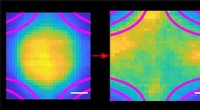
- Wetenschappers verbeteren de nauwkeurigheid van de directionele polarimetrische camera verder

- Het koudste plasma ter wereld bottelen
 Heeft een uitgerekt elastiekje potentiële energie?
Heeft een uitgerekt elastiekje potentiële energie?  Microsoft biedt softwaretools om verkiezingen te beveiligen
Microsoft biedt softwaretools om verkiezingen te beveiligen Onderzoekers ontwikkelen een toonaangevende microgolffotonica-chip voor snelle signaalverwerking
Onderzoekers ontwikkelen een toonaangevende microgolffotonica-chip voor snelle signaalverwerking  Lasermethode veelbelovend voor detectie van sporenchemicaliën in lucht
Lasermethode veelbelovend voor detectie van sporenchemicaliën in lucht Online technologie verandert de dynamiek van het geven van geschenken
Online technologie verandert de dynamiek van het geven van geschenken Doel raken in kankerbestrijding nu gemakkelijker met nieuw platform voor nanodeeltjes
Doel raken in kankerbestrijding nu gemakkelijker met nieuw platform voor nanodeeltjes Continentale controles nodig om de strijd tegen boomziekten te handhaven
Continentale controles nodig om de strijd tegen boomziekten te handhaven Race over de toendra - witte spar versus sneeuwhaas
Race over de toendra - witte spar versus sneeuwhaas
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

