
Wetenschap
Stampede2, Bridges-simulaties tonen zwakke plekken in het nucleocapside van het Ebola-virus
De resultaten van de studie, gepubliceerd in het tijdschrift Structure, laten zien hoe dit specifieke eiwit van vorm verandert naarmate het virus een cel infecteert en mogelijke doelwitten voor potentiële therapieën identificeren.
“Het nucleocapside-eiwit van het Ebola-virus speelt een belangrijke rol in het virusreplicatieproces”, zegt onderzoeksleider Rumela Chakrabarti, bio-ingenieur en universitair hoofddocent aan de UC San Diego Jacobs School of Engineering en Skaggs School of Pharmacy and Pharmaceutical Sciences. “Dit eiwit kapselt het genetisch materiaal van het virus in. Het is als noppenfolie voor het virus-RNA, dat het beschermt tegen schade en tegen de immuunreactie van de cel. Hoe meer we begrijpen over de structuur van dit eiwit en hoe het functioneert, hoe groter de kans dat we nieuwe manieren vinden om het virus te behandelen.”
Chakrabarti en haar team kozen ervoor om het Ebola-nucleocapside-eiwit te onderzoeken met behulp van gespecialiseerde simulaties die 'enhanced sampling' moleculaire dynamica worden genoemd. Deze computationele benadering stelt wetenschappers in staat de bewegingen van individuele atomen in het eiwit te simuleren, waardoor wordt onthuld hoe het eiwit in de loop van de tijd verandert en zwakke punten in de eiwitstructuur worden blootgelegd.
Het team voerde deze uitgebreide computersimulaties uit op Stampede2. De onderzoekers zeggen dat ze de kracht en schaalbaarheid van Stampede2 nodig hadden om duizenden simulaties uit te voeren, die elk enkele dagen in beslag namen.
“Met het Stampede2-systeem konden we grote conformationele veranderingen van de eiwitstructuur simuleren, wat inzicht geeft in hoe het zich zou kunnen gedragen in een geïnfecteerde cel”, zegt Chakrabarti.
De simulaties onthulden verschillende mogelijke doelwitten voor potentiële nieuwe therapieën, waaronder de flexibele delen van het eiwit die het meest veranderen tijdens infectie. Deze gebieden kunnen het doelwit zijn van kleine moleculen of antilichamen, waardoor ze hun functie niet kunnen uitoefenen en uiteindelijk de gastheercel tegen infectie kunnen worden beschermd.
“Onze volgende stappen zullen zijn het ontwerpen van specifieke medicijnen of medicijnachtige moleculen die zich aan deze holtes kunnen binden om de virale replicatie en infectiviteit te verminderen”, zegt Chakrabarti.
Dit onderzoek werd gedeeltelijk ondersteund door de National Institutes of Health en het ministerie van Defensie. Er werden berekeningen uitgevoerd op het Stampede2-systeem bij de TACC.
 Hoe de zuurgraad van fruitsoorten te meten
Hoe de zuurgraad van fruitsoorten te meten Wetenschappers ontwerpen nieuw responsief poreus materiaal geïnspireerd op eiwitten
Wetenschappers ontwerpen nieuw responsief poreus materiaal geïnspireerd op eiwitten Video:Waarom werkt onkruidverdelger niet meer?
Video:Waarom werkt onkruidverdelger niet meer? De kosten van ethanol verlagen, andere biobrandstoffen en benzine
De kosten van ethanol verlagen, andere biobrandstoffen en benzine Onderzoek onthult waarom het moeilijk is om de geur uit polyester te krijgen
Onderzoek onthult waarom het moeilijk is om de geur uit polyester te krijgen
 De omvang van de grote aardbeving in Lissabon was mogelijk lager dan eerdere schattingen
De omvang van de grote aardbeving in Lissabon was mogelijk lager dan eerdere schattingen Lava crasht door dak van rondvaartboot Hawaï geblesseerd 23 (update)
Lava crasht door dak van rondvaartboot Hawaï geblesseerd 23 (update) Wetenschappers analyseren hoe de pandemie de luchtkwaliteit beïnvloedde
Wetenschappers analyseren hoe de pandemie de luchtkwaliteit beïnvloedde Hoe het behoud van het leefgebied voor migrerende kraanvogels te verbeteren
Hoe het behoud van het leefgebied voor migrerende kraanvogels te verbeteren  Biochar kan op maat worden gemaakt voor een reeks milieuvoordelen, uit onderzoek blijkt
Biochar kan op maat worden gemaakt voor een reeks milieuvoordelen, uit onderzoek blijkt
Hoofdlijnen
- Hoe één soort uiteindelijk de dominante partner kan worden in een mutualistische relatie
- Suiker in babyvoeding:waarom Nestlé rekening moet houden Afrika
- Wat zijn de biomoleculen van ribosomen?
- Terwijl de vogelgriep zich verspreidt naar melkkoeien, vertonen de roofvogels uit Minnesota tekenen dat ze een opmerkelijke immuniteit opbouwen
- Hoe de hoektanden van vleesetende zoogdieren zich ontwikkelden tot supermoordenaars
- Wat hebben we geleerd van het Human Genome Project?
- Wetenschappers onthullen hoe een weinig bekende amoebe een bacterie overspoelde om fotosynthetisch te worden
- Sinds de beursintroductie heeft Snap Inc. precies gedaan wat het beloofde, dus waarom hebben aandelen het moeilijk?
- Handelen of niet handelen? De ivoren impasse doorbreken
- Kwantumsystemen:hetzelfde, maar anders

- Minder risico, minder kosten:draagbare spectroscopie-apparaten kunnen binnenkort echt worden
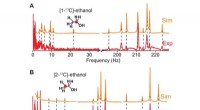
- Zoeken naar geluidsgolven in de superfluïde volgordeparameter

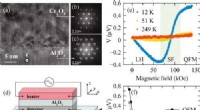
- Antferromagnetische hybriden bereiken belangrijke functionaliteit voor spintronische toepassingen
- Kwantummechanica loopt warm in een koud plasma:onderzoek

 Metalenen kunnen de vacuüm UV-markt verstoren
Metalenen kunnen de vacuüm UV-markt verstoren Waarom een aanstaande afspraak ons minder productief maakt
Waarom een aanstaande afspraak ons minder productief maakt Elektrisch geladen stofstormen stimuleren de chloorcyclus van Mars
Elektrisch geladen stofstormen stimuleren de chloorcyclus van Mars Inmenging in buitenlandse verkiezingen richt zich op het cultiveren van wantrouwen, consensus verminderen
Inmenging in buitenlandse verkiezingen richt zich op het cultiveren van wantrouwen, consensus verminderen Geboorte van een storm in de Arabische Zee valideert klimaatmodel
Geboorte van een storm in de Arabische Zee valideert klimaatmodel Intracellulaire opnames met behulp van nanotoren-elektroden
Intracellulaire opnames met behulp van nanotoren-elektroden Onderzoekers ontdekken dat elektronenchiraliteit in grafeen de stroomstroom beïnvloedt
Onderzoekers ontdekken dat elektronenchiraliteit in grafeen de stroomstroom beïnvloedt Bereiding van anti-tumor nanodeeltjes met behulp van tijgermelkpaddestoel
Bereiding van anti-tumor nanodeeltjes met behulp van tijgermelkpaddestoel
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

