
Wetenschap
Wat is roest?

U kent waarschijnlijk wel de schade die roest kan aanrichten aan een auto in de winter, of aan een fiets die buiten in de regen staat. Maar wat is roest , echt waar?
Inhoud
- Wat is roest?
- Hoe roest ontstaat
- Roestpreventie
Wat is roest?
Roest is de algemene naam voor een veel voorkomende verbinding:ijzeroxide. IJzeroxide, de chemische stof Fe2 O3 , komt vaak voor omdat ijzer zich heel gemakkelijk met zuurstof verbindt – zo gemakkelijk zelfs dat puur ijzer zelden in de natuur voorkomt.
Roest van ijzer (of staal) is een voorbeeld van corrosie:een elektrochemisch proces waarbij een anode (een stuk metaal dat gemakkelijk elektronen afgeeft), een elektrolyt (een vloeistof die elektronen helpt bewegen) en een kathode (een stuk metaal dat gemakkelijk elektronen afgeeft) betrokken zijn. accepteert elektronen).
Wanneer een stuk metaal corrodeert, helpt de elektrolyt de anode van zuurstof te voorzien. Terwijl zuurstof zich met het metaal verbindt, komen er elektronen vrij. Wanneer ze door de elektrolyt naar de kathode stromen, verdwijnt het metaal van de anode, weggevaagd door de elektrische stroom of omgezet in metaalkationen in een vorm zoals roest.
Hoe roest ontstaat
Om ijzer ijzeroxide te laten worden, zijn drie dingen nodig:ijzer, water en zuurstof. Dit is wat er gebeurt als de drie samenkomen:
Wanneer een druppel water een ijzeren voorwerp raakt, gebeuren er vrijwel onmiddellijk twee dingen. Ten eerste combineert het water, een goede elektrolyt, met kooldioxide in de lucht een zwak koolzuur, een nog betere elektrolyt.
Terwijl het zuur ontstaat en het ijzer oplost, zal een deel van het water uiteenvallen in zijn samenstellende delen:waterstof en zuurstof. De vrije zuurstof en het opgeloste ijzer binden zich tot ijzeroxide, waarbij elektronen vrijkomen. De elektronen die vrijkomen uit het anodegedeelte van het ijzer stromen naar de kathode, die een stuk metaal kan zijn dat minder elektrisch reactief is dan ijzer, of een ander punt op het stuk ijzer zelf.
De chemische verbindingen die worden aangetroffen in vloeistoffen zoals zure regen, zeewater en het met zout beladen opspattend water van sneeuwgordelwegen maken ze tot betere elektrolyten dan zuiver water, waardoor hun aanwezigheid het proces van roest op ijzer en andere vormen van corrosie op andere metalen kan versnellen.
Roestpreventie
IJzer reageert met zuurstof en water waardoor roest ontstaat. De eenvoudigste manier om het roestproces te voorkomen is dus door het oppervlak van ijzer en ijzerlegeringen uit de buurt van vocht te houden.
Als u uw auto bijvoorbeeld in een droge garage bewaart, uit de buurt van neerslag en temperatuurschommelingen (die het oxidatieproces kunnen versnellen), wordt de levensduur ervan verlengd.
Kathodische bescherming
Maar wat gebeurt er als je het metalen voorwerp niet zomaar naar binnen kunt verplaatsen? Kathodische bescherming (CP) is de methode die wordt gebruikt om alles te beschermen, van pijpleidingen tot boilers en schepen.
CP is afhankelijk van de elektrochemische reactie van elektrolyse. Wanneer twee metalen in contact komen met water, zal het meest elektropositieve van de twee metalen zijn elektronen opgeven en corroderen. In CP wordt ijzer gecombineerd met een ander, meer elektropositief metaal, zoals zink. Zink is een veel voorkomende "opofferingsanode" omdat het eerder zal oxideren dan ijzer.
Volgens de American Galvanizers Association kunnen zinkcoatings het roesten met 10 tot 100 procent vertragen.
Dat is willekeurigIJzeroxide deelt een naam met de programmeertaal Rust. In tegenstelling tot veel andere programmeertalen biedt Rust-taal ontwikkelaars de mogelijkheid om handmatig geheugenbeheer uit te voeren, terwijl het een leencontrole en sterke geheugenveiligheidsgaranties biedt. Rust-code is in de eerste plaats een programmeertaal voor systemen, die wordt gebruikt op plaatsen waar prestaties en betrouwbaarheid van cruciaal belang zijn, zoals bij besturingssystemen, game-engines en ingebedde systemen.
Dit artikel is bijgewerkt in combinatie met AI-technologie, vervolgens op feiten gecontroleerd en bewerkt door een HowStuffWorks-editor.
Veel beantwoorde vragen
Waarom is Rust beter dan C++?
Rust is een programmeertaal voor systemen die razendsnel werkt, segfaults voorkomt en threadveiligheid garandeert. Rust is syntactisch vergelijkbaar met C++, maar biedt betere garanties voor geheugenveiligheid. Rust heeft ook een aantal functies die het gemakkelijker maken om veilige code te schrijven, zoals het eigendoms- en leensysteem.Veel meer informatie
Meer geweldige links
- Wat is corrosie?
- Corrosionsource.com
 Nieuwe op papier gebaseerde technologie maakt betrouwbare, goedkope detectie van ijzerniveaus in verrijkte voedingsmiddelen
Nieuwe op papier gebaseerde technologie maakt betrouwbare, goedkope detectie van ijzerniveaus in verrijkte voedingsmiddelen Nieuw coatingproces biedt effectieve bescherming voor remschijven
Nieuw coatingproces biedt effectieve bescherming voor remschijven Brandstof uit diamanten?
Brandstof uit diamanten? Nieuwe techniek bereidt 2-D perovskiet-eenkristallen voor voor de hoogste fotodetectie
Nieuwe techniek bereidt 2-D perovskiet-eenkristallen voor voor de hoogste fotodetectie Hoe Graden Brix in Sugar
Hoe Graden Brix in Sugar
 Ontdekking van sediment ontsluit het verborgen netto-nulpotentieel van Australië
Ontdekking van sediment ontsluit het verborgen netto-nulpotentieel van Australië  NASA vindt windschering die tropische storm Edouard . treft
NASA vindt windschering die tropische storm Edouard . treft Hoe bouwen katoenstaartkonijnen een nest om geboorte te geven?
Hoe bouwen katoenstaartkonijnen een nest om geboorte te geven?  Redders gehinderd door beschadigde wegen, meer regen in Indonesië
Redders gehinderd door beschadigde wegen, meer regen in Indonesië Blackout na de tyfoon roept vragen op over rampen in Japan
Blackout na de tyfoon roept vragen op over rampen in Japan
Hoofdlijnen
- Onderzoekers gebruiken het ritme van DNA-replicatie om kankercellen te doden
- Chromosoomorganisatie komt voort uit 1-D-patronen
- Waarom herinneren we ons pijn?
- Hoe verschillen schimmelsporen van bacteriële endosporen?
- Nieuwe kandidaat-genen voor menselijke mannelijke onvruchtbaarheid gevonden door het ongebruikelijke voortplantingssysteem van gorilla's te analyseren
- Wolven bleken meer coöperatief te zijn met hun eigen soort dan honden met die van hen
- Hoe is een Cells DNA net als de boeken in een bibliotheek?
- Onderzoek naar het verleden van aardappelen kan de spuds van de toekomst verbeteren
- Een bouwsteen voor leverfitness op oudere leeftijd
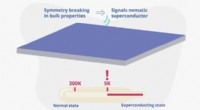
- Onverwachte eigenschappen ontdekt in recent ontdekte supergeleider
- Hoogdimensionale kwantumversleuteling voor het eerst uitgevoerd in echte stadsomstandigheden

- Micro-organismen gebruiken om de waterkwaliteit snel te controleren

- Decodering van elektronendynamica
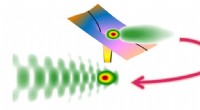
- Een supergeleidende toekomst leiden met grafeen-kwantummagie

 Orkaan Ian treft Cuba als storm van categorie 3
Orkaan Ian treft Cuba als storm van categorie 3 Wetenschappers bakken glutenvrij brood met een revolutionaire technologie
Wetenschappers bakken glutenvrij brood met een revolutionaire technologie Onderzoekers ontwikkelen een vast materiaal met mobiele deeltjes die reageren op de omgeving
Onderzoekers ontwikkelen een vast materiaal met mobiele deeltjes die reageren op de omgeving Een samengestelde machine maken voor een schoolproject
Een samengestelde machine maken voor een schoolproject  Nieuwe behandelingstechnologie kan de belasting van nucleair afval in het VK verminderen
Nieuwe behandelingstechnologie kan de belasting van nucleair afval in het VK verminderen Een alternatieve opstelling:hoe een propellervormig isomeer organische zonnecellen kan verbeteren
Een alternatieve opstelling:hoe een propellervormig isomeer organische zonnecellen kan verbeteren  Grootschalige koolstofvastlegging in bossen kan de voedselprijzen doen stijgen
Grootschalige koolstofvastlegging in bossen kan de voedselprijzen doen stijgen Blockchain komt duurzame voedselproductie ten goede
Blockchain komt duurzame voedselproductie ten goede
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

