
Wetenschap
De wetenschap achter het bevriezen van water:van moleculen tot ijsexpansie
Door Ann Johnson, bijgewerkt op 24 maart 2022
Moleculaire beweging tijdens bevriezing
Wanneer water van vloeibaar naar vast verandert, gaan de moleculen van een constante, chaotische dans naar een zeer geordend rooster. In vloeibare toestand botsen moleculen, glijden langs elkaar heen en blijven nooit lang op dezelfde plek. Naarmate de temperatuur daalt tot 0°C, vertraagt de beweging en sluiten de moleculen zich aan in een zich herhalende, kristallijne opstelling die we als ijs zien.
Moleculaire aantrekkingskracht en het vriespunt
Elk molecuul ervaart krachten die het naar zijn buren trekken. Sterke aantrekkingskrachten, zoals die in koolstof, kunnen atomen zelfs op duizenden graden bij elkaar houden, terwijl zwakke krachten in helium ervoor zorgen dat het gasvormig blijft tot extreme kou. De intermoleculaire krachten van water zijn gematigd:sterk genoeg om moleculen bij elkaar te houden bij een temperatuur van 32 °F, maar toch zwak genoeg om bij 0 °C (32 °F) weer te smelten. Dit evenwicht geeft water zijn unieke vriestemperatuur.
Vriespuntverlaging met opgeloste stoffen
Door stoffen als suiker, zout of alcohol toe te voegen, wordt de temperatuur waarbij water bevriest verlaagd. Hoe meer opgeloste stof u toevoegt, hoe groter de daling. Dat is de reden dat wegploegen zout op ijzige trottoirs strooien. Zout verlaagt het vriespunt, waardoor ijs in vloeibaar water verandert, zelfs als de temperatuur net onder de 32°F blijft. Op dezelfde manier blijft wodka, die ongeveer 40% ethanol bevat, vloeibaar in een standaardvriezer omdat de aanwezigheid van alcohol het vriespunt met enkele graden verlaagt.
IJsvorming, uitzetting en kristalstructuren
De meeste materialen trekken samen bij afkoeling, maar water gedraagt zich anders. Het bereikt de maximale dichtheid bij ongeveer 39 F (4 C). Daaronder zet water uit naarmate de moleculen een hexagonaal rooster aannemen, waardoor gaten ontstaan die ijs minder dicht maken dan vloeibaar water. Deze uitzetting is de reden dat er sneeuwvlokken ontstaan, terwijl de zeshoekige opstelling blijft uitgroeien tot delicate kristallen.
De druk van uitzettend ijs
Omdat ijs uitzet, kan een afgesloten bak met water scheuren als deze bevroren is. De druk die wordt uitgeoefend door uitzettend ijs kan oplopen tot 40.000 psi bij –22 °C (7,6 °F). Zelfs robuuste containers, zoals staal of ijzer, kunnen onder deze belasting bezwijken. Daarom zie je vaak flessen barsten in de vriezer.
 Brexit 1.0:wetenschappers vinden bewijs van de oorspronkelijke scheiding van Groot-Brittannië van Europa
Brexit 1.0:wetenschappers vinden bewijs van de oorspronkelijke scheiding van Groot-Brittannië van Europa Het sprookjesachtige boshyacintenbos van België slachtoffer van eigen schoonheid
Het sprookjesachtige boshyacintenbos van België slachtoffer van eigen schoonheid NASA vindt tropische depressie 13W aan de zuidoostkust
NASA vindt tropische depressie 13W aan de zuidoostkust Oude regenmeter:nieuw bewijs verbindt grondwater, klimaatveranderingen in diepe tijd
Oude regenmeter:nieuw bewijs verbindt grondwater, klimaatveranderingen in diepe tijd De eerste weergave van verwering op angströmschaal
De eerste weergave van verwering op angströmschaal
Hoofdlijnen
- Wat is de naam van kleine organismen die je nodig hebt om een microscoop te zien?
- Welke criteria gebruiken wetenschappers om te bepalen of iets organisme is of niet?
- De associatie van planten en schimmels in mycorrhizae illustreert een type relatie?
- Evenwichtige bemesting:een steunpunt voor duurzame productie van maïs en rijst in Afrika
- Hoe leidt DNA wetenschappers ertoe om organismen beter te classificeren?
- Beweging van grote moleculen in een cel wordt genoemd?
- Wat is een celanalogie voor de nucleous?
- Wat is het proces van organismen die zich in de loop van de tijd aan hun omgeving aanpassen?
- Welke structuur van een cel helpt bij het handhaven van homeostase door dingen naar of uit cel te verplaatsen?
- Past één maat allemaal? Een nieuw model voor organische halfgeleiders

- Membraanlaadsensor om de regulatie van onze T-cellen te bekijken
- Spinazie gebruikt in neutronenstudies zou het geheim kunnen ontrafelen voor een sterkere plantengroei

- Hoe maak je lijmen voor elektronica, voertuigen, en moeilijker bouwen?
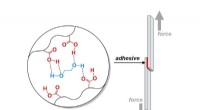
- Onderzoekers ontwikkelen micro-organismen om vervuiling door PET-plastic aan te pakken
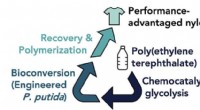
 Hoe zal radium reageren met zuurstof?
Hoe zal radium reageren met zuurstof?  Welke methode wordt gebruikt om metalen te extraheren die boven koolstof staan in de reactiviteitsreeks?
Welke methode wordt gebruikt om metalen te extraheren die boven koolstof staan in de reactiviteitsreeks?  In hun dichtste afstemming in 800 jaar, Jupiter en Saturnus zullen een wonder creëren:een kerstster
In hun dichtste afstemming in 800 jaar, Jupiter en Saturnus zullen een wonder creëren:een kerstster 304 oz is gelijk aan hoeveel pond?
304 oz is gelijk aan hoeveel pond?  Een effectieve manier om atrazin en zijn bijproducten in oppervlaktewater te elimineren
Een effectieve manier om atrazin en zijn bijproducten in oppervlaktewater te elimineren Hoe beïnvloedt een type plant transpiratie?
Hoe beïnvloedt een type plant transpiratie?  Waarom koolstofdioxide zo'n buitensporige invloed heeft op het klimaat op aarde?
Waarom koolstofdioxide zo'n buitensporige invloed heeft op het klimaat op aarde? Computermodellen tonen aan dat hittegolven in het noorden van de Stille Oceaan mogelijk te wijten zijn aan het feit dat China de aerosolen terugdringt
Computermodellen tonen aan dat hittegolven in het noorden van de Stille Oceaan mogelijk te wijten zijn aan het feit dat China de aerosolen terugdringt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

