
Wetenschap
Evenwichtsdrukken berekenen:een stapsgewijze handleiding
Door Lee Johnson • Bijgewerkt op 24 maart 2022
Chemisch evenwicht beschrijft de stabiele toestand van een omkeerbare reactie waarbij reactanten met gelijke snelheden in producten worden omgezet en omgekeerd. In de praktijk kwantificeren scheikundigen dit evenwicht met behulp van de evenwichtsconstante Kp , die de partiële drukken van de betrokken gassen met elkaar verbindt.
De evenwichtsconstante begrijpen
Voor een algemene gasfasereactie:
\(aA(g)+bB(g)\rechtslinksharpoenen cC(g)+dD(g)\)
de evenwichtsconstante wordt gedefinieerd als:
\(K_p =\frac{(P_C)^c(P_D)^d}{(P_A)^a(P_B)^b}\)
Wanneer alle stoichiometrische coëfficiënten gelijk zijn aan één, wordt de uitdrukking vereenvoudigd tot ‘producten over reactanten’. Deze vorm is alleen geldig bij evenwicht.
Soms zie je de evenwichtsconstante uitgedrukt in termen van molaire concentraties, Kc , gerelateerd aan Kp door:
\(K_p =K_c (RT)^{\Delta n}\)
waarbij Δn de verandering is in het aantal gasmollen tussen producten en reactanten.
De vergelijking herschikken om evenwichtsdruk te vinden
De belangrijkste stap is het introduceren van de variabele x , wat de verandering in druk vertegenwoordigt van de beginwaarde naar evenwicht. Stel dat de begindruk van elke reactant P_i is en de producten beginnen bij nuldruk. Vervolgens kan elke evenwichtsdruk worden uitgedrukt in termen van x .
Met alle coëfficiënten ingesteld op één, de Kp expressie wordt:
\(\begin{uitgelijnd}K_p &=\frac{x^2}{(P_i - x)^2}\end{uitgelijnd}\)
Oplossen voor x geeft:
\(x =\frac{\sqrt{K_p}\,P_i}{1 + \sqrt{K_p}}\)
De partiële evenwichtsdruk van een reactant is P_i - x , terwijl die van een product simpelweg x is .
Voorbeeld:productie van chloormethaan
Kijk eens naar de reactie:
\(\text{CH}_3\text{OH(g)} + \text{HCl(g)} \rightleftharpoons \text{CH}_3\text{Cl(g)} + \text{H}_2\text{O(g)}\)
Met Kp =5{}900 en een initiële druk P_i =0,75 atm voor elke reactant, bereken x :
\(\begin{uitgelijnd} x &=\frac{\sqrt{K_p}\,P_i}{1 + \sqrt{K_p}} \\ &=\frac{\sqrt{5900}\times 0,75\;\text{atm}}{1 + \sqrt{5900}} \\ &\ approx 0,74\;\text{atm}\end{uitgelijnd}\)
De evenwichtsdruk van elk product is dus ongeveer 0,74 atm, en die van elke reactant is 0,75 - 0,74 =0,01 pinautomaat
Door deze systematische aanpak te volgen, kunt u nauwkeurig de evenwichtsdrukken bepalen voor elke gasfasereactie.
 Continue monitoring van eiwitten een game-changer voor patiënten met snel verslechterende aandoeningen
Continue monitoring van eiwitten een game-changer voor patiënten met snel verslechterende aandoeningen Hoe definiëren of bepalen atomen elementen?
Hoe definiëren of bepalen atomen elementen?  Welke van de volgende is een organisch molecuul ijzeroxide sucrose water of zuurstofgas?
Welke van de volgende is een organisch molecuul ijzeroxide sucrose water of zuurstofgas?  Thermodynamica uitgelegd:de drie wetten die de energie in het universum beheersen
Thermodynamica uitgelegd:de drie wetten die de energie in het universum beheersen  Wat produceert ATP NADH en CO2?
Wat produceert ATP NADH en CO2?
Hoofdlijnen
- Wat zijn enkele overeenkomsten in uiteenlopende en convergente evolutie?
- Walvisliederen weerspiegelen de menselijke taal:een onderzoek toont aan dat de wet van Zipf van toepassing is op bultruggen
- Welke organismen vormen de biologische gemeenschappen van het benthische rijk?
- Wat voor soort Scientis bestudeert virussen?
- Tweelingen versus klonen:de verschillen begrijpen
- Hoe ontwikkelen en groeien Amphebians?
- Welke lichaamscellen ondergaan mesiose?
- Hoe een molecuul met twee gezichten problematische genen tot zwijgen kan brengen
- Voorbeeld van gemeenschappelijke namen om levende organismen te identificeren?
- Een 3D-zuurstofatoommodel maken:stapsgewijze handleiding
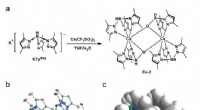
- Bio-geïnspireerde moleculaire kleurstoffen voor biomedische fluorescerende beeldvorming

- Licht van zeldzame aarde:nieuwe kansen voor organische light-emitting diodes
- Kunststoffen, brandstoffen en chemische grondstoffen uit CO2? Ze werken eraan
- Uitbreidbaar schuim voor 3D-printen van grote objecten

 Hoe beïnvloeden antibiotica de eiwitsynthese?
Hoe beïnvloeden antibiotica de eiwitsynthese?  Wat is de vergelijking voor natriumthiosulfaat en ijzernitraat alstublieft?
Wat is de vergelijking voor natriumthiosulfaat en ijzernitraat alstublieft?  Waarom worden de covalente verbindingen niet geëlektrolyseerd?
Waarom worden de covalente verbindingen niet geëlektrolyseerd?  Wat is een geconserveerde hoeveelheid?
Wat is een geconserveerde hoeveelheid?  Hoe noem je iemand die dieren bestudeert?
Hoe noem je iemand die dieren bestudeert?  Vier elementen maken een 2D optisch platform
Vier elementen maken een 2D optisch platform Hoe zijn cowbirds parasieten?
Hoe zijn cowbirds parasieten?  Wat gebeurt er als een atoom ijzer wordt met een 2 lading?
Wat gebeurt er als een atoom ijzer wordt met een 2 lading?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

