
Wetenschap
Waarom eieren krimpen in oplossingen met veel opgeloste stoffen:een duidelijke uitleg over osmose
Door Mary Tarsi | Bijgewerkt op 24 maart 2022
Waarom eieren krimpen in oplossingen met veel opgeloste stoffen
Een ei verliest volume als het in een oplossing wordt geplaatst met een hogere concentratie opgeloste stoffen dan in het ei. In een dergelijke oplossing beweegt het oplosmiddel (water) door osmose uit het ei, waardoor het ei krimpt. Het fenomeen demonstreert het basisprincipe van de cellulaire waterbalans.
Stap 1:Verwijder de schaal
Los eerst de schaal op met azijn. Het azijnzuur reageert met het calciumcarbonaat, waardoor het semipermeabele membraan van het ei intact blijft.
Stap 2:plaats het ei in een oplossing
Dompel het schaalvrije ei onder in een homogeen mengsel, bijvoorbeeld water, glucosestroop of honing. De concentratie opgeloste stoffen in de oplossing bepaalt de richting van de waterbeweging.
Osmose begrijpen
Osmose is de passieve waterstroom door een semipermeabel membraan van een gebied met een lagere concentratie opgeloste stoffen naar een gebied met een hogere concentratie, met als doel de concentraties aan beide zijden gelijk te maken. Wanneer de externe oplossing hypertoon is (hogere concentratie opgeloste stoffen), verlaat water het ei, waardoor krimp ontstaat. Als de oplossing hypotoon is, zwelt het ei op. Een isotone oplossing houdt het ei onveranderd.
De rol van het semipermeabele membraan
Alleen kleine moleculen zoals water kunnen het membraan passeren; grotere opgeloste moleculen (bijvoorbeeld suiker in glucosestroop) zijn uitgesloten. Deze selectieve permeabiliteit is de reden dat het ei kan krimpen in suikerhoudende oplossingen.
In onderwijsomgevingen biedt dit experiment een praktische illustratie van osmose en membraanpermeabiliteit.
 Welk polyatomisch ion vormt een neutrale verbinding in combinatie met groep 1A monatomic in 1 tot 2 verhouding?
Welk polyatomisch ion vormt een neutrale verbinding in combinatie met groep 1A monatomic in 1 tot 2 verhouding?  Wat zijn chemische kenmerken van seleniums?
Wat zijn chemische kenmerken van seleniums?  Wat zijn de 2 soorten verbindingen die elk beschrijven?
Wat zijn de 2 soorten verbindingen die elk beschrijven?  Een veiligere manier om aziden te maken voor gebruik in klikchemie
Een veiligere manier om aziden te maken voor gebruik in klikchemie Kernfusie Hoe reactoren werken
Kernfusie Hoe reactoren werken
 Studie identificeert eerste stap om waterschaarste te verslaan
Studie identificeert eerste stap om waterschaarste te verslaan Aanhoudende niveaus van matige opwarming kunnen de Oost-Antarctische ijskap doen smelten
Aanhoudende niveaus van matige opwarming kunnen de Oost-Antarctische ijskap doen smelten De soorten reptielen in Vietnam
De soorten reptielen in Vietnam Planten zijn afhankelijk van de atmosfeer als grootste bron van?
Planten zijn afhankelijk van de atmosfeer als grootste bron van?  Onderzoek naar de impact van klimaatverandering op snowpack
Onderzoek naar de impact van klimaatverandering op snowpack
Hoofdlijnen
- Kennis van larvale vissen slechts een druppel op de gloeiende plaat
- Een dunne bedekking die de cellen in alle levende dingen hebben?
- Waar lipiden worden geproduceerd, hebben gespecialiseerde functies?
- Kan een organisme met een GG -genotype gameten produceren of het dominante of recessieve allel in gelijke hoeveelheden?
- Deze sociale wetenschap zou de gezinsstructuur van Romeinen bestuderen.
- Methode maakt inzichtelijk wat bacteriën in hun omgeving waarnemen
- Welke organel helpt bij de dierencel van de celdeling?
- Wat zijn het verschil dat wetenschap wordt geprojecteerd?
- Wat is de naam voor een complexe georganiseerde groep organismen?
- Nieuwe zilveren holle vezel verhoogt de elektroreductie van CO2
- Hoe u de temperatuurstijging kunt berekenen:een eenvoudige stapsgewijze handleiding

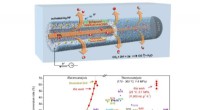
- Benchmarks om de zon beter te vangen

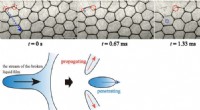
- Twee verschillende fysieke mechanismen geïdentificeerd voor hoe eenvoudig schuim instort
- Wetenschappers vinden een kunstmatige neus uit voor continue bacteriële monitoring
 Moet het woord Mercurius zoals in element worden gekapitaliseerd?
Moet het woord Mercurius zoals in element worden gekapitaliseerd?  Europese moslims ervaren de EU positiever dan andere Europeanen
Europese moslims ervaren de EU positiever dan andere Europeanen Wat is de belangrijkste energievaluta van alle cellen die worden genoemd?
Wat is de belangrijkste energievaluta van alle cellen die worden genoemd?  Was de temperatuur 5,2 biljoen jaar geleden -270 graden Celsius?
Was de temperatuur 5,2 biljoen jaar geleden -270 graden Celsius?  Wat is een glaciale afzetting en een voorbeeld?
Wat is een glaciale afzetting en een voorbeeld?  Gegevens van zeeolifanten onthullen nieuwe kenmerken van de Blob-hittegolf op zee
Gegevens van zeeolifanten onthullen nieuwe kenmerken van de Blob-hittegolf op zee Waarom gaan mutatie die optreden op lichaamscellen niet door aan zijn nakomelingen?
Waarom gaan mutatie die optreden op lichaamscellen niet door aan zijn nakomelingen?  Welk enzym versnelt de reactie van CO2 en H2O om koolzuur te vormen?
Welk enzym versnelt de reactie van CO2 en H2O om koolzuur te vormen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

