
Wetenschap
Variabele valentie:hoe elementen hun ladingstoestanden in de chemie verschuiven
Door David Stewart • Bijgewerkt op 24 maart 2022
Elektronen draaien in discrete energieniveaus rond een atoomkern. De buitenste elektronen, bekend als valentie-elektronen, bepalen hoe een atoom met anderen interageert. Atomen streven ernaar een stabiele configuratie te bereiken die lijkt op het dichtstbijzijnde edelgas, meestal door deze elektronen te doneren, te accepteren of te delen. Dit gedrag wordt de valentie van een atoom genoemd.
TL;DR
Variabele valentie beschrijft het vermogen van een element om verschillende ladingstoestanden te vertonen, afhankelijk van de reactie. IJzer vormt bijvoorbeeld FeO met een +2 valentie en Fe2O3 met een +3 valentie.
Valentie en binding
Wanneer een atoom valentie-elektronen doneert of accepteert, ontstaat er vaak een ionische binding. Omgekeerd, wanneer atomen deze elektronen delen, vormt zich een covalente binding. Beide typen bindingen zijn van cruciaal belang voor de structuur en eigenschappen van chemische verbindingen.
Variabele valentie
Sommige elementen houden zich niet aan één enkele valentie. Hun oxidatietoestanden variëren afhankelijk van de chemische omgeving en beïnvloeden de eigenschappen van de resulterende verbindingen. De verschuiving van ijzer van +2 in ijzeroxide (FeO) naar +3 in ijzeroxide (Fe2O3) is een voorbeeld van dit fenomeen. Het magnetische gedrag van deze oxiden verschilt dienovereenkomstig.
Elementen die variabele valentie vertonen
- Overgangsmetalen:ijzer (Fe), nikkel (Ni), koper (Cu), tin (Sn)
- Niet-metalen:stikstof (N), zuurstof (O), waterstof (H)
Voorbeelden hiervan zijn waterstofperoxide (H2O2), waarbij waterstof een valentie van +2 heeft, versus water (H2O), waar waterstof +1 is. Stikstof komt voor in ammonium (NH4+), waar het een valentie van -3 heeft, en in lachgas (N2O), waar het +1 is.
Vertegenwoordigt variabele valentie
Chemici duiden de oxidatietoestand van een element aan met een Romeins cijfer in superscript naast het symbool. Bijvoorbeeld P V Cl5 geeft aan dat fosfor zich in de +5-toestand bevindt in fosforpentachloride.
Gegevens afkomstig uit de International Union of Pure and Applied Chemistry (IUPAC) en standaard handboeken over anorganische chemie.
 Hoeveel mol N2 worden geproduceerd door de ontleding 2.88 mol natriumazide?
Hoeveel mol N2 worden geproduceerd door de ontleding 2.88 mol natriumazide?  Wat is de juiste volgorde van de nucleaire vervalmodus voor wijzigingen van U-238 naar U-234?
Wat is de juiste volgorde van de nucleaire vervalmodus voor wijzigingen van U-238 naar U-234?  Polariteit in de chemie begrijpen:hoe elektronen moleculen vormen
Polariteit in de chemie begrijpen:hoe elektronen moleculen vormen  Stoffen die bij relatief lage temperaturen kunnen worden getransformeerd in een gas worden genoemd?
Stoffen die bij relatief lage temperaturen kunnen worden getransformeerd in een gas worden genoemd?  Wetenschappers bouwen M29-clustermodelkatalysator
Wetenschappers bouwen M29-clustermodelkatalysator
 Waarom vallen objecten naar het centrum van de aarde?
Waarom vallen objecten naar het centrum van de aarde?  Wat is actieve kool en waarom wordt het gebruikt in filters?
Wat is actieve kool en waarom wordt het gebruikt in filters?  Wat kan ervoor zorgen dat de Mississippi-bocht hypoxisch wordt?
Wat kan ervoor zorgen dat de Mississippi-bocht hypoxisch wordt? Dieren zien de wereld in andere kleuren dan mensen:een nieuwe camera laat zien hoe dit eruit ziet
Dieren zien de wereld in andere kleuren dan mensen:een nieuwe camera laat zien hoe dit eruit ziet  Wat is nut van wetenschap aan de mens?
Wat is nut van wetenschap aan de mens?
Hoofdlijnen
- Honingbijen steken minder snel in grotere groepen
- Wat is een woord voor bacteriën?
- Hoe plankton en bacteriën oceaanspray vormen
- Wat waren de eerste kennis van levende organismen op aarde en wanneer verschenen ze?
- Hoe verschilt DNA in cellen dan individuen?
- Groenlandse walvissen komen naar Cumberland Sound in Nunavut om te exfoliëren
- Mariene microplastics:hoe de verspreiding van watermassa de transporttrajecten beïnvloedt
- Waarom worden virussen niet opgenomen als onderdeel van de celtheorie?
- Groter en slimmer:hebben dingo's thylacines gedood?
- Slimme inkt voegt nieuwe dimensies toe aan 3D-printen

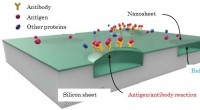
- Een halfgeleiderchip detecteert antigeenconcentraties bij 1 delen per quadriljoen molmassa
- Elektrostatische kracht neemt de leiding in bio-geïnspireerde polymeren

- Wetenschappers ontwikkelen zeer gevoelige moleculaire optische druksensor

- Positiespecifieke isotoopeffecten in butaan - een nieuwe geochemische tracer

 Veroorzaken bases denaturatie van eiwitten?
Veroorzaken bases denaturatie van eiwitten?  De traditie verklaart waarom sommige stokstaartjes uitslapers zijn
De traditie verklaart waarom sommige stokstaartjes uitslapers zijn  Wat mengt zich met stikstof om paars te worden?
Wat mengt zich met stikstof om paars te worden?  Hoe de koffie-industrie op het punt staat te worden gebrand door klimaatverandering
Hoe de koffie-industrie op het punt staat te worden gebrand door klimaatverandering Nieuw-Zeeland introduceert baanbrekende nulkoolstofrekening, inclusief doelen voor landbouwmethaan
Nieuw-Zeeland introduceert baanbrekende nulkoolstofrekening, inclusief doelen voor landbouwmethaan Welk element is NH4CL?
Welk element is NH4CL?  Productiesubsidies:het geheim van het succes van China?
Productiesubsidies:het geheim van het succes van China?  Wat is de weerstand van Germanium?
Wat is de weerstand van Germanium?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

