
Wetenschap
Hoe atomen zich binden om verbindingen te vormen:een duidelijke gids voor ionische, covalente, metallische en waterstofbindingen
Door Carolyn Kaberline | Bijgewerkt op 24 maart 2022
Afbeelding met dank aan Prill/iStock/GettyImages
Hoewel atomen als geïsoleerde entiteiten kunnen bestaan, combineren ze meestal met andere atomen om verbindingen te creëren. De kleinste stabiele eenheid van een verbinding wordt een molecuul genoemd, en de vorming ervan hangt af van het type chemische binding dat de atomen bij elkaar houdt. De vier primaire typen bindingen (ionisch, covalent, metallisch en waterstof) hebben elk verschillende mechanismen en verlenen unieke eigenschappen aan de resulterende moleculen.
Ionische binding
Ionische bindingen ontstaan wanneer een atoom een of meer valentie-elektronen aan een ander atoom schenkt, waardoor tegengesteld geladen ionen ontstaan die elektrostatisch aantrekken. Een klassiek voorbeeld is de reactie van natrium (Na) met chloor (Cl). Natrium, met een enkel elektron in de buitenste schil, verliest dat elektron gemakkelijk en wordt Na⁺, terwijl chloor, bijna vol bij zeven valentie-elektronen, een elektron krijgt om Cl⁻ te worden. De elektrostatische aantrekkingskracht tussen Na⁺ en Cl⁻ resulteert in de neutrale, stabiele verbinding natriumchloride (NaCl). Ionische binding omvat doorgaans een volledige overdracht van elektronen en komt het meest voor tussen metalen en niet-metalen.
Covalente binding
Covalente bindingen ontstaan daarentegen wanneer atomen valentie-elektronen delen in plaats van ze over te dragen. Niet-metaalatomen, zoals koolstof, zuurstof en stikstof, hebben de neiging covalente bindingen te vormen. Door elektronen te delen bereikt elk atoom een stabiele elektronenconfiguratie, vaak de octetregel. Afhankelijk van het aantal gedeelde elektronenparen kunnen covalente bindingen enkelvoudig (één paar), dubbel (twee paren) of drievoudig (drie paren) zijn. Een zuurstofmolecuul (O₂) vormt bijvoorbeeld een dubbele covalente binding tussen twee zuurstofatomen, terwijl stikstof (N₂) een drievoudige binding heeft. Deze gedeelde elektronen zorgen ervoor dat moleculen in een gebalanceerde, energiezuinige toestand kunnen bestaan.
Metaalbinding
Metaalbindingen vinden uitsluitend plaats tussen metaalatomen. In deze opstelling worden valentie-elektronen gedelokaliseerd en vormen ze een ‘zee van elektronen’ die vrij rond een rooster van positief geladen metaalionen bewegen. Deze elektronenmobiliteit is verantwoordelijk voor de kenmerkende eigenschappen van metalen:elektrische geleidbaarheid, thermische geleidbaarheid, ductiliteit en kneedbaarheid. De uitstekende elektrische prestaties van koper en het vermogen van ijzer om in dunne platen te worden gehamerd, zijn bijvoorbeeld directe gevolgen van de metaalverbindingsstructuur.
Waterstofbinding
Waterstofbinding is een gespecialiseerde, maar krachtige, intermoleculaire kracht die optreedt wanneer waterstof, gebonden aan een zeer elektronegatief atoom (zuurstof, stikstof of fluor), een gedeeltelijke positieve lading ervaart. Het elektronegatieve atoom heeft een gedeeltelijke negatieve lading, waardoor de waterstof van het ene molecuul de negatieve plaats van een ander molecuul kan aantrekken. Deze polariteit is de reden dat watermoleculen (H₂O) aan elkaar plakken, waardoor water zijn hoge oppervlaktespanning krijgt en veel stoffen kan oplossen. Waterstofbruggen beïnvloeden ook de structuur van eiwitten en DNA.
Bondingresultaten
Atomen kunnen afhankelijk van hun partners meer dan één type binding aangaan. Magnesium (Mg) kan bijvoorbeeld een ionische binding vormen met een niet-metaal zoals chloor (MgCl₂) of een metaalbinding met andere magnesiumatomen in een metaalrooster. Ongeacht het type binding is het eindresultaat een stabiele verbinding met onderscheidende fysische en chemische eigenschappen; eigenschappen die ten grondslag liggen aan alles, van alledaagse materialen tot geavanceerde technologieën.
Het begrijpen van deze bindingsmechanismen is van fundamenteel belang voor de scheikunde, materiaalkunde en talloze toegepaste velden. Door te begrijpen hoe atomen met elkaar omgaan, kunnen wetenschappers materiaalgedrag voorspellen, nieuwe stoffen ontwerpen en in verschillende sectoren innoveren.
 Spinzijde gemaakt door fotosynthetische bacteriën
Spinzijde gemaakt door fotosynthetische bacteriën Wat is een algemene verklaring met betrekking tot de grootte van deeltjesstoffen en hun gecombineerde volume wanneer ze worden gemengd?
Wat is een algemene verklaring met betrekking tot de grootte van deeltjesstoffen en hun gecombineerde volume wanneer ze worden gemengd?  Wat is het doel van frisdrank limoen in detectiestikstof die verbindingen bevat?
Wat is het doel van frisdrank limoen in detectiestikstof die verbindingen bevat?  Wat is het mengsel van voornamelijk stikstof en zuurstof?
Wat is het mengsel van voornamelijk stikstof en zuurstof?  Hebben nobele gassen een volledig octet van elektronen?
Hebben nobele gassen een volledig octet van elektronen?
 Supercomputer helpt wetenschappers nieuwe functies te vinden, mechanismen in tornado's
Supercomputer helpt wetenschappers nieuwe functies te vinden, mechanismen in tornado's Studie volgt stormwater orkaan Harvey met GPS
Studie volgt stormwater orkaan Harvey met GPS Mariene mist komt onder de aandacht in nieuwe vijfjarige studie
Mariene mist komt onder de aandacht in nieuwe vijfjarige studie NASA toont zwaarste regenval ontheemd in tyfoon Chan-hom
NASA toont zwaarste regenval ontheemd in tyfoon Chan-hom Het valt wel mee! Wetenschap, toerisme botsing op Great Barrier Reef
Het valt wel mee! Wetenschap, toerisme botsing op Great Barrier Reef
Hoofdlijnen
- Waar hoort Psilophyta bij de fylogenie?
- Welke seksuele reproductie kan zijn ontstaan als een manier voor cellen?
- Wat is de naam van het gebruikte celgebruik dat vorm en stijfheid geeft aan plantencellen?
- Welk organisme geloven dat wetenschappers voorouders zijn?
- Welke organel zou je verwachten in een dierlijke cellen, maar geen plantenoproepen?
- Waarom moet gedrag een genetische component hebben om te worden begunstigd door natuurlijke selectie?
- Toezichthouders overwegen wat ze moeten doen aan het ingestorte kreeftenbestand
- Zijn archaebacteriën of heterotrofe autotrofe saprofytic?
- Hoe belangrijke genen samenwerken om een gezonde huid te maken
- Een betere koolstofvanger haalt broeikasgassen uit de lucht en zet ze in gebruik
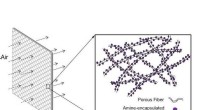
- Farmaconutritie:modern medicijnontwerp voor functionele studies
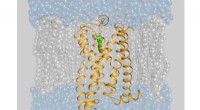
- Onderzoekers ontdekken een manier om in eiwitten te kijken om te zien hoe ze zijn bedraad
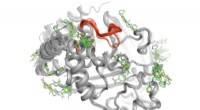
- Groeven houden belofte in voor verfijnde genezing

- Materialen voor waterstofservice ontwikkeld door nieuw multilab-consortium

 Leg uit hoe gistcellen kunnen worden beschouwd als eencellige organismen wanneer ze nog steeds met elkaar zijn verbonden.
Leg uit hoe gistcellen kunnen worden beschouwd als eencellige organismen wanneer ze nog steeds met elkaar zijn verbonden.  Onderzoekers ontwikkelen nieuwe manier om nanovezels te maken
Onderzoekers ontwikkelen nieuwe manier om nanovezels te maken Hoeveel seks is genoeg?
Hoeveel seks is genoeg?  Het pleidooi voor het delen van het risico op koolstofopslag
Het pleidooi voor het delen van het risico op koolstofopslag  Handgebreide moleculen
Handgebreide moleculen Wat is de rol van carotenoïden in fotosynthese?
Wat is de rol van carotenoïden in fotosynthese?  Waarom is zuurstof essentieel in onze atmosfeer?
Waarom is zuurstof essentieel in onze atmosfeer?  NASA's nieuwste testpiloten zijn ervaren astronauten, vrienden
NASA's nieuwste testpiloten zijn ervaren astronauten, vrienden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

