
Wetenschap
De eindtemperatuur voorspellen in een calorimeter:een stapsgewijze handleiding
Door John Brennan, bijgewerkt op 24 maart 2022
Afbeelding tegoed:tonuacatic/iStock/GettyImages
Calorimetrie is een hoeksteen van de experimentele thermochemie, waardoor wetenschappers reactie-enthalpieën en warmtecapaciteiten kunnen bepalen. Hoewel veel leerlingen het prettig vinden om de eindtemperatuur (T_f) van een calorimeterexperiment te meten, is een veel voorkomende uitdaging in de klas het voorspellen van T_f wanneer de reactie-enthalpie (ΔH_rxn) en de warmtecapaciteiten van alle componenten bekend zijn. In dit artikel wordt die berekening op een duidelijke, systematische manier doorgenomen.
Stap 1 – Identificeer de gegeven gegevens
Lees de probleemstelling aandachtig door. Meestal vind je het volgende:
- ΔH_rxn voor de reactie (kJ)
- Warmtecapaciteit van het reactiemengsel, C_p,inhoud (kJg⁻¹K⁻¹)
- Totale massa van de reactieproducten, m_contents (g)
- Calorimeterconstante, C_cal (kJK⁻¹)
- Begintemperatuur, T_i (°C)
Stap 2 – Ga uit van een perfecte calorimeter
In een ideale, adiabatische calorimeter gaat er geen warmte verloren naar de omgeving. Alle warmte die vrijkomt bij de reactie wordt geabsorbeerd door de calorimeter en de inhoud ervan.
Stap 3 – Stel de energiebalans in
Omdat de calorimeter en zijn inhoud dezelfde eindtemperatuur bereiken, is de vrijkomende warmte gelijk aan de opgenomen warmte:
ΔH_rxn =[C_p,inhoud × m_inhoud + C_cal] × (T_i – T_f)
Let op de aftrekkingsvolgorde:(T_i – T_f). Reactie-enthalpieën zijn negatief voor exotherme processen, dus deze tekenconventie houdt de algebra eenvoudig.
Stap 4 – Los T_f op
Herschik de vergelijking:
ΔH_rxn / [C_p,contents × m_contents + C_cal] = T_i – T_f
Draai het bord om en voeg T_i:
toeT_f = T_i – ΔH_rxn / [C_p,contents × m_contents + C_cal]
Stap 5 – Voer de cijfers in
Voorbeeld:ΔH_rxn =–200kJ, C_p,inhoud =0,00418kJg⁻¹K⁻¹, m_inhoud =200g, C_cal =2kJK⁻¹, T_i =25°C.
T_f = 25 – [–200 / (0.00418 × 200 + 2)]
= 25 – [–200 / 2.836]
= 25 + 70.5
= 95.5 °C
De eindtemperatuur bedraagt 95,5°C.
Dingen die nodig zijn
- Potlood en papier voor kraswerk
- Wetenschappelijke rekenmachine (of spreadsheet) voor rekenen
Referenties
- Chemische principes:de zoektocht naar inzicht , Peter Atkins et al., 2008
 De vervorming van enzymmoleculen die bij hoge temperaturen optreedt, staat bekend als?
De vervorming van enzymmoleculen die bij hoge temperaturen optreedt, staat bekend als?  Wat is de moleculaire formule voor 2-butyne?
Wat is de moleculaire formule voor 2-butyne?  Een proces waarin vloeibaar water in damp verandert?
Een proces waarin vloeibaar water in damp verandert?  Wat zijn de namen van volgende verbindingen CACL2 CUCL AGCL MG3P2?
Wat zijn de namen van volgende verbindingen CACL2 CUCL AGCL MG3P2?  Bleekmiddel:de meest effectieve chemische reiniger voor organisch afval
Bleekmiddel:de meest effectieve chemische reiniger voor organisch afval
 De EU moet zich aanpassen aan het opwarmende continent:ambtenaren
De EU moet zich aanpassen aan het opwarmende continent:ambtenaren  Hoe herken je man en vrouw Bluegills Apart
Hoe herken je man en vrouw Bluegills Apart  Hoe wordt het genoemd als alle organismen die in een gebied en niet -levende kenmerken van hun omgeving leven?
Hoe wordt het genoemd als alle organismen die in een gebied en niet -levende kenmerken van hun omgeving leven?  Emissiekenmerken van vuurvaste zwarte koolstofaërosolen van verbranding van verse biomassa
Emissiekenmerken van vuurvaste zwarte koolstofaërosolen van verbranding van verse biomassa Hoe meten we de veerkracht van de gemeenschap bij rampen?
Hoe meten we de veerkracht van de gemeenschap bij rampen?
Hoofdlijnen
- Wat is een term voor de vele manieren waarop wetenschapperwereld wereld om hen heen is?
- Wat is de functie van sponsachtig weefsel?
- Welke mobiele organel zou in een amoeba overspoeld voedsel omsluiten?
- Een cel met 10 chromosomen ondergaat mitose?
- Ontdekking van aminozuur onthult hoe licht huidmondjes in planten open maakt
- Wat zijn de reactenten van cellulaire ademhaling?
- Welk orgaan is nodig in een aseksuele reproductie?
- Welk deel van de dierencel maakt dingen in en uit cel?
- Kan de wetenschap verklaren waarom we zoenen met onze ogen dicht?
- Biomaterialen voor de regeneratie van bot- en kraakbeenweefsel uit appelafval
- Nieuw keramisch materiaal kan de kosten van piëzo-elektrische apparaten verlagen
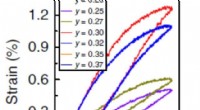
- Synchrotron onthult belangrijke informatie over het beroemde beeldhouwwerk van Paul Gauguin

- Kunstmatige fotosynthese kan nutteloos kooldioxide omzetten in mierenzuur dat in de industrie wordt gebruikt

- Natuurkundigen decoderen de dynamische interactie tussen moleculaire machines in metaal-organische raamwerken
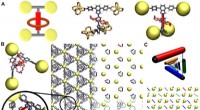
 Kubieke centimeters converteren naar granen
Kubieke centimeters converteren naar granen  Nieuw witboek brengt de zeer reële risico's in kaart die kwantumaanvallen met zich meebrengen voor Bitcoin
Nieuw witboek brengt de zeer reële risico's in kaart die kwantumaanvallen met zich meebrengen voor Bitcoin Feiten over Nylon
Feiten over Nylon De vorming van schakelbare en metastabiele discrete structuren door middel van chirale zelfsortering
De vorming van schakelbare en metastabiele discrete structuren door middel van chirale zelfsortering  Welk stuk apparatuur moet je klaar hebben voordat je het gaslicht een bunsenbrander draai?
Welk stuk apparatuur moet je klaar hebben voordat je het gaslicht een bunsenbrander draai?  Hebben bijgeloof over kometen en asteroïden een wetenschappelijke basis, waarom?
Hebben bijgeloof over kometen en asteroïden een wetenschappelijke basis, waarom?  Zal het wegglijden of vastgrijpen:Wetenschappers vragen zich af:'Wat is slakkenslijm?'
Zal het wegglijden of vastgrijpen:Wetenschappers vragen zich af:'Wat is slakkenslijm?'  Op welke snelheid is de massa van een elektron dubbel?
Op welke snelheid is de massa van een elektron dubbel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

