
Wetenschap
De vijf essentiële eigenschappen van water die het leven in stand houden
Door Catherine Carney | Bijgewerkt op 24 maart 2022
greenaperture/iStock/GettyImages
1. Cohesie en hechting
Watermoleculen zijn polair, met een licht negatieve lading op het zuurstofatoom en een licht positieve lading op de waterstofatomen. Deze polariteit creëert waterstofbruggen:aantrekkende krachten tussen de tegengestelde ladingen van aangrenzende moleculen. Het resultaat is cohesie (water plakt aan zichzelf) en adhesie (water kleeft aan andere hydrofiele oppervlakken). Deze eigenschappen geven water zijn hoge oppervlaktespanning, waardoor verschijnselen mogelijk zijn zoals capillaire werking bij planten en de “plakkerigheid” van een plas.
2. Temperatuurregeling
De waterstofbinding van water geeft het een hoge soortelijke warmte, een hoge verdampingswarmte en een krachtig verdampingskoelingseffect. Omdat het meer energie kost om deze bindingen te verbreken, is water bestand tegen snelle temperatuurveranderingen, waardoor ecosystemen en organismen worden gebufferd tegen extreme hitte of kou. De verdampingskoeling van zweten of transpiratie is een goed voorbeeld van deze natuurlijke thermostaat.
3. Oplosmiddelkracht
Polariteit maakt water ook tot een uitstekend oplosmiddel voor andere polaire of hydrofiele moleculen. Het lost gemakkelijk zouten, suikers en vele biologische macromoleculen op, waardoor talloze biochemische reacties mogelijk worden gemaakt. Daarentegen blijven niet-polaire, hydrofobe stoffen zoals oliën grotendeels onopgelost en vormen ze afzonderlijke fasen.
4. Dichtheidsafwijking – Uitbreiding bij bevriezing
In tegenstelling tot de meeste vloeistoffen zet water uit als het bevriest. Het stijve rooster gevormd door waterstofbruggen neemt meer volume in beslag dan het vloeibare rooster, dus ijs heeft een lagere dichtheid dan vloeibaar water. Dit zorgt ervoor dat ijs gaat drijven, waardoor watermassa's worden geïsoleerd en het waterleven behouden blijft tijdens koude seizoenen.
5. Neutrale pH
Zuiver water dissocieert in ongeveer gelijke concentraties H⁺- en OH⁻-ionen, wat een neutrale pH van 7 oplevert. Dankzij deze neutraliteit kan het dienen als buffer in biologische systemen, waarbij het zich aanpast aan lichtzure of basische omstandigheden die vereist zijn voor diverse enzymen.
Deze vijf onderling verbonden eigenschappen (cohesie/adhesie, temperatuurstabiliteit, oplosmiddelvermogen, uitzetting bij bevriezing en neutrale pH) maken water tot de hoeksteen van al het bekende leven.
 De wetenschap waarom 'broers en zussen of daten' zo moeilijk is
De wetenschap waarom 'broers en zussen of daten' zo moeilijk is  Hoe, wanneer en waarom industriële ecologie goed is voor het bedrijfsleven
Hoe, wanneer en waarom industriële ecologie goed is voor het bedrijfsleven  Extreem weer dat de Britse landbouw treft, maar aanpassing aan het veranderende klimaat een uitdaging voor veel boeren
Extreem weer dat de Britse landbouw treft, maar aanpassing aan het veranderende klimaat een uitdaging voor veel boeren De helft van de mangrove-ecosystemen in gevaar:natuurbeschermers
De helft van de mangrove-ecosystemen in gevaar:natuurbeschermers  Is Sydney in een torrid gematigde of koude zone?
Is Sydney in een torrid gematigde of koude zone?
Hoofdlijnen
- Soorten monomeren
- Wat zijn locomotaire organen in Euglena?
- Waarom is UV-licht schadelijk?
- Schrijf twee kenmerken van plantencel die het onderscheiden van dierencel?
- Wat is de functie van erythrocryten?
- Een organisme dat uit één cel bestaat, heeft geen kern?
- Eieren van wijnstokvretende insecten ontdekt op weg naar Californië:lopen wijngaarden gevaar?
- Wat is de studie van Way Body gebruikt stoffen in voedsel voor groeiregulering en onderhoudsweefsel?
- Wat is de functie van orbicularis oris?
- Het voorkomen van zuurstofafgifte leidt tot veiligere batterijen met een hoge energiedichtheid
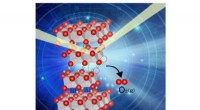
- De hoogste hittebestendige kunststof ooit is ontwikkeld uit biomassa
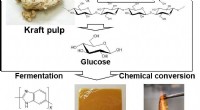
- Eenvoudige éénpotssynthese van medicamenteuze tricyclische peptiden
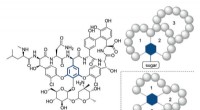
- Focus op kinetiek voor betere medicijnontwikkeling

- Onderzoekers maken blaastest die marihuana kan detecteren

 Waarom uw 5G-telefoon de luchtvaartindustrie aangaat:wat we weten over de impact op reizen, vluchten en meer
Waarom uw 5G-telefoon de luchtvaartindustrie aangaat:wat we weten over de impact op reizen, vluchten en meer Hoe bereiken enzymen het deel van de cel waarin ze nodig zijn?
Hoe bereiken enzymen het deel van de cel waarin ze nodig zijn?  'Gecko vision':sleutel tot de multifocale contactlens van de toekomst?
'Gecko vision':sleutel tot de multifocale contactlens van de toekomst?  Wat zijn de site van ATP -productie en fotosynthese?
Wat zijn de site van ATP -productie en fotosynthese?  Hoeveel deli liter naar liter?
Hoeveel deli liter naar liter?  Waarom zullen sommige stoffen in de chromatografie verder op het papier terechtkomen?
Waarom zullen sommige stoffen in de chromatografie verder op het papier terechtkomen?  Computeren met moleculen:een grote stap in moleculaire spintronica
Computeren met moleculen:een grote stap in moleculaire spintronica Welk probleem heeft een op aarde gebaseerde telescoop die een ruimte heeft die niet heeft?
Welk probleem heeft een op aarde gebaseerde telescoop die een ruimte heeft die niet heeft?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

