
Wetenschap
Een atoom diagrammen:een stapsgewijze handleiding
Door Maya Austen – Bijgewerkt op 24 maart 2022
Een atoom is de kleinste eenheid van een chemisch element dat zijn karakteristieke eigenschappen behoudt. Het bestaat uit een positief geladen kern – gemaakt van protonen en neutronen – en een wolk van negatief geladen elektronen die in een baan om de kern draaien. Om een atoom nauwkeurig in kaart te kunnen brengen, moet je het aantal protonen, neutronen en elektronen kennen, evenals de configuratie van de elektronenschil van het element.
Stap 1 – Zoek de basisgegevens van het element
Raadpleeg een modern periodiek systeem der elementen om het atoomnummer en het atoomgewicht te vinden van het element dat u wilt illustreren. De rastervierkanten van de tabel vermelden deze waarden; het atoomnummer verschijnt bovenaan elk vierkant, terwijl het atoomgewicht onderaan wordt weergegeven. Deze cijfers vormen de basis voor alle daaropvolgende berekeningen.
Stap 2 – Tel protonen en elektronen
Het atoomnummer is gelijk aan het aantal protonen in het atoom. Omdat neutrale atomen geen netto lading hebben, is het aantal elektronen identiek aan het aantal protonen. Stikstof (N) heeft bijvoorbeeld een atoomnummer van 7, dus een neutraal stikstofatoom bevat 7 protonen en 7 elektronen.
Stap 3 – Bepaal het aantal neutronen
Neutronen worden berekend met behulp van de formule:
Massagetal – Protonen =Neutronen
Om het massagetal te verkrijgen, rondt u het atoomgewicht af op het dichtstbijzijnde gehele getal. Het atoomgewicht van stikstof is 14,0067; afgerond is het massagetal 14. Het aftrekken van de 7 protonen geeft 14 – 7 =7 neutronen.
Stap 4 – Teken de kern
Schets een cluster van cirkels die de kern voorstellen. Gebruik één cirkel voor elk proton en één voor elk neutron. Onderscheid protonen door een positief teken toe te voegen of ze anders te kleuren, en neutronencirkels blanco te laten of ze uniform te kleuren. Dit cluster geeft visueel de samenstelling van de kern weer.
Stap 5 – Identificeer de Electron-Shell-configuratie
De elektronenschilconfiguratie geeft weer hoe elektronen de energieniveaus rond de kern bezetten. De configuratie van stikstof is bijvoorbeeld 1s²2s²2p³, wat betekent twee elektronen in de eerste schil en vijf in de tweede. Het begrijpen van deze opstelling is de sleutel tot nauwkeurig diagrammen.
Stap 6 – Schets de elektronenschillen
Teken concentrische ringen rond de kern, één voor elke schaal aangegeven door de configuratie. Plaats op elke ring kleine cirkels die de elektronen in die schil voorstellen; de eerste ring bevindt zich het dichtst bij de kern. Hiermee is de visuele weergave van het atoom voltooid.
 Australië verhuizen 2, 000 mensen van krachtig cyclonenpad
Australië verhuizen 2, 000 mensen van krachtig cyclonenpad Plantennomenclatuur:hoe namen het uiterlijk van planten onthullen
Plantennomenclatuur:hoe namen het uiterlijk van planten onthullen  Openbaarmaking van klimaatgerelateerde financiële risico's niet voldoende om actie te stimuleren
Openbaarmaking van klimaatgerelateerde financiële risico's niet voldoende om actie te stimuleren Wat zijn wetenschappelijke attitudes?
Wat zijn wetenschappelijke attitudes?  Waarom een koolstofprijs alleen niet genoeg zal zijn om de uitstoot van Nieuw-Zeeland te verlagen?
Waarom een koolstofprijs alleen niet genoeg zal zijn om de uitstoot van Nieuw-Zeeland te verlagen?
Hoofdlijnen
- Waarom we vleermuizen niet zo snel moeten demoniseren
- Wat is de belangrijkste organel in een cel en waarom?
- Wat is om te beginnen met een zaadje?
- Waarom is het belangrijk in de wetenschap dat we tests ontwerpen en uitvoeren die in staat zijn om een hypothese te vervalsen?
- Welke drie vormen kunnen bacteriecellen hebben?
- Waar bevat de erfelijke informatie van een organisme?
- Waarom was de wetenschap belangrijk voor Elizabeth Blackwell?
- Waarom zijn sommige slangen zo giftig?
- Waarom is de reproductie een belangrijk kenmerk van het leven?
- Chemische additieven verbeteren de stabiliteit van lithium-ionbatterijen met hoge dichtheid

- De weg verlichten om van chemische reactiepaden te wisselen

- Communicatie verstoren bij infectieuze bacteriën
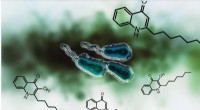
- Sensoren op plantenbladeren waarschuwen voor watertekort

- Gastro-intestinaal-bewoner, vormveranderende microdevices voor verlengde medicijnafgifte
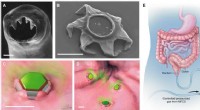
 Wat is het type energie in brandstoffen?
Wat is het type energie in brandstoffen?  Zelfbestuiving produceert zaden met genetische informatie van ouderplanten?
Zelfbestuiving produceert zaden met genetische informatie van ouderplanten?  Waarom meet je tijd bij de zon?
Waarom meet je tijd bij de zon?  Wat zijn voorbeelden van alternatieve vormen energie?
Wat zijn voorbeelden van alternatieve vormen energie?  wat alle mineralen?
wat alle mineralen?  Energieopslag oppompen met metaaloxiden
Energieopslag oppompen met metaaloxiden Wetenschapper breken de evolutie in welke twee catorgories?
Wetenschapper breken de evolutie in welke twee catorgories?  Wat zou er gebeuren als het licht van een ster door koele wolk van natriumgas gaat?
Wat zou er gebeuren als het licht van een ster door koele wolk van natriumgas gaat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

