
Wetenschap
Hoe u nauwkeurig de pH van een mengsel van twee chemicaliën kunt berekenen
Door Blake Flournoy | Bijgewerkt op 24 maart 2022
Afbeelding tegoed:StanislavSalamanov/iStock/GettyImages
De pH is de logaritmische maatstaf voor de waterstofionenconcentratie in een oplossing, variërend van 0 tot 14. Voor oplossingen met één component is het berekenen van de pH eenvoudig. Wanneer twee zuren of twee basen worden gecombineerd, wordt de berekening iets ingewikkelder, maar blijft deze met de juiste aanpak beheersbaar.
TL;DR
Het mengen van zuren of basen veroorzaakt een neutralisatiereactie waarbij zout (en soms water) ontstaat. Om de pH van een mengsel van twee chemicaliën te vinden:
- Bepaal het volume en de molariteit van elke component.
- Bereken het totaal aantal mol H⁺ (voor zuren) of OH⁻ (voor basen) dat in het mengsel is geïntroduceerd.
- Deel de totale H⁺-concentratie door het totale volume van de gemengde oplossing om [H⁺] te krijgen.
- Pas pH=–log₁₀[H⁺] toe.
Draag altijd geschikte PBM's, vooral als u met sterke zuren of basen werkt.
De pH begrijpen
pH kwantificeert de concentratie waterstofionen in een oplossing. Hoewel de term meestal wordt geassocieerd met vloeistoffen, is deze even relevant voor bodems, gels en andere media. Omdat de pH een logaritmische schaal is, kunnen kleine veranderingen in [H⁺] aanzienlijke verschuivingen in de zuurgraad of alkaliteit veroorzaken.
Componentberekeningen
Voordat u twee zuren of twee basen combineert, verzamelt u voor elke component de volgende gegevens:
- Volume (in liters of milliliters)
- Molariteit (molL⁻¹)
Bereken met behulp van deze informatie het aantal mol waterstofionen (voor zuren) of hydroxide-ionen (voor basen) dat door elke oplossing wordt bijgedragen. De som van deze mol vertegenwoordigt het totale ionengehalte van het mengsel.
Gemengde oplossingen
Zodra het totale aantal mol H⁺ bekend is, is de concentratie waterstofionen in het uiteindelijke mengsel:
[H⁺]=(totaal aantal molH⁺)/(totaal volume in liters)
Als twee zuren bijvoorbeeld respectievelijk 0,025 mol en 0,015 mol H⁺ leveren en het gecombineerde volume 200 ml (0,200 l) is, dan:
[H⁺]=(0,025+0,015)mol/0,200L=0,0002molL⁻¹
Tenslotte wordt de pH als volgt berekend:
pH=–log₁₀(0,0002)≈3,70
Herhaal de analoge stappen voor base-base mengsels, vervang [OH⁻] en gebruik de relatie pH=14–pOH.
 Is regenwater een geïoniseerd water?
Is regenwater een geïoniseerd water?  Wat is de naam van samengestelde CH3 CH2 BR?
Wat is de naam van samengestelde CH3 CH2 BR?  Nrl ontvangt patent voor koolstofafvangapparaat - een belangrijke stap in de productie van synthetische brandstof uit zeewater
Nrl ontvangt patent voor koolstofafvangapparaat - een belangrijke stap in de productie van synthetische brandstof uit zeewater Nieuwe methode maakt efficiënte monstervoorbereiding voor eencellige proteomics mogelijk
Nieuwe methode maakt efficiënte monstervoorbereiding voor eencellige proteomics mogelijk Wat is de formule voor één bariumatoom om de twee fluoratomen?
Wat is de formule voor één bariumatoom om de twee fluoratomen?
 Nabootsen hoe water en wind complexe vormen in de natuur creëren
Nabootsen hoe water en wind complexe vormen in de natuur creëren  Great Barrier Reef onthult snelle veranderingen van oude gletsjers
Great Barrier Reef onthult snelle veranderingen van oude gletsjers Waarom wordt Zuid-Amerika getroffen door dodelijke aardverschuivingen?
Waarom wordt Zuid-Amerika getroffen door dodelijke aardverschuivingen? Albert Einsten Wat is de wetenschappelijke houding die een wetenschapper moet bezitten?
Albert Einsten Wat is de wetenschappelijke houding die een wetenschapper moet bezitten?  Sprinkhanen de nieuwste vloek van extreme weersomstandigheden in Oost-Afrika
Sprinkhanen de nieuwste vloek van extreme weersomstandigheden in Oost-Afrika
Hoofdlijnen
- Eenvoudig epitheelweefsel:definitie, structuur en functionele voorbeelden
- Hebben gecontroleerde experimenten of meerdere waarnemingen geleid tot de generalisatie dat alle organismen uit cellen zijn samengesteld?
- Testen hoe goed biomarkers werken:nieuwe fluorescentiemicroscopiemethode kan de resolutie verbeteren tot op de Ångström-schaal
- Wat is een enylena alsjeblieft, ik heb een antwoord nodig voor mijn examen op cellen?
- Hoe krijgt een met veroudering geassocieerd enzym toegang tot ons genetisch materiaal?
- Wie zou er winnen in een gevecht tussen een grote witte haai en een blauwe vinvis?
- Wat is een organisme dat de nakomelingen van vele generaties dezelfde eigenschap hebben?
- Welke celorganellen omringen het nucleaire membraan?
- Hebben de billen meer bacteriën dan genitalia van vrouwen?
- Organische afstandhouders verbeteren de LED-prestaties
- Onze eerste blik op een nieuw lichtabsorberend eiwit in cyanobacteriën
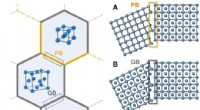
- Chemische grenstechniek gebruiken om staal te maken dat sterk en flexibel is zonder een hoog koolstofgehalte
- Neutronen gebruiken om te bestuderen hoe resistente bacteriën evolueren

- Van orkanen tot aardbevingen, ruimtestation experiment overwint uitdagingen

 Kunnen we een singulariteit zien, het meest extreme object in het universum?
Kunnen we een singulariteit zien, het meest extreme object in het universum?  Wat gebeurt er met de permafrost?
Wat gebeurt er met de permafrost?  Taalkundigen voorspellen onbekende woorden met behulp van taalvergelijking
Taalkundigen voorspellen onbekende woorden met behulp van taalvergelijking Onderzoekers spuiten ultradunne coatings die van kleur veranderen met slechts een paar atomen verschil in dikte
Onderzoekers spuiten ultradunne coatings die van kleur veranderen met slechts een paar atomen verschil in dikte Wetenschappers lossen een duurzaamheidsprobleem op in brandstofcellen voor waterstofauto's
Wetenschappers lossen een duurzaamheidsprobleem op in brandstofcellen voor waterstofauto's Citroenfruit versterken om beter bestand te zijn tegen klimaatverandering
Citroenfruit versterken om beter bestand te zijn tegen klimaatverandering Zonnecyclus 25 is begonnen
Zonnecyclus 25 is begonnen Wetenschappers ontrafelen verbrande 16e-eeuwse rol vrijwel
Wetenschappers ontrafelen verbrande 16e-eeuwse rol vrijwel
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

