
Wetenschap
Bepalen of atomen polair of niet-polair zijn:een praktische gids
Door Jess Kroll, bijgewerkt op 24 maart 2022
Wanneer atomen covalente bindingen vormen, delen ze elektronen om een stabiel molecuul te creëren. Als één atoom een sterkere aantrekkingskracht uitoefent op de gedeelde elektronen, krijgt het een gedeeltelijk negatieve lading terwijl het andere atoom een gedeeltelijk positieve lading draagt. Deze ongelijke ladingsverdeling definieert een polair molecuul, terwijl een gelijkmatige verdeling resulteert in een niet-polair molecuul. Volg deze stappen om te beoordelen of een specifiek atoom polair of niet-polair is.
Stap 1:Identificeer het obligatietype
Bepaal eerst of de binding covalent of ionisch is. Ionische bindingen vormen zich tussen ionen:atomen die elektronen hebben gewonnen of verloren en een netto lading hebben. Omdat bij ionische bindingen geladen soorten betrokken zijn, worden de atomen zelf niet beschreven als polair of niet-polair in de context van moleculaire polariteit. Bij covalente bindingen zijn daarentegen neutrale atomen betrokken die elektronen delen, en alleen atomen in dergelijke bindingen kunnen polariteit vertonen.
Stap 2:Onderzoek de atomaire samenstelling
Kijk vervolgens naar de elementen waaruit het molecuul bestaat. Homonucleaire bindingen (bijvoorbeeld N₂, O₂, O₃) delen de elektronen gelijkelijk, waardoor de atomen niet-polair worden. Heteronucleaire bindingen – die tussen verschillende elementen – hebben de neiging polair te zijn omdat de atomen verschillende elektronegativiteiten hebben. Voorbeelden hiervan zijn CO₂, waarbij de koolstof-zuurstofbindingen polair zijn, en H₂O, waarbij de waterstof-zuurstofbindingen sterk polair zijn. Als een molecuul meer dan één element bevat, zijn de atomen die betrokken zijn bij heteronucleaire bindingen doorgaans polair.
Stap 3:Beoordeel de moleculaire geometrie
Evalueer ten slotte de algehele vorm van het molecuul. Symmetrische arrangementen kunnen individuele dipoolmomenten opheffen, waardoor het hele molecuul niet-polair wordt, zelfs als de samenstellende atomen polair zijn. CO₂ is bijvoorbeeld lineair en niet-polair omdat de twee polaire bindingen spiegelbeelden zijn. Asymmetrische moleculen, zoals water (H₂O), bezitten een netto dipoolmoment en worden als polair geclassificeerd. Deze stap is cruciaal voor het voorspellen van de fysische eigenschappen van de stof.
Deze principes zijn fundamenteel in het scheikundeonderwijs en worden door wetenschappers gebruikt om de reactiviteit, oplosbaarheid en andere belangrijke kenmerken van verbindingen te voorspellen.
 Krachtcentrales aangedreven door licht
Krachtcentrales aangedreven door licht Ambtenaren en kiezers tonen zich na presentaties voor kinderen meer bezorgd over het afval in de oceaan
Ambtenaren en kiezers tonen zich na presentaties voor kinderen meer bezorgd over het afval in de oceaan  Reinigen zonder te schrobben en chemicaliën te gebruiken. Wetenschappers ontwikkelen zelfreinigend aluminium oppervlak
Reinigen zonder te schrobben en chemicaliën te gebruiken. Wetenschappers ontwikkelen zelfreinigend aluminium oppervlak Wat zijn enkele zichtbare gassen?
Wat zijn enkele zichtbare gassen?  Hoe vormen chemische rotsen zich?
Hoe vormen chemische rotsen zich?
 Wanneer magma vulkaanuitbarstingen voorkomt
Wanneer magma vulkaanuitbarstingen voorkomt Een schip uit de Tweede Wereldoorlog, aangemeerd in Alameda, wordt een testinstrument om de opwarming van de aarde tegen te gaan
Een schip uit de Tweede Wereldoorlog, aangemeerd in Alameda, wordt een testinstrument om de opwarming van de aarde tegen te gaan  Onderzoek toont aan dat bosbehoud een krachtig hulpmiddel is om de voeding in ontwikkelingslanden te verbeteren
Onderzoek toont aan dat bosbehoud een krachtig hulpmiddel is om de voeding in ontwikkelingslanden te verbeteren Wat zijn de top 10 moeilijkste bossen op aarde?
Wat zijn de top 10 moeilijkste bossen op aarde?  Hoe beïnvloedt zoutgehalte oceanenstromen?
Hoe beïnvloedt zoutgehalte oceanenstromen?
Hoofdlijnen
- Wat bevat erfelijke informatie?
- Onder de microscoop gespot:hoe een virus zijn pantser aantrekt
- Hoe kan moleculair bewijs aantonen hoe nauw verwante soorten elkaar zijn?
- Veranderen welke niveaus van structurele organisatie de functie van een eiwit kunnen veranderen?
- Wat is de kleinste eenheid van een organisme dat een specifieke functie heeft?
- Je hoeft geen schattige koala te zijn om een Instagram-beïnvloeder te zijn. Geef hagedissen en insecten een kans
- Wat houdt de cellen bij elkaar?
- Wie is de wetenschapper die een systeem heeft verlaten om organismen te classificeren op basis van hun fysieke en structurele overeenkomsten?
- Hoe kunnen cellen hetzelfde DNA hebben?
- Wat onthullen subscripts in chemische formules?

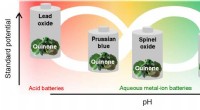
- Goedkoop organisch materiaal geeft veilige batterijen een langere levensduur
- Hi-res afbeelding van structuur van het oorsprongherkenningscomplex gebonden aan DNA onthuld
- IJsbestendige coating voor grote constructies is afhankelijk van een prachtige demonstratie van mechanica

- Hoe u nauwkeurig de pH van een mengsel van twee chemicaliën kunt berekenen

 Waarom heeft de mens zuurstof nodig om te kunnen leven?
Waarom heeft de mens zuurstof nodig om te kunnen leven?  Waarom heeft ecologie een interdicinaire wetenschap beschouwd?
Waarom heeft ecologie een interdicinaire wetenschap beschouwd?  Welke moleculaire vaste stof zou het hoogste smeltpunt hebben?
Welke moleculaire vaste stof zou het hoogste smeltpunt hebben?  Wat is het punt op aardoppervlak dat direct boven waar aardbeving begint?
Wat is het punt op aardoppervlak dat direct boven waar aardbeving begint?  In de wereld van schoonheidswedstrijden van een miljoen dollar - voor kamelen
In de wereld van schoonheidswedstrijden van een miljoen dollar - voor kamelen Wat zijn de voor- en nadelen van P-fenyleendiamine?
Wat zijn de voor- en nadelen van P-fenyleendiamine?  Welke energietransformaties komen voor in een ventilator?
Welke energietransformaties komen voor in een ventilator?  Revolutionaire benadering van het opslaan en gebruiken van koolstof, en de indrukwekkende inspanning die nodig is om dit te bereiken
Revolutionaire benadering van het opslaan en gebruiken van koolstof, en de indrukwekkende inspanning die nodig is om dit te bereiken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

