
Wetenschap
Een oververzadigde oplossing creëren:een stapsgewijze handleiding
Wat is een verzadigde oplossing?
De unieke polariteit van water – twee waterstofatomen gebonden aan een groter, negatief geladen zuurstofatoom – creëert een netto dipool die het mogelijk maakt waterstofbruggen te vormen met zichzelf en met opgeloste moleculen.
Wanneer een opgeloste stof zoals suiker of zout wordt toegevoegd, omringen watermoleculen de opgeloste deeltjes en trekken ze uit elkaar. Naarmate er meer opgeloste stof wordt toegevoegd, bereikt het water uiteindelijk een punt waarop alle beschikbare locaties bezet zijn; op dat moment is de oplossing verzadigd.
Een oververzadigde oplossing creëren
Om het verzadigingspunt te overschrijden, verwarmt u het oplosmiddel tot bijna de kooktemperatuur. De verhoogde kinetische energie breidt de ruimtes tussen watermoleculen uit, waardoor extra opgeloste stoffen oplossen. Blijf de opgeloste stof al roerend toevoegen totdat er geen oplossing meer is, ook al is het verzadigingspunt overschreden.
Verwijder het vuur en laat de oplossing langzaam afkoelen. De overtollige opgeloste stof blijft korte tijd opgelost en vormt een metastabiele, oververzadigde oplossing die bij verstoring zeer gevoelig is voor kristallisatie.
Heet ijs, rotssnoepjes en kristalgroei
Eén klassieke demonstratie maakt gebruik van natriumacetaat. Een oververzadigde natriumacetaatoplossing kan onmiddellijk tot kristallisatie worden gebracht door een enkel entkristal te introduceren, waardoor ‘heet ijs’ ontstaat:ijsachtige kristallen die tegelijkertijd warmte afgeven.
Op dezelfde manier kan een hete suikeroplossing worden gekoeld terwijl er een touwtje of naald in hangt. Na verloop van tijd hopen suikermoleculen zich op aan het oppervlak en vormen een groot, eetbaar kristal, algemeen bekend als rock candy. Geniet op een verantwoorde manier en vergeet niet om een goede mondhygiëne te handhaven, aangezien overmatige suikerconsumptie tot gaatjes kan leiden.
 Video:Waarom stinkende kazen stinken
Video:Waarom stinkende kazen stinken  Welke volgorde toont de vorm van water uit de koudste tot de heetste temperaturen?
Welke volgorde toont de vorm van water uit de koudste tot de heetste temperaturen?  Hoe meet je de snelheid waarmee waterstofperoxide wordt afgebroken?
Hoe meet je de snelheid waarmee waterstofperoxide wordt afgebroken?  Waar dissocieert azijnzuur in?
Waar dissocieert azijnzuur in?  Huid verantwoordelijk voor grotere blootstelling aan kankerverwekkende stoffen in barbecuerook dan longen
Huid verantwoordelijk voor grotere blootstelling aan kankerverwekkende stoffen in barbecuerook dan longen
 Heeft de klimaatverandering de menselijke evolutie bepaald?
Heeft de klimaatverandering de menselijke evolutie bepaald?  Westerse staten verzetten zich tegen plan om Amerikaans reservoirwater in rekening te brengen
Westerse staten verzetten zich tegen plan om Amerikaans reservoirwater in rekening te brengen Hoe woestijnvorming en droogte thuis en onderweg te bestrijden?
Hoe woestijnvorming en droogte thuis en onderweg te bestrijden? Onderzoek naar microben belicht de toxiciteit van de Groenlandse ijskap
Onderzoek naar microben belicht de toxiciteit van de Groenlandse ijskap Inleiding tot zonne-airconditioners
Inleiding tot zonne-airconditioners
Hoofdlijnen
- Wanneer dode planten en dieren uiteenvallen, wat gebeurt er dan met de kwestie waar het van heeft gemaakt?
- Waarom Biome beschouwd als een open systeem?
- Studie onderzoekt wat we weten over hoe neonicotinoïden bijen beïnvloeden
- Wat is een voorbeeld van culturele evolutie?
- Welke van de volgende organismen zijn het nauwst gerelateerd aan ursus arctos en maritimus bfelis ursus cfelis felis dursus felis felis?
- Kan een veel gecellig organisme vanzelf bewegen?
- Eukaryotische cellen:structuur, functie en belangrijkste organellen uitgelegd
- Onderzoekers bieden visserij een oplossing voor overbevissing
- Wat is een product in de biologie?
- Een type semi-transparant polymeer dat bij kamertemperatuur kan worden hersteld met een kleine druk

- Doorbraak in actinide metaal-metaal binding
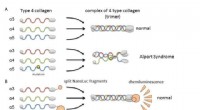
- Een zeer gevoelig en multi-analytisch systeem voor erfelijke nierziekte
- Wat gebeurt er als calcium 6M zoutzuur ontmoet? Een uitgebreide gids

- Waarom wordt een zilveren ketting zwart? De oorzaken en preventie begrijpen

 Waarom is het belangrijk dat water veel warmte kan absorberen?
Waarom is het belangrijk dat water veel warmte kan absorberen?  Is een volle maan zichtbaar van de aarde overdag of 's nachts?
Is een volle maan zichtbaar van de aarde overdag of 's nachts?  Nieuw geïdentificeerd jetstreampatroon kan de wereldwijde voedselvoorziening in gevaar brengen, zegt studie
Nieuw geïdentificeerd jetstreampatroon kan de wereldwijde voedselvoorziening in gevaar brengen, zegt studie Waar bevindt de aarde zich in de Melkweg?
Waar bevindt de aarde zich in de Melkweg?  Wat is de volgorde van uitlijning tijdens een zonsverduistering op weg naar het randsysteem?
Wat is de volgorde van uitlijning tijdens een zonsverduistering op weg naar het randsysteem?  Wat is de meest fundamentele fysieke wetenschappen?
Wat is de meest fundamentele fysieke wetenschappen?  Welke structuren worden door cellen gebruikt voor beweging?
Welke structuren worden door cellen gebruikt voor beweging?  Onderzoekers optimaliseren het 3D-printen van optisch actieve nanostructuren
Onderzoekers optimaliseren het 3D-printen van optisch actieve nanostructuren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

