
Wetenschap
Covalente bindingen begrijpen:hoe atomen elektronen delen
Wittayayut/iStock/GettyImages
Wat is een covalente binding?
Een covalente binding wordt gevormd wanneer twee of meer niet-metaalatomen een of meer paren valentie-elektronen delen, waardoor een stabiele, gerichte verbinding ontstaat. Het verbreken van een dergelijke binding vergt aanzienlijke energie (doorgaans tussen de 50 en 200 kcal/mol), wat de kracht en de stabiliteit weerspiegelt die het aan het molecuul verleent.
Belangrijkste kenmerken van covalente obligaties
• Alleen niet-metalen (of metalloïden) met vergelijkbare elektronegativiteiten vormen covalente verbindingen.
• Elektronen worden gedeeld binnen de buitenste schillen, waardoor de atomen een vaste ruimtelijke oriëntatie krijgen.
• Polariteit hangt af van verschillen in elektronegativiteit:gelijk delen levert een niet-polaire covalente binding op; ongelijk delen produceert een polaire covalente binding.
• Vanwege de lage polariteit en de sterke directionele aard hebben moleculen met covalente bindingen vaak lage smelt- en kookpunten, waardoor ze bij kamertemperatuur gassen of vloeistoffen blijven.
Veelvoorkomende voorbeelden van covalente moleculen
• Methaan (CH4 ) – een niet-polair molecuul waarin koolstof vier equivalente elektronenparen deelt met waterstof.
• Zoutzuur (HCl) – een polaire covalente binding; de hogere elektronegativiteit van chloor trekt het gedeelde paar naar zich toe.
• Water (H2 O) – een klassiek polair covalent molecuul; De sterkere aantrekkingskracht van zuurstof creëert een dipoolmoment, waardoor water zijn unieke eigenschappen krijgt.
• Ammoniak (NH3 ) – een polaire covalente verbinding met een trigonale piramidale geometrie.
Contrast met ionische bindingen
Bij een ionische binding doneert een metaal een of meer elektronen aan een niet-metaal, waardoor tegengesteld geladen ionen ontstaan die elkaar aantrekken. Alledaagse voorbeelden zijn tafelzout (NaCl), fluoridetandpasta (NaF), roest (Fe2 O3 ), en maagzuurremmer calciumhydroxide (Ca(OH)2 ).
 Wat zijn de laboratoriumapparaten die van porselein zijn gemaakt?
Wat zijn de laboratoriumapparaten die van porselein zijn gemaakt?  Wat zijn enkele voorbeelden van pure oplossingen?
Wat zijn enkele voorbeelden van pure oplossingen?  Zeer efficiënt, duurzame elektrokatalysator om de productie van waterstofbrandstof te stimuleren
Zeer efficiënt, duurzame elektrokatalysator om de productie van waterstofbrandstof te stimuleren Onconventioneel oplossingsproces voor 2-D heterostructuur
Onconventioneel oplossingsproces voor 2-D heterostructuur Afstembaar emissief organisch platform
Afstembaar emissief organisch platform
Hoofdlijnen
- Onderzoekers krijgen inzicht in hoe ultrakleine bacteriën uit de omgeving zich hebben aangepast om in mensen te leven
- Waar kwamen de eerste suikers vandaan?
- Wat zijn de vier theorieën over ziekteveroorzaak?
- Wie ontdekte biotechnologie?
- Waarom fantastische sprookjesachtige samenlevingen net zo complex kunnen zijn als de onze
- Breng cellen het grootste deel van hun leven door in interfase?
- Biologen leren hoe planten hun groeihormoon auxine synthetiseren
- Wat is Agrobacterium gemedieerde genoverdracht?
- Welk aspect van de celfunctie omvat het verplaatsen van stoffen en signalen tussen organellen?
- Samenwerking vormt de strategie voor het vasthouden van extracellulaire blaasjes
- Duurzaam leer, garen en papier—van broodetende schimmels

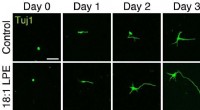
- Oleoyl-LPE oefent neurietstimulatie en neuroprotectie uit
- Ontdekking van levensverlengingspad in wormen toont nieuwe manier om veroudering te bestuderen
- De ontwikkeling van laagdimensionale nanomaterialen kan een revolutie teweegbrengen in toekomstige technologieën
 Wat is BWR van kernenergie?
Wat is BWR van kernenergie?  Hoe heet het object dat thermische energie en elektriciteit geleidt?
Hoe heet het object dat thermische energie en elektriciteit geleidt?  Welke geografische kenmerken worden niet gevonden in India 1. Lagoon 2. Glacier 3. Iceberg 4. Desert?
Welke geografische kenmerken worden niet gevonden in India 1. Lagoon 2. Glacier 3. Iceberg 4. Desert?  Gefossiliseerde schelpen vertonen tekenen van verzuring van de oceaan vóór dinosaurusvernietigende asteroïde
Gefossiliseerde schelpen vertonen tekenen van verzuring van de oceaan vóór dinosaurusvernietigende asteroïde Als draken echt zouden bestaan, zouden ze dan vuur kunnen spuwen?
Als draken echt zouden bestaan, zouden ze dan vuur kunnen spuwen?  Nieuwe techniek kan medicijnontwerp stroomlijnen
Nieuwe techniek kan medicijnontwerp stroomlijnen Is Lyft te vriendelijk om tegen Uber te vechten?
Is Lyft te vriendelijk om tegen Uber te vechten?  Onderzoek toont aan hoe het lichaam een reeks warme temperaturen waarneemt
Onderzoek toont aan hoe het lichaam een reeks warme temperaturen waarneemt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

