
Wetenschap
Berekening van de katalytische efficiëntie van enzymen:een praktische gids
Door Kevin Beck
Bijgewerkt op 30 augustus 2022
Enzymen zijn biologische katalysatoren die reacties versnellen door de activeringsenergie te verlagen zonder de thermodynamica van de reactanten of producten te veranderen. Hun opmerkelijke specificiteit – vaak vergeleken met een slot-en-sleutelmechanisme – maakt ze onmisbaar in zowel de fysiologie als de biotechnologie. Begrijpen hoe efficiënt een enzym zijn werk uitvoert, is essentieel voor de ontwikkeling van geneesmiddelen, metabolische engineering en diagnostische tests.
Basisprincipes van enzymen
Elk enzym is een uniek eiwit dat bestaat uit een reeks aminozuren. De actieve plaats, gevormd door specifieke residuen, bindt een enkel substraatmolecuul (de “sleutel”) en vergemakkelijkt de omzetting ervan in een product. Omdat enzymen bij de reactie niet worden verbruikt, kunnen ze herhaaldelijk nieuwe substraatmoleculen binden, waardoor een enzym-substraatcomplex ontstaat dat uiteindelijk het product vrijgeeft.
Enzymkinetiek
De katalytische cyclus kan worden weergegeven als:
E + S ⇔ ES → E + P
Hier, E is het enzym, S het substraat, ES het enzym-substraatcomplex, en P het product. De omkeerbare vorming van ES weerspiegelt het dynamische evenwicht tussen binding en dissociatie, terwijl de omzetting in product effectief onomkeerbaar is onder fysiologische omstandigheden.
Snelheidsconstanten
Drie elementaire stappen bepalen de reactie:
- Bindend:E + S → ES met snelheidsconstante k1
- Dissociatie:ES → E + S met snelheidsconstante k-1
- Katalyse:ES → E + P met snelheidsconstante k2 (kkat )
De Michaelis-constante en enzymefficiëntie
Onder stabiele omstandigheden is de snelheid van productvorming (snelheid, v ) is:
v =k2 [ES]
Vanwege de vorming en afbraak van ES in evenwicht zijn, hebben we:
k1 [E][S] =k2 [ES] + k-1 [ES]
Herschikken levert de Michaelis-constante op, KM =(k2 + k-1 )/k1 :
[E][S] =KM [ES]
Vervanging in de snelheidsvergelijking levert de bekende Michaelis-Menten-vorm op:
v =(k2 /KM )·[E][S]
De verhouding k2 /KM wordt de specificiteit of kinetische efficiëntieconstante genoemd. Het omvat zowel de katalytische omloopsnelheid als de affiniteit voor substraat, waardoor één enkele maatstaf wordt geboden voor het vergelijken van enzymen onder identieke omstandigheden.
Om deze efficiëntie uit experimentele gegevens te berekenen, herschikt u de vergelijking:
k2 /KM =v / ([E][S])
Door de reactiesnelheid (v ), enzymconcentratie ([E] ), en substraatconcentratie ([S] ), kunnen onderzoekers kwantificeren hoe effectief een enzym substraat omzet in een product, waardoor de selectie van enzymen in industriële processen wordt begeleid en het ontwerp van therapeutische enzymen wordt geïnformeerd.
 Wat is een kleurstof die chemisch reageert met zuren en basis om één kleur in zure basen te produceren?
Wat is een kleurstof die chemisch reageert met zuren en basis om één kleur in zure basen te produceren?  Voorbeelden van verdamping en destillatie
Voorbeelden van verdamping en destillatie  Hoe vormen en interageren watermoleculen?
Hoe vormen en interageren watermoleculen?  Is H2O een formule die niet -polair molecuul vertegenwoordigt?
Is H2O een formule die niet -polair molecuul vertegenwoordigt?  Onderzoekers lossen een wetenschappelijk mysterie over verdamping op
Onderzoekers lossen een wetenschappelijk mysterie over verdamping op
 Geofysische waarnemingen onthullen de waterverdeling en het effect in de aardmantel
Geofysische waarnemingen onthullen de waterverdeling en het effect in de aardmantel Waarom zijn ondiepe meren gevoelig voor eutrofiëring?
Waarom zijn ondiepe meren gevoelig voor eutrofiëring?  Scheuren luiden het afkalven van een grote ijsberg van de Petermann-gletsjer in
Scheuren luiden het afkalven van een grote ijsberg van de Petermann-gletsjer in Een wolkenloze toekomst? Het mysterie in het hart van klimaatvoorspellingen
Een wolkenloze toekomst? Het mysterie in het hart van klimaatvoorspellingen Wetenschapsprojecten op slangen
Wetenschapsprojecten op slangen
Hoofdlijnen
- Hoe Candida albicans zuurstofgebrek exploiteert om ziekten te veroorzaken
- Vergelijk en contrasteer de structuur van gistalgen.
- Waarom is mitose belangrijk voor eukaryotische organismen?
- Voorbereiden op toekomstige coronavirusvarianten met behulp van kunstmatige intelligentie
- Planten kunnen de intensiteit van zoutstress meten
- Een term die een losjes gebreide associatie van cellen beschrijft?
- Wie stelde voor dat verworven eigenschappen konden worden doorgegeven aan een nakomelingen van organismen?
- Wat zijn de vier stappen van theorie -evolutie?
- Wie patenteert wiens genoom?
- Hoe technologie die is ontworpen voor de ruimte, kan helpen bij het opsporen van ziekten op planeet Aarde

- De lengte van een gebogen lijn (boog) berekenen - een praktische gids

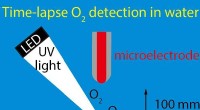
- Snellere detectie van door fotokatalysatoren gegenereerde zuurstof heeft grote gevolgen voor schone energie
- Nieuwe materialen en processen om pathogene micro-organismen uit water te verwijderen
- Calciumchloride veilig oplossen:een praktische stap-voor-stap handleiding

 Hoe werkt de biosfeer?
Hoe werkt de biosfeer?  Zijn deeltjes van materie altijd in beweging?
Zijn deeltjes van materie altijd in beweging?  Doet de reactie natriumbromide en zoutzuur op?
Doet de reactie natriumbromide en zoutzuur op?  De kleur met de golflengte is?
De kleur met de golflengte is?  Hoe is het land in Mexico City?
Hoe is het land in Mexico City?  Welke drie dingen hebben planten nodig om fotosynthese te gebeuren?
Welke drie dingen hebben planten nodig om fotosynthese te gebeuren?  Decimalen omzetten in gemengde getallen:een stapsgewijze handleiding
Decimalen omzetten in gemengde getallen:een stapsgewijze handleiding  Kunnen we onze organen klonen voor gebruik bij een transplantatie?
Kunnen we onze organen klonen voor gebruik bij een transplantatie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

