
Wetenschap
Soorten metalen op het periodiek systeem:een expertoverzicht
Door Kevin Beck, bijgewerkt op 30 augustus 2022
Eyematrix/iStock/GettyImages
Wat zijn elementen?
In de scheikunde een element is een stof die bestaat uit atomen die allemaal hetzelfde aantal protonen bevatten. Een element kan niet met conventionele chemische methoden in eenvoudiger stoffen worden opgesplitst. Sinds 2018 hebben wetenschappers 92 natuurlijk voorkomende elementen bevestigd, plus 11 synthetische isotopen die alleen onder laboratoriumomstandigheden voorkomen. Elk element bestaat onder standaardomstandigheden in een van de drie fysieke toestanden:vast, vloeibaar of gasvormig.
Atomen zijn kleine clusters van protonen, neutronen en elektronen. Waterstof, de eenvoudigste, bevat één proton en één elektron, terwijl de meest voorkomende isotoop van uranium 92 protonen, 92 elektronen en 146 neutronen heeft. Protonen hebben een positieve lading; elektronen hebben een gelijke negatieve lading; neutronen zijn neutraal. De balans tussen protonen en elektronen bepaalt de identiteit van een element, terwijl variaties in het aantal neutronen isotopen voortbrengen.
Het periodiek systeem der elementen
Het periodiek systeem is de hoeksteen van de moderne scheikunde, waarbij alle bekende elementen zijn gerangschikt op oplopend atoomnummer:het aantal protonen in de kern. Deze ordening onthult zich herhalende patronen van chemisch gedrag, vandaar de naam ‘periodiek’. Hoewel de tabel 113 vermeldingen bevat (118 vanaf 2023), zijn de elementen gegroepeerd in families die gedeelde eigenschappen weerspiegelen.
Wanneer u de tabel bekijkt, zult u merken dat de bovenste rijen hiaten bevatten; dit zijn elementen die nog niet zijn ontdekt of gesynthetiseerd. De lay-out bevat kolommen (groepen) en rijen (punten) die de elektronenconfiguratie en reactiviteit weerspiegelen.
Periodieke Tabelgroepen
Historisch gezien zijn elementen onderverdeeld in drie brede categorieën:metalen, niet-metalen en metalloïden. Niet-metalen zijn beperkt tot zeven kernelementen:waterstof (H), koolstof (C), stikstof (N), zuurstof (O), fosfor (P), zwavel (S) en selenium (Se). Bijkomende niet-metaalfamilies omvatten de halogenen (F, Cl, Br, I, At) en de edelgassen (He, Ne, Ar, Kr, Xe, Ra). Metalloïden, zoals silicium en arseen, vertonen tussenliggende kenmerken.
Kenmerken van metalen
Van de 113 elementen worden er 88 geclassificeerd als metalen. Ondanks hun diversiteit hebben metalen verschillende kenmerkende eigenschappen gemeen:
- Vast bij kamertemperatuur (behalve kwik, een vloeibaar metaal dat van oudsher in thermometers werd gebruikt).
- Glans —een glanzend oppervlak dat licht reflecteert, wat bijdraagt aan de esthetische en economische waarde ervan.
- Maakbaarheid —het vermogen om tot dunne platen te worden gehamerd of gerold zonder te barsten.
- Ductiliteit —het vermogen om in draden te worden getrokken, een belangrijke eigenschap voor elektrische en thermische geleiders.
- Hoge dichtheid —de meeste metalen hebben een hoge massa per volume-eenheid.
- Verhoogde smelt- en kookpunten —Het smeltpunt van wolfraam is bijvoorbeeld 3422°C, waardoor het onmisbaar is voor de gloeidraden van gloeilampen.
Soorten metalen
Metalen worden verder onderverdeeld in vijf hoofdgroepen:
- Alkalimetalen (zes elementen in groepIA:Li, Na, K, Rb, Cs, Fr).
- Aardalkalimetalen (zes elementen in groepIIA:Be, Mg, Ca, Sr, Ba, Ra).
- Overgangsmetalen (veertig elementen verspreid over groepenIIIB–XII, rijen3–6).
- Lanthaniden (elementen 58–71, ook bekend als zeldzame aardmetalen).
- Actiniden (elementen 90–103, een subset van de familie van zeldzame aardmetalen).
- Niet-gespecificeerde metalen (acht elementen die niet netjes in de bovenstaande categorieën passen).
Als je deze groepen bij elkaar optelt, krijg je een totaal van 88 metalen:6 alkali + 6 aardalkalimetalen + 40 overgangsmetalen + 28 zeldzame aardmetalen + 8 niet gespecificeerd.
Metalloïden en niet-metalen
Metalloïden bezetten een niche tussen metalen en niet-metalen en combineren geleidende eigenschappen met halfgeleidergedrag. De zeven veel voorkomende metalloïden zijn:
- Boor (B)
- Silicium (Si)
- Germaan (Ge)
- Arseen (As)
- Antimoon (Sb)
- Tellurium (Te)
- Polonium (Po)
Deze elementen zijn vast bij kamertemperatuur en spelen een cruciale rol in moderne elektronica, waarbij ze vaak legeringen vormen met metalen elementen om de elektrische en thermische eigenschappen aan te passen.
Bezoek onze bronnenpagina voor een interactieve verkenning van het periodiek systeem .
Belangrijkste punten
- Metalen omvatten de meerderheid van de elementen, met 88 van de 113 op het periodiek systeem.
- Ze worden gekenmerkt door glans, kneedbaarheid, ductiliteit, dichtheid en hoge smeltpunten.
- De primaire metaalfamilies (alkali, aardalkalimetaal, transitie, lanthanide en actinide) vertonen elk verschillend chemisch gedrag.
- Metalloïden overbruggen de kloof tussen metalen en niet-metalen en vormen de basis van de halfgeleidertechnologie.
 Wat te tekenen voor een element in de wetenschap?
Wat te tekenen voor een element in de wetenschap?  Koraalskeletten fungeren als archief van woestijnomstandigheden uit Little Ice Age
Koraalskeletten fungeren als archief van woestijnomstandigheden uit Little Ice Age Science Fair Project voor het testen van verschillende bodems met plantengroei
Science Fair Project voor het testen van verschillende bodems met plantengroei Europese steden hebben meer juridische flexibiliteit nodig om inwoners voor te bereiden en te beschermen tegen de klimaatnoodsituatie, waarschuwt studie
Europese steden hebben meer juridische flexibiliteit nodig om inwoners voor te bereiden en te beschermen tegen de klimaatnoodsituatie, waarschuwt studie Welk eten produceren bomen?
Welk eten produceren bomen?
Hoofdlijnen
- Een fylogenetische boom die is geworteld?
- Wat zijn de leefgebieden van de zes koninkrijken?
- Nieuwe inzichten in hoe epilancine 15X bacteriën doodt
- Wat is een bio -engineer?
- Wat zijn Biomes?
- Welke cel wordt gebruikt om licht te vangen tijdens fotosynthese?
- Waarom zijn bacteriën belangrijk voor de stikstofcyclus?
- Welke twee factoren zijn abiotische beperkende beperkende die van invloed zijn op organismen in mariene biomen?
- Wat omsluit de mitochondria?
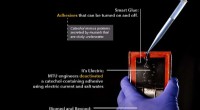
- Ingenieurs zappen en maken onderwater slimme lijm los
- Welke producten ontstaan bij het mengen van een zuur met een base? Een gedetailleerde gids voor neutralisatie

- Bedrieglijk eenvoudig proces kan de recycling van kunststoffen stimuleren

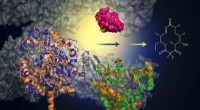
- Wetenschappers ontwikkelen groenere, efficiëntere methode om antibiotica van de volgende generatie te produceren
- Het voorspellen van chemische reactieproducten:een praktische gids

 Wat wordt potentiële energie omgezet als water over een waterval loopt?
Wat wordt potentiële energie omgezet als water over een waterval loopt?  Wat was de Heinrich -methode om talen te leren?
Wat was de Heinrich -methode om talen te leren?  Minstens 265 doden bij overstromingen, aardverschuivingen als regens Oost-Afrika teisteren
Minstens 265 doden bij overstromingen, aardverschuivingen als regens Oost-Afrika teisteren Bevatten radiogolven de minste hoeveelheid energie?
Bevatten radiogolven de minste hoeveelheid energie?  De betekenis van de Death Tarot-kaart ontdekken
De betekenis van de Death Tarot-kaart ontdekken  Ken je die 'regen'-geur? Het kan wetenschappers helpen bestuderen hoe geur gedrag beïnvloedt
Ken je die 'regen'-geur? Het kan wetenschappers helpen bestuderen hoe geur gedrag beïnvloedt  Wat zijn de belangrijkste natuurlijke kenmerken van Malawi?
Wat zijn de belangrijkste natuurlijke kenmerken van Malawi?  BuzzFeed gaat 15% van zijn werknemers schrappen:rapporten
BuzzFeed gaat 15% van zijn werknemers schrappen:rapporten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

