
Wetenschap
Molariteit uitgelegd:definitie, berekening en praktische voorbeelden
Door Michael Merijn
Bijgewerkt op 30 augustus 2022
Hinterhaus Productions/DigitalVision/GettyImages
Concentratie in de scheikunde begrijpen
Bij chemisch werk is het essentieel om te weten hoeveel van een stof is opgelost in een bepaald volume oplossing. Deze meting staat bekend als concentratie, en molariteit is de meest gebruikte eenheid om deze uit te drukken. Molariteit komt perfect overeen met stoichiometrische berekeningen omdat reactanten combineren in molaire verhoudingen van gehele getallen. Bij de reactie 2H₂ + O₂ → 2H₂O gaat het bijvoorbeeld om 2 mol waterstofgas dat reageert met 1 mol zuurstofgas, waardoor 2 mol water ontstaat.
De Mol:een teleenheid voor atomen en moleculen
Een mol wordt gedefinieerd als de hoeveelheid van een stof die precies 6,022×10²³ elementaire entiteiten bevat:atomen, moleculen, ionen of andere deeltjes. Deze waarde, bekend als het getal van Avogadro, werd internationaal overeengekomen op basis van het aantal atomen in 12 g van de koolstof-12-isotoop. Het gebruik van deze teleenheid vereenvoudigt massaberekeningen:1 mol zuurstof weegt 16,00 g, 1 mol water 18,02 g en 1 mol kooldioxide 44,01 g.
Wat is molariteit?
Molariteit, aangegeven met het symbool M, is het aantal mol opgeloste stof opgelost in één liter oplossing. Het verschilt van molaliteit, die het aantal mol opgeloste stof per kilogram oplosmiddel uitdrukt. Molariteit heeft de voorkeur in laboratoriumomgevingen omdat deze rechtstreeks verband houdt met het volume van de oplossing die in reacties wordt gebruikt.
Molariteit berekenen:een stapsgewijs voorbeeld
Stel dat u de molariteit nodig heeft van een oplossing die 100 g natriumchloride (NaCl) bevat in 2,5 liter oplossing.
Stap 1:Bepaal het formulegewicht van NaCl.
Na (22,99 g/mol) + Cl (35,45 g/mol) =58,44 g/mol.
Stap 2:Vind het aantal mol NaCl.
100g ÷ 58,44g/mol =1,71mol.
Stap 3:Bereken de molariteit.
1,71mol ÷ 2,5L =0,684M.
Een oplossing met een gewenste molariteit voorbereiden
Hoeveel natriumsulfaat (Na₂SO₄) is nodig om 250 ml van een 0,5 M oplossing te maken?
Stap 1:Bereken de benodigde moedervlekken.
0,25L × 0,5mol/L =0,125mol.
Stap 2:Bereken het formulegewicht van Na₂SO₄.
2Na (22,99 g/mol × 2) + S (32,07 g/mol) + 4O (16,00 g/mol × 4) =142,1 g/mol.
Stap 3:Bepaal de massa van Na₂SO₄.
0,125mol × 142,1g/mol =17,76g.
Deze eenvoudige berekeningen illustreren hoe molariteit een nauwkeurige bereiding en analyse van chemische oplossingen mogelijk maakt.
 Gemiddelde mensen kunnen het verschil maken bij mondiale uitdagingen, zegt onderzoeker
Gemiddelde mensen kunnen het verschil maken bij mondiale uitdagingen, zegt onderzoeker Australië ziet tweede jaar Barrier Reef bleken
Australië ziet tweede jaar Barrier Reef bleken Een beetje dieper graven:nieuwe studie onderzoekt de eigenschappen op nanoschaal van het Gulong-schalieoliereservoir
Een beetje dieper graven:nieuwe studie onderzoekt de eigenschappen op nanoschaal van het Gulong-schalieoliereservoir Klimaat:Kan 'Dr. Het idee van Strangelove een optie zijn?
Klimaat:Kan 'Dr. Het idee van Strangelove een optie zijn?  Waarom heeft de wetenschap meer kwaad dan goed gedaan?
Waarom heeft de wetenschap meer kwaad dan goed gedaan?
Hoofdlijnen
- Zijn linkshandigen snellere denkers dan rechtshandigen?
- Wat is een eigenschap die wordt bestuurd door een enkel gen met twee allelen?
- Geef een voorbeeld van organisme en zijn niche?
- Waarom zijn er wel hoppende muizen in Australië, maar geen kangoeroes in Azië? Het is een lang verhaal
- Wat is de naam van polysacharide die gevonden in celwanden schimmels en exoskeletten geleedpotigen?
- Welke stof is gemaakt van suikers en peptiden gevonden in de cel Eubacteriën?
- De wetenschap van het verbeteren van erfelijke kwaliteiten staat bekend als?
- Wat is belangrijk aan de DNA -sequenties van belangrijke archeaberiale genen?
- Draagt man het A -dominaatgen?
- Een computersysteem dat chemisch afval analyseert en manieren voorstelt om er nieuwe producten van te maken
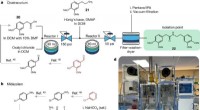
- Chemici maken harde kunststoffen recyclebaar

- Vliegen injecteren met slakkengif kan ons helpen moleculen te ontdekken voor het ontwikkelen van nieuwe medicijnen

- Membraantechnologie kan emissies en energieverbruik bij olieraffinage verminderen

- Het begrijpen van bederf- en kwaliteitsproblemen kan de Amerikaanse ambachtelijke kaasindustrie verbeteren

 Hoe zou je suikerwater classificeren?
Hoe zou je suikerwater classificeren?  Zijn moleculen samengevoegd om elementen te vormen?
Zijn moleculen samengevoegd om elementen te vormen?  Duidelijke verschillen in hoe Noordse journalisten hun professionele rol en externe invloed ervaren
Duidelijke verschillen in hoe Noordse journalisten hun professionele rol en externe invloed ervaren Energie die niet wordt omgezet in nuttige energie die wordt afgegeven als?
Energie die niet wordt omgezet in nuttige energie die wordt afgegeven als?  Wat zijn de twee belangrijkste componenten van de atmosfeer van de aarde?
Wat zijn de twee belangrijkste componenten van de atmosfeer van de aarde?  De energie die nodig is om twee atomen volledig te dissociëren die covalent samengevoegd zijn, wordt opgeroepen?
De energie die nodig is om twee atomen volledig te dissociëren die covalent samengevoegd zijn, wordt opgeroepen?  Welk woord is de beschrijving van helderheidslicht?
Welk woord is de beschrijving van helderheidslicht?  Tijdmachinesimulaties gemaakt om de levenscyclus van clusters van voorouderlijke melkwegstelsels te bestuderen
Tijdmachinesimulaties gemaakt om de levenscyclus van clusters van voorouderlijke melkwegstelsels te bestuderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

