
Wetenschap
Hoe u het aantal mollen in een chemische reactie kunt berekenen – stapsgewijze handleiding
Door Kylene Arnold – Bijgewerkt 30 augustus 2022
TL;DR
Om het aantal mol in een reactie te bepalen, converteert u alle massa's van de reactanten naar grammen, berekent u de molaire massa van elke verbinding, deelt u de grammen door de molaire massa en gebruikt u de stoichiometrische coëfficiënten om de beperkende reagens- en productopbrengsten te vinden.
1. Reagensmassa's omrekenen naar gram
Begin met het uitdrukken van de massa van elke reactant in grammen. 0,05 kg natrium (Na) is bijvoorbeeld gelijk aan 50,0 g (0,05 kg x 1000 g/kg). In het natriumchloorvoorbeeld hebben we 50,0 gNa en 25.000 gCl₂.
2. Atoomgewichten bepalen
Haal het atoomgewicht van elk element op uit het periodiek systeem (uitgedrukt in atomaire massa-eenheden, amu). Na = 22.990 amu, Cl = 35.453 amu.
3. Bereken de molaire massa van reactanten en producten
Tel de atoomgewichten van alle atomen in elke verbinding bij elkaar op om de molaire massa (gmol⁻¹) te verkrijgen. Bijvoorbeeld:
- Na:22,990 gmol⁻¹
- Cl₂:2×35,453 = 70,506 gmol⁻¹
- NaCl:22,990 + 35,453 = 58,443 gmol⁻¹
4. Converteer gram naar mol
Verdeel de massa van elke reactant door zijn molaire massa:
- Na:50,0 g÷22,990 gmol⁻¹ = 2,1749 mol
- Cl₂:25,000 g÷70,506 gmol⁻¹ = 0,3546 mol
5. Inspecteer de reactiecoëfficiënten
De uitgebalanceerde vergelijking is2 Na + Cl₂ → 2 NaCl. Coëfficiënten geven de molverhouding aan:2Na:1Cl₂:2NaCl.
6. Identificeer de beperkende reagens
Bereken hoeveel mol product elke reactant kan genereren met behulp van de stoichiometrische verhouding.
- Na → 2,1749 molNa ×(2NaCl/2Na) = 2,1749 molNaCl
- Cl₂ → 0,3546 molCl₂ ×(2NaCl/1Cl₂) = 0,7092 molNaCl
De kleinere waarde (0,7092 molNaCl) geeft aan dat Cl₂ de beperkende reactant is.
7. Bereken de maximale massa van het product
Vermenigvuldig het aantal mol product met de molaire massa:
- 0,7092 molNaCl × 58,443 gmol⁻¹ = 41,4 gNaCl
8. Controleer het resultaat
Voer een kruiscontrole uit door de massa te berekenen op basis van de Na-limiet:2,1749 molNaCl × 58,443 gmol⁻¹ =127,0 gNaCl. Omdat de uit Cl₂ afkomstige hoeveelheid kleiner is, produceert de reactie slechts ~41,4 g NaCl.
9. Bereken het uiteindelijke aantal mol product
Deel de productmassa door de molaire massa om de molmassa te bevestigen:
- 41,4 g÷58,443 gmol⁻¹ = 0,709 molNaCl
Veiligheidsopmerking
Natrium is zeer reactief; dit experiment mag alleen worden uitgevoerd in een gecontroleerde laboratoriumomgeving door getrainde professionals.
Voor gezaghebbende gegevens over de constante en molaire massaberekeningen van Avogadro, zie IUPAC en Wikipedia:Avogadro constante .
 De koloniale geschiedenis van de Marshalleilanden beperkt hun vermogen om zichzelf te redden van klimaatverandering
De koloniale geschiedenis van de Marshalleilanden beperkt hun vermogen om zichzelf te redden van klimaatverandering Mechanismemodellering voor betere voorspellingen, klimaatvoorspellingen
Mechanismemodellering voor betere voorspellingen, klimaatvoorspellingen Waterdamp afkomstig van verbranding kan de luchtkwaliteit in de winter verslechteren
Waterdamp afkomstig van verbranding kan de luchtkwaliteit in de winter verslechteren Onthulling van de rotte landbouwbedrijven in Brazilië
Onthulling van de rotte landbouwbedrijven in Brazilië Heeft de mens zichzelf gedomesticeerd?
Heeft de mens zichzelf gedomesticeerd?
Hoofdlijnen
- Bij-nabootsende kaalvleugelmot zoemt na 130 jaar weer tot leven
- Laat DNA de cellen weten wat eiwitten moeten maken?
- Wat is de naam van cel -eiwitten en een lipide dubbellaagse barrière?
- Welke term definieert vraag over wat mensen doen met de kennis in de biologie die niet kan worden beantwoord met behulp van de wetenschappelijke methode?
- Als een cel geen ribosomen heeft, wat kan hij dan doen?
- Celbioloog legt uit hoe RNA-virussen zichzelf kopiëren
- Wat zijn enkele voordelen van bioloog?
- Hoe voorspelbaar is evolutie?
- Wat is het biochemische bewijs dat de biologische evolutie ondersteunt?
- Herhalingssleutel tot zelfgenezing, flexibele medische hulpmiddelen

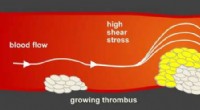
- Antiblokkeersysteem in slagaders beschermt tegen hartaanvallen
- Wetenschappers gebruiken gel-polymeer-elektrolyt voor hoogwaardige magnesiumbatterijen

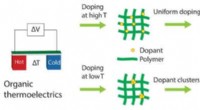
- Hoe restwarmte-energie op te vangen met verbeterde polymeren
- Onderzoekers observeren de reactie van silicaatglas met waterige oplossingen in realtime

 Wat zijn de kenmerken van gas?
Wat zijn de kenmerken van gas?  Wat is de duurste hernieuwbare energie?
Wat is de duurste hernieuwbare energie?  Wat is een actie die op een lichaam wordt uitgeoefend om de staat van rust of bewegingskracht te veranderen, heeft een grootte en richting?
Wat is een actie die op een lichaam wordt uitgeoefend om de staat van rust of bewegingskracht te veranderen, heeft een grootte en richting?  De ecologische voetafdruk van een volledig Engels ontbijt, en hoe het te verminderen?
De ecologische voetafdruk van een volledig Engels ontbijt, en hoe het te verminderen? Naar welk gebied van biologie zou een wetenschapper die de ontbossing in het regenwoud bestudeert dat waarschijnlijk is?
Naar welk gebied van biologie zou een wetenschapper die de ontbossing in het regenwoud bestudeert dat waarschijnlijk is?  Thermen naar KWH
Thermen naar KWH Nieuw model onthult vergeten influencers en slapende schoonheden van de wetenschap
Nieuw model onthult vergeten influencers en slapende schoonheden van de wetenschap Hoe heet het ion gevormd door een natriumatoom?
Hoe heet het ion gevormd door een natriumatoom?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

