
Wetenschap
Verbrandingsreacties begrijpen:hoe vuur brandstof omzet in energie
Een verbrandingsreactie, vaak afgekort tot RXN, is het chemische proces waarbij een brandbare stof reageert met zuurstof, waarbij warmte en licht vrijkomen.
Hoewel veel reacties warmte produceren, hebben echte verbrandingsreacties specifieke kenmerken gemeen:er is zuurstof bij betrokken, ze produceren energie en resulteren doorgaans in kooldioxide en waterdamp als er koolwaterstoffen bij betrokken zijn.
TL;DR
Verbranding =brandstof + zuurstof → warmte + licht. Koolwaterstoffen (hout, benzine, propaan) verbranden tot CO₂ en H₂O. Andere verbranding, zoals de verbranding van magnesium, genereert MgO zonder CO₂.
Hoe verbranding plaatsvindt
Om de verbranding te starten zijn drie elementen essentieel:een brandstof, zuurstof en een ontstekingsbron. Hoewel sommige materialen spontaan ontbranden, hebben de meeste een externe vonk of vlam nodig om hun moleculaire bindingen te verbreken.
Zodra de reactie begint, is de geproduceerde warmte voldoende om het proces in stand te houden, waardoor de brandstof in een continue vlam verandert totdat het reactieve materiaal is uitgeput. Onzuiverheden in de brandstof verschijnen als as, terwijl vocht de vlam kan doven door warmte te absorberen en water te verdampen.
Typisch verbrandingsvoorbeeld:methaan
Aardgaskachels zijn afhankelijk van de verbranding van methaan (CH₄). De reactie verloopt als:
CH₄ + 2O₂ → CO₂ + 2H₂O
Het waakvlammetje of de vonk levert de initiële energie, waarna de exotherme reactie warmte en licht genereert voor het koken.
Verbranding zonder koolwaterstoffen:Magnesium
Magnesium verbrandt in de lucht en vormt magnesiumoxide (MgO). De verbrandingsvergelijking is:
2Mg + O₂ → 2MgO
In tegenstelling tot koolwaterstofbranden stoot deze reactie geen CO₂ of H₂O uit, maar produceert intense hitte en een helderwitte vlam, wat illustreert dat verbranding geen traditionele brandproducten hoeft te produceren.
Belangrijkste punten
Verbranding is een gecontroleerde, exotherme reactie tussen brandstof en zuurstof die warmte en licht produceert. Het begrijpen van de werking ervan helpt bij het ontwerpen van veiligere motoren, efficiënte verwarmingen en betere brandveiligheidsprotocollen.
Lees hier meer over de chemie van verbranding .
 Beïnvloeden mensen de koolstofcyclus door vegetatie te vernietigen?
Beïnvloeden mensen de koolstofcyclus door vegetatie te vernietigen?  Snakes in Nevada
Snakes in Nevada Onbekende wateren:wetenschappers gaan de diepten van de Indische Oceaan verkennen
Onbekende wateren:wetenschappers gaan de diepten van de Indische Oceaan verkennen Canada, Amerikaanse hittegolf op steroïden door klimaatverandering, zeggen experts
Canada, Amerikaanse hittegolf op steroïden door klimaatverandering, zeggen experts Hittegolven en plotselinge overstromingen:ja, dit is het nieuwe normaal van Groot-Brittannië
Hittegolven en plotselinge overstromingen:ja, dit is het nieuwe normaal van Groot-Brittannië
Hoofdlijnen
- Welke kenmerken onderscheiden schimmels van planten?
- Wat is het belangrijkste doel van genregulatie in eukaryoten?
- Plant versus dierlijke cellen:belangrijkste overeenkomsten en verschillen
- Welke organismen zijn de producenten in de energiestroom van een ecosysteem?
- Hoe genen hun werkruimte delen
- Wat is de relatie tussen fysieke en biologische wetenschap?
- Wetenschappers laten zien dat de evolutie van complexe bioluminescente eigenschappen voorspelbaar kan zijn
- Er is een Y -vormige replicatievork aan elke kant van bubbel. Hoe worden de zijkanten genoemd?
- De functie van bacteriële endosporen is?
- Laatste onbekende structuur van HIV-1 opgelost, weer een stap in de strijd tegen het aids-virus
- Hoe u de antireflectiecoating veilig van een bril kunt verwijderen

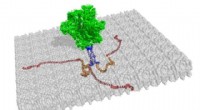
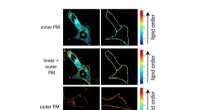
- Lipidenasymmetrie speelt een sleutelrol bij het activeren van immuuncellen
- Natuurkundigen ontwikkelen nieuwe methode om antibioticaresistente bacteriën te identificeren

- Waterstof als traphulp

 Hoe vaak meerdere bacteriën meerdere?
Hoe vaak meerdere bacteriën meerdere?  Om welke redenen is windenergie beter dan fossiele brandstoffen?
Om welke redenen is windenergie beter dan fossiele brandstoffen?  Hoeveel chromosomen zitten er bij mitose in elke dochtercel?
Hoeveel chromosomen zitten er bij mitose in elke dochtercel?  Onderzoekers gebruiken cryo-elektronenmicroscopie om te leren hoe DNA zich strak om nucleosomen wikkelt
Onderzoekers gebruiken cryo-elektronenmicroscopie om te leren hoe DNA zich strak om nucleosomen wikkelt  De rol van een verkeerde toewijzing van middelen in de productiviteit neemt af sinds de financiële crisis van 2007
De rol van een verkeerde toewijzing van middelen in de productiviteit neemt af sinds de financiële crisis van 2007 Identificeer de twee stukjes informatie die u moet weten Velocity een object?
Identificeer de twee stukjes informatie die u moet weten Velocity een object?  Wat betekent snelheid in de natuurkunde?
Wat betekent snelheid in de natuurkunde?  Wie stelde de relativiteitstheorie voor?
Wie stelde de relativiteitstheorie voor?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

