
Wetenschap
Hoe kleurveranderende chemische reacties verborgen moleculaire dynamiek onthullen
Door Claire Gillespie, bijgewerkt op 30 augustus 2022
Grafner/iStock/GettyImages
Een chemische reactie is niet altijd zichtbaar met het blote oog, maar sommige veroorzaken dramatische kleurveranderingen die experimenten gedenkwaardig maken. Wanneer reactanten zich combineren, vormen ze nieuwe producten waarvan de veranderde elektronische structuren hun lichtabsorptie en -emissie verschuiven, wat leidt tot een zichtbare kleurverandering.
Natriumhydroxide en fenolftaleïne
Fenolftaleïne is een universele pH-indicator. In zure media blijft het kleurloos, terwijl het in alkalische oplossingen lichtroze kleurt. Omdat natriumhydroxide een sterke base is, produceert het toevoegen van fenolftaleïne aan een NaOH-oplossing onmiddellijk de karakteristieke roze kleur. Andere veel voorkomende indicatoren zijn lakmoes, die verschuift van rood (zuur) naar blauw (alkalisch) en door paars gaat bij neutraliteit, en methyloranje, dat verandert van rood in geel naarmate de pH stijgt.
Zetmeel- en jodiumoplossingen
De zetmeeltest bevestigt de aanwezigheid van amylose. Een oplossing van jodium en kaliumjodide is licht oranjebruin; wanneer het wordt aangebracht op een zetmeelhoudend monster (zoals aardappel of brood), vormt het een diep blauwzwart complex. Deze kleurverandering is te wijten aan de vorming van een zetmeel-jodiumcomplex dat licht absorbeert in het zichtbare gebied.
Gehydrateerd kopercarbonaat
Koper dat wordt blootgesteld aan zuurstof, water en kooldioxide, oxideert tot gehydrateerd kopercarbonaat, waardoor de heldere roodbruine tint verandert in een groene patina. Een beroemd voorbeeld is het Vrijheidsbeeld:de koperen bekleding, oorspronkelijk rood, is de afgelopen eeuw geleidelijk naar groen verschoven. Hetzelfde proces vindt plaats op koperen munten en bij een daarmee samenhangende oxidatie roest ijzer tot roodbruine roest.
Blue Bottle-demonstratie
In het klassieke 'blauwe fles'-experiment oscilleert een mengsel van glucose, natriumhydroxide, methyleenblauw en water tussen blauw en kleurloos. Schudden introduceert zuurstof en oxideert methyleenblauw tot zijn blauwe vorm. Wanneer het schudden stopt, ontsnapt er zuurstof en wordt de kleurstof teruggebracht tot zijn kleurloze staat. Deze omkeerbare redoxcyclus is een schoolvoorbeeld van kinetische controle.
Niet alle kleurveranderingen duiden op een chemische reactie. Het mengen van rode en blauwe kleurstof levert paars water op, maar de kleurstoffen blijven chemisch verschillend; de verandering is slechts een mengsel van kleuren, geen nieuwe substantie.
Deze visuele aanwijzingen bieden intuïtief inzicht in onderliggende chemische processen, waardoor studenten en onderzoekers reacties in realtime kunnen volgen.
 In de reactie van aluminiummetaal en zuurstofgasoxide wordt gevormd, hoeveel mol O2 zal reageren met 2,0 Al?
In de reactie van aluminiummetaal en zuurstofgasoxide wordt gevormd, hoeveel mol O2 zal reageren met 2,0 Al?  Onderzoekers krijgen nieuwe inzichten in een dynamisch eiwit gericht op kankertherapie
Onderzoekers krijgen nieuwe inzichten in een dynamisch eiwit gericht op kankertherapie Onderzoekers synthetiseren genezende verbindingen in schorpioengif
Onderzoekers synthetiseren genezende verbindingen in schorpioengif Wat zijn de formules voor natriumethanoaat?
Wat zijn de formules voor natriumethanoaat?  Moleculen maken met tandenstokers en marshmallows
Moleculen maken met tandenstokers en marshmallows
 Koudwaterstromen kunnen een toevluchtsoord bieden tegen het veranderende klimaat
Koudwaterstromen kunnen een toevluchtsoord bieden tegen het veranderende klimaat NASA-satelliet vindt een langgerekte tropische storm Rene veroorzaakt door windschering
NASA-satelliet vindt een langgerekte tropische storm Rene veroorzaakt door windschering Waarom kopen mensen brood en melk voordat er een storm losbarst?
Waarom kopen mensen brood en melk voordat er een storm losbarst?  China, Economische ontwikkeling in India sleutel tot het bereiken van de millenniumdoelstelling voor veilig drinkwater
China, Economische ontwikkeling in India sleutel tot het bereiken van de millenniumdoelstelling voor veilig drinkwater Fosfaatgesteente een effectieve meststof in Kenia
Fosfaatgesteente een effectieve meststof in Kenia
Hoofdlijnen
- Welke cel wordt waargenomen als A de vorming van een contractiele ring vertoont net voorafgaand aan cytoplasmatische divisie?
- Wat is de biologische rol van zetmeel?
- Wat is de wetenschap van het classificeren van het organisme?
- Wat is Mitochondna?
- Is de volgende vraag waar of onwaar classificeren, maakt het gemakkelijker om organismen te vergelijken en te contrasteren hun actiesgedragfuncties?
- Wat voor soort overerving wanneer het genotype noch homozygoot of heterozygoot is?
- Wat zijn de zes menselijke levensprocessen?
- Hoe past een mug in voedselweb?
- Wat is het doel van het manipuleren van DNA?
- Onderzoekers ontdekken methode om kankerverwekkende formaldehydeafgifte uit hout in huis te beheersen

- Atomair dunne perovskieten boost voor toekomstige elektronica

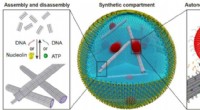
- Nog een stap in de richting van synthetische cellen
- Nieuw biosensor-zymonzuur toont veranderingen in pH-waarde

- De samenstelling van staal uitgelegd:de chemische formule van staal

 Wat is de naam voor een regio die een weerspiegeling is van menselijke gevoelens en attitudes?
Wat is de naam voor een regio die een weerspiegeling is van menselijke gevoelens en attitudes?  Duitsland zet stappen om btw-fraude in e-commerce aan te pakken
Duitsland zet stappen om btw-fraude in e-commerce aan te pakken Wat is een grond met gemiddelde textuur die van allerlei verschillende mineralen is gemaakt?
Wat is een grond met gemiddelde textuur die van allerlei verschillende mineralen is gemaakt?  Een rots bevindt zich op de top van een berg die 22 meter hoge massa 48 kg Hoeveel potentiële energie heeft?
Een rots bevindt zich op de top van een berg die 22 meter hoge massa 48 kg Hoeveel potentiële energie heeft?  De Hubble Space Telescope draait de aarde en verzendt afbeeldingen van verre objecten. Waarom vormt zich beter dan de optische telescopen die op het land worden gebruikt?
De Hubble Space Telescope draait de aarde en verzendt afbeeldingen van verre objecten. Waarom vormt zich beter dan de optische telescopen die op het land worden gebruikt?  Als het orbitale vlak van de manen precies was uitgelijnd met ecliptisch vlak?
Als het orbitale vlak van de manen precies was uitgelijnd met ecliptisch vlak?  Hoe een verandering in potentiële energie te berekenen
Hoe een verandering in potentiële energie te berekenen Een speler schopt een voetbal van het maaiveld en stuurt deze in een hoek van 30 graden snelheid 26 ms Wat is de horizontale snelheidscomponent tot het dichtst bij de tiende?
Een speler schopt een voetbal van het maaiveld en stuurt deze in een hoek van 30 graden snelheid 26 ms Wat is de horizontale snelheidscomponent tot het dichtst bij de tiende?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

