
Wetenschap
Wat drijft waterstofbinding aan?
Waterstofbinding is een hoeksteen van de chemie en ondersteunt het gedrag van talloze stoffen, met name water. Het begrijpen waarom deze bindingen ontstaan is essentieel voor een dieper begrip van intermoleculaire krachten en chemisch gedrag.
TL;DR
Waterstofbinding ontstaat wanneer elektronegatieve atomen (O, N, F) gedeelde elektronen wegtrekken van waterstof, waardoor permanente dipolen ontstaan die elkaar over moleculen heen aantrekken.
Elektronegativiteit en permanente dipoolmomenten
Wanneer twee atomen elektronen delen, hangt de verdeling van de elektronendichtheid af van hun elektronegativiteiten. Identieke elektronegativiteiten leveren een gelijk aandeel op, maar wanneer een atoom elektronegatiever is, clusteren de gedeelde elektronen er dichter bij. Deze onbalans geeft het meer elektronegatieve atoom een lichte negatieve lading en het minder elektronegatieve atoom een lichte positieve lading, wat resulteert in een permanent dipoolmoment:een polair molecuul.
Hoe waterstofbruggen ontstaan
Polaire moleculen bezitten zowel een positief geladen waterstofzijde als een negatief geladen heteroatoomzijde. Wanneer de waterstof van het ene molecuul het elektronegatieve atoom van een ander molecuul nadert, vindt er een aantrekkelijke, intermoleculaire interactie – waterstofbinding – plaats. Hoewel ze zwakker zijn dan covalente bindingen (ongeveer een tiende van de sterkte), zijn deze bindingen cruciaal bij het bepalen van de fysische eigenschappen van vloeistoffen en vaste stoffen.
Waterstofbinding in water
Water (H2 O) is een prachtig voorbeeld van waterstofbruggen. De hogere elektronegativiteit van zuurstof trekt de elektronendichtheid naar zich toe, waardoor waterstofatomen gedeeltelijk positief blijven. Elk watermolecuul kan twee waterstofbruggen doneren (via zijn twee H-atomen) en er twee accepteren (via zijn twee alleenstaande paren aan zuurstof). Dit uitgebreide netwerk verhoogt het kookpunt van water boven dat van vergelijkbare moleculen als ammoniak en verklaart de lagere dichtheid van ijs als gevolg van een open, waterstofgebonden rooster.
 Berekening van het aantal moleculen in 1 kg waterstofgas:een stapsgewijze handleiding
Berekening van het aantal moleculen in 1 kg waterstofgas:een stapsgewijze handleiding  Wat maakt CO2-oplosbaar in H2O?
Wat maakt CO2-oplosbaar in H2O?  Welke methode voor het behandelen van waterdoodmicroben en verwijdert andere verontreinigingen zoals zware metalen?
Welke methode voor het behandelen van waterdoodmicroben en verwijdert andere verontreinigingen zoals zware metalen?  Voorspel en leg uit welke van de volgende systemen elektrisch geleiders zijn ASOLID NaCl bmolten kan waterige oplossing NaCl?
Voorspel en leg uit welke van de volgende systemen elektrisch geleiders zijn ASOLID NaCl bmolten kan waterige oplossing NaCl?  Welk aspect van een chemische reactie wordt beïnvloed door enzymen?
Welk aspect van een chemische reactie wordt beïnvloed door enzymen?
 Onderzoekers bestuderen hoe goed de habitat van het saliehoen andere soorten beschermt
Onderzoekers bestuderen hoe goed de habitat van het saliehoen andere soorten beschermt  Hoe vuurvliegjes hun betoverende gloed produceren
Hoe vuurvliegjes hun betoverende gloed produceren  Hoe veranderen mensen hun abiotische factoren in habitat?
Hoe veranderen mensen hun abiotische factoren in habitat?  NASA ziet krachtige tropische cycloon Enawo aan land komen in Madagaskar
NASA ziet krachtige tropische cycloon Enawo aan land komen in Madagaskar De economische waarde van insectenbestuivingsdiensten is veel hoger dan eerder werd gedacht in de VS
De economische waarde van insectenbestuivingsdiensten is veel hoger dan eerder werd gedacht in de VS
Hoofdlijnen
- Zijn er meer organismen in het geslachtsniveau dan op volgorde niveau?
- Welke structuur in het neuron ontvangt informatie van een andere zenuwcel?
- Noem drie delen die elke cel heeft?
- Hoe weet een bacterie dat het tijd is om zich te splitsen?
- Wat voor soort wetenschapper bestudeert de oceaan?
- De bodemtemperatuur kan de verspreiding van plagen in gewassen voorspellen
- Hoe beïnvloedt een enzym het menselijk leven?
- Wat zijn de 5 nucleotiden die DNA en RNA vormen?
- Wat is het voordeel van fosforyleringscascade?
- Moleculen net zo gemakkelijk vastbinden als veters

- Wetenschappers bedenken diervrije testen van dodelijke neurotoxines

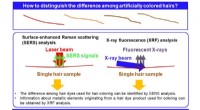
- Binnen een haarbreedte - forensische identificatie van enkel geverfde haarstreng nu mogelijk
- Nieuwe methode verdubbelt suikerproductie uit planten meer dan

- Onderzoekers brengen de bling om implantaten te verbeteren

 Waar wordt siltstone over de hele wereld gevonden?
Waar wordt siltstone over de hele wereld gevonden?  Meteotsunami's:hoe wind catastrofale golven kan genereren
Meteotsunami's:hoe wind catastrofale golven kan genereren  6-delige activiteiten voor lesgeven aan potentiële en kinetische energie
6-delige activiteiten voor lesgeven aan potentiële en kinetische energie  Op welke factoren hangt de kinetische energie van een object af van (top)?
Op welke factoren hangt de kinetische energie van een object af van (top)?  Hallucinogene planten afkomstig uit de Verenigde Staten
Hallucinogene planten afkomstig uit de Verenigde Staten  Monopoly is 100 jaar geleden ontworpen om de gevaren van het kapitalisme te onderwijzen
Monopoly is 100 jaar geleden ontworpen om de gevaren van het kapitalisme te onderwijzen Wat zijn enkele redenen waarom mensen in een park de ene plant boven de andere zouden verkiezen?
Wat zijn enkele redenen waarom mensen in een park de ene plant boven de andere zouden verkiezen?  Nieuwe algoritmen trainen AI om specifiek slecht gedrag te voorkomen
Nieuwe algoritmen trainen AI om specifiek slecht gedrag te voorkomen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

