
Wetenschap
Conversiefactoren beheersen in chemische formules:een praktische gids
In de scheikunde vertegenwoordigen subscripts in formules kwantitatieve relaties, niet alleen symbolen. Elk subscript codeert voor een conversiefactor die elementen, moleculen en meetbare hoeveelheden met elkaar verbindt. Het begrijpen van deze verborgen vermenigvuldigers, vaak dimensionale analyse genoemd, is essentieel voor nauwkeurige berekeningen op het gebied van stoichiometrie, laboratoriumwerk en chemische technologie.
Molen verbindingen naar molen elementen
In een chemische formule geeft een geheel getal subscript aan hoeveel mol van het voorgaande element (of groep) aanwezig is per mol van de verbinding. Water (H₂O) bevat bijvoorbeeld twee mol waterstof en één mol zuurstof per mol H2O. De bijbehorende conversiefactoren zijn:
- 2molH / 1molH₂O
- 1molO / 1molH₂O
Mollen naar atomen en moleculen
Een mol wordt gedefinieerd als 6,022×10²³ entiteiten:atomen, ionen of moleculen. De conversiefactor is daarom:
- 6,022×10²³atomen (of moleculen) / 1mol
Mollen naar Gram
Grammen zorgen voor een meetbare massa in het laboratorium. De conversiefactor voor een element komt van de atomaire massa (meestal vermeld onder het symbool in het periodiek systeem). Germanium heeft bijvoorbeeld een atoommassa van 72,61 gmol⁻¹, dus:
- 72,61gGe / 1molGe
Percentages naar Mol
Sommige formules bevatten gedeeltelijke subscripts die gewichts- of molpercentages weergeven in plaats van hele getallen. Als u een op percentages gebaseerde compositie wilt omzetten in subscripts van gehele getallen, deelt u 100% door de kleinste procentuele waarde en vermenigvuldigt u vervolgens elk percentage met die factor. Voorbeeld:voor C₀.₂H₀.₆O₀.₂ is het kleinste percentage 20%. Als je 100 deelt door 20, krijg je 5. Als je elk percentage met 5 vermenigvuldigt, krijg je de vereenvoudigde formule CH₃O.
Als u deze conversiefactoren beheerst, beschikt u over de precisie die nodig is voor stoichiometrische berekeningen, materiaalbalans en analytische chemie.
 Digitale gegevens van bewaarde planten en dieren veranderen de manier waarop wetenschappers de wereld verkennen
Digitale gegevens van bewaarde planten en dieren veranderen de manier waarop wetenschappers de wereld verkennen  Orkaan Genevieve teistert Mexicos Baja met wind en regen
Orkaan Genevieve teistert Mexicos Baja met wind en regen Studie werpt nieuw licht op de manier waarop Schotse bevers omgaan met het milieu
Studie werpt nieuw licht op de manier waarop Schotse bevers omgaan met het milieu  Gletsjers en raadselachtige steenstrepen in de Ethiopische hooglanden
Gletsjers en raadselachtige steenstrepen in de Ethiopische hooglanden Onderzoekers van CLOUD-experimenten laten zien dat emissies uit bossen de allereerste fase van wolkenvorming beïnvloeden
Onderzoekers van CLOUD-experimenten laten zien dat emissies uit bossen de allereerste fase van wolkenvorming beïnvloeden
Hoofdlijnen
- Hoe gebruiken een genetische stambomen?
- Onderzoek werpt nieuw licht op hoe Salmonella ‘sterft’ bij lage temperaturen
- Bacteriën reproduceren meestal aseksueel, maar soms wisselen ze genetische informatie uit tijdens conjugatie Welke structuur vormen dit proces dat wordt gebruikt om info?
- Welke lichaamssystemen beschermen de tegen vreemde stoffen?
- Hoe maken wetenschappers die verschillende talen spreken hun gegevens begrijpelijk voor elkaar?
- Wat is typisch en samengesteld uit een kern -DNA of RNA omgeven door eiwitjas?
- Stopt de celdeling wanneer een persoon groeit?
- Bioloog kan de aminozuursequentie van hetzelfde eiwit van twee of meer soortensequenties vergelijken, anders zijn heel vergelijkbaar met wat doen overeenkomsten en verschillen ons vertellen?
- Welke wetenschappers hebben de dubbele helixvorm van DNA ontdekt?
- De weg verlichten naar poreuze elektronica en sensoren

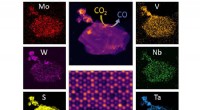
- Nieuwe 2D-legering combineert vijf metalen, breekt koolstofdioxide af
- Plasma-eiwit kan veelbelovend zijn voor wondsteigers

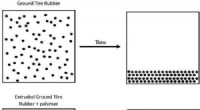
- Polymeren effenen de weg voor een breder gebruik van gerecyclede banden in asfalt
- Cryo-elektronenmicroscopie werpt nieuw licht op batterijen

 Wat eten we? Onderzoek naar het dieet van dolfijnen
Wat eten we? Onderzoek naar het dieet van dolfijnen  Hoe kan het uitsterven van een enkele soort beïnvloeden hoe een ecosysteem functioneert?
Hoe kan het uitsterven van een enkele soort beïnvloeden hoe een ecosysteem functioneert?  Nucleaire oorlog zou een wereldwijde hongersnood veroorzaken en miljarden doden, zo blijkt uit onderzoek
Nucleaire oorlog zou een wereldwijde hongersnood veroorzaken en miljarden doden, zo blijkt uit onderzoek Hoe maak je ijzerchloride?
Hoe maak je ijzerchloride?  Welke rotsen zijn poreus?
Welke rotsen zijn poreus?  Geluidsoverlast het hardst in zwarte wijken, gescheiden steden
Geluidsoverlast het hardst in zwarte wijken, gescheiden steden Hoeveel wegen metamorfe rotsen in gram?
Hoeveel wegen metamorfe rotsen in gram?  Studie:Activisme en burgerlijke ongehoorzaamheid helpen de wetenschap van klimaatverandering te communiceren
Studie:Activisme en burgerlijke ongehoorzaamheid helpen de wetenschap van klimaatverandering te communiceren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

